Clear Sky Science · fr
Plateforme de diagnostic sur site CRISPR « tout-en-un » pour la détection rapide, spécifique et sensible du HPV 16 sans pré-amplification
Pourquoi identifier un seul type de virus est réellement important
Le cancer du col de l’utérus est souvent lié à une infection par des papillomavirus humains (HPV), mais tous les types d’HPV n’ont pas le même niveau de risque. Les médecins ont donc besoin de tests capables de distinguer de manière fiable ces virus très proches, en particulier le type à haut risque appelé HPV16. Le problème est que les tests génétiques actuels peuvent parfois confondre des parents proches, entraînant de fausses alertes ou des cas manqués. Cette étude présente une nouvelle méthode de test qui améliore nettement à la fois la précision et la praticité, visant à apporter un sous-typage HPV précis en clinique et au point de soin.
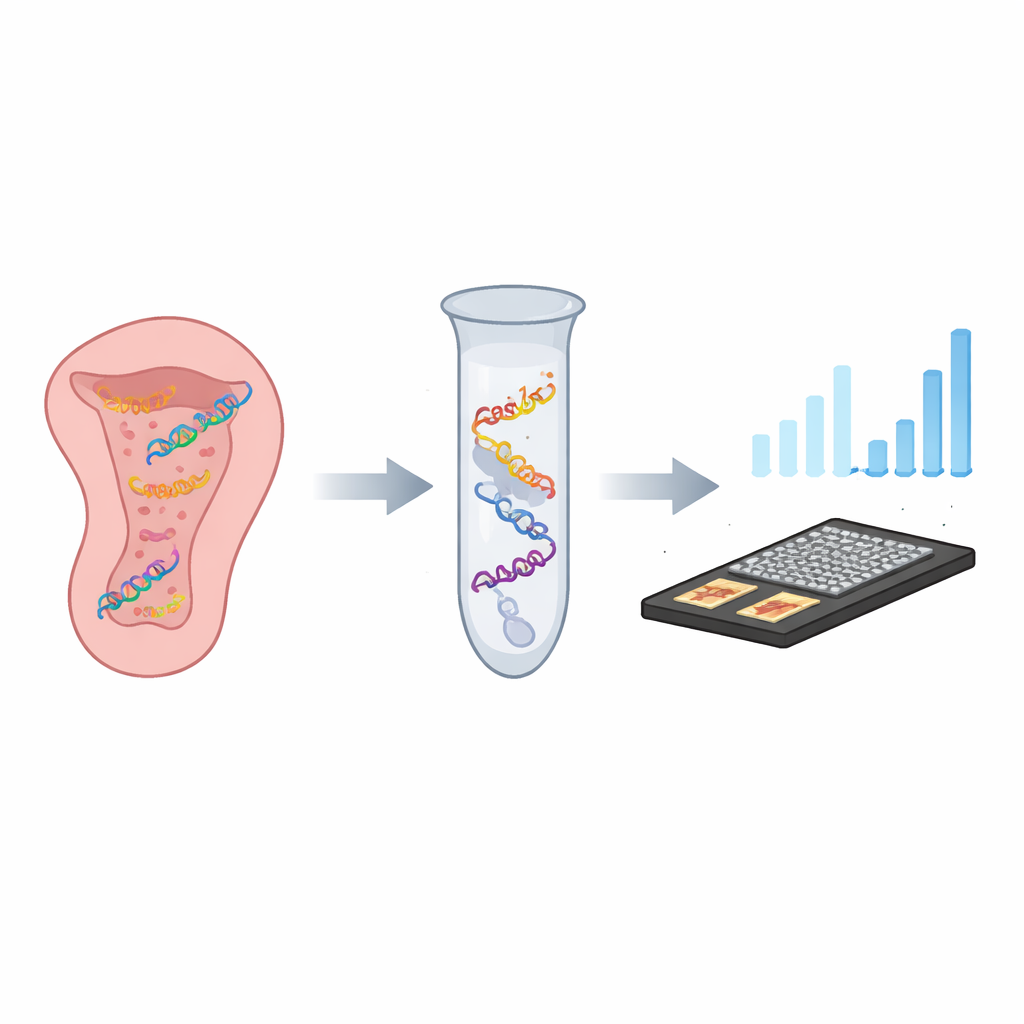
Une serrure et une clé moléculaires intelligentes
Les chercheurs ont conçu un test en tube unique qu’ils appellent CASTSA, qui combine deux idées puissantes : la précision du système CRISPR, une machinerie de ciblage génétique adaptée des bactéries, et la capacité d’amplification du signal de la PCR, la méthode standard de copie de l’ADN. Dans CASTSA, une protéine CRISPR nommée Cas12a est guidée vers la séquence génétique du HPV16 par un court ARN « clé ». Lorsqu’elle trouve la correspondance exacte plus un motif court adjacent requis, Cas12a coupe l’ADN viral en un point prévisible. Cette coupure crée une extrémité caractéristique sur un brin d’ADN qui sert de point de départ unique pour l’amplification. Les autres types d’HPV, même avec des séquences très similaires, ne sont soit pas coupés soit ne génèrent pas le bon point de départ, et ne sont donc pas amplifiés.
Transformer une petite coupure en un signal fort
Pour convertir la coupure CRISPR en signal détectable, l’équipe a conçu une amorce d’ADN spéciale appelée amorce terminale spécifique. Cette amorce ne s’attache correctement qu’au brin produit par la coupure de Cas12a, puis se replie sur elle-même comme une épingle à cheveux et aide à construire un gabarit stable pour la PCR. Des séquences d’amorces « universelles » supplémentaires se lient ensuite et entraînent une réaction PCR en temps réel conventionnelle. De manière cruciale, l’amplification n’a lieu que si Cas12a a d’abord effectué sa tâche et si l’amorce se replie correctement, créant deux niveaux de vérification. Cette architecture réduit fortement la probabilité que de l’ADN partiellement correspondant et non ciblé soit amplifié accidentellement, répondant à une faiblesse fréquente des tests CRISPR antérieurs qui reposaient sur une étape de pré-amplification séparée.
Tout dans un seul tube, avec moins d’erreurs
Un progrès pratique clé est que la coupure par CRISPR et l’amplification par PCR se déroulent ensemble dans le même tube scellé, évitant la nécessité d’ouvrir les tubes entre les étapes — une source majeure de contamination dans de nombreux protocoles de laboratoire. Les auteurs ont finement ajusté les conditions réactionnelles, en particulier le taux de magnésium, de sorte que Cas12a et l’enzyme copiant l’ADN fonctionnent bien sans favoriser de réactions parasites. Ils ont montré que leur configuration en « one‑pot » peut distinguer fidèlement le HPV16 de plusieurs autres types à haut risque, notamment HPV18, 33, 45 et 52, malgré des régions génétiques fortement conservées. Comparé à la PCR en temps réel standard seule, ou à des tests CRISPR qui amplifient d’abord l’ADN puis effectuent la détection CRISPR, CASTSA a produit beaucoup moins de signaux trompeurs provenant de types HPV hors cible.
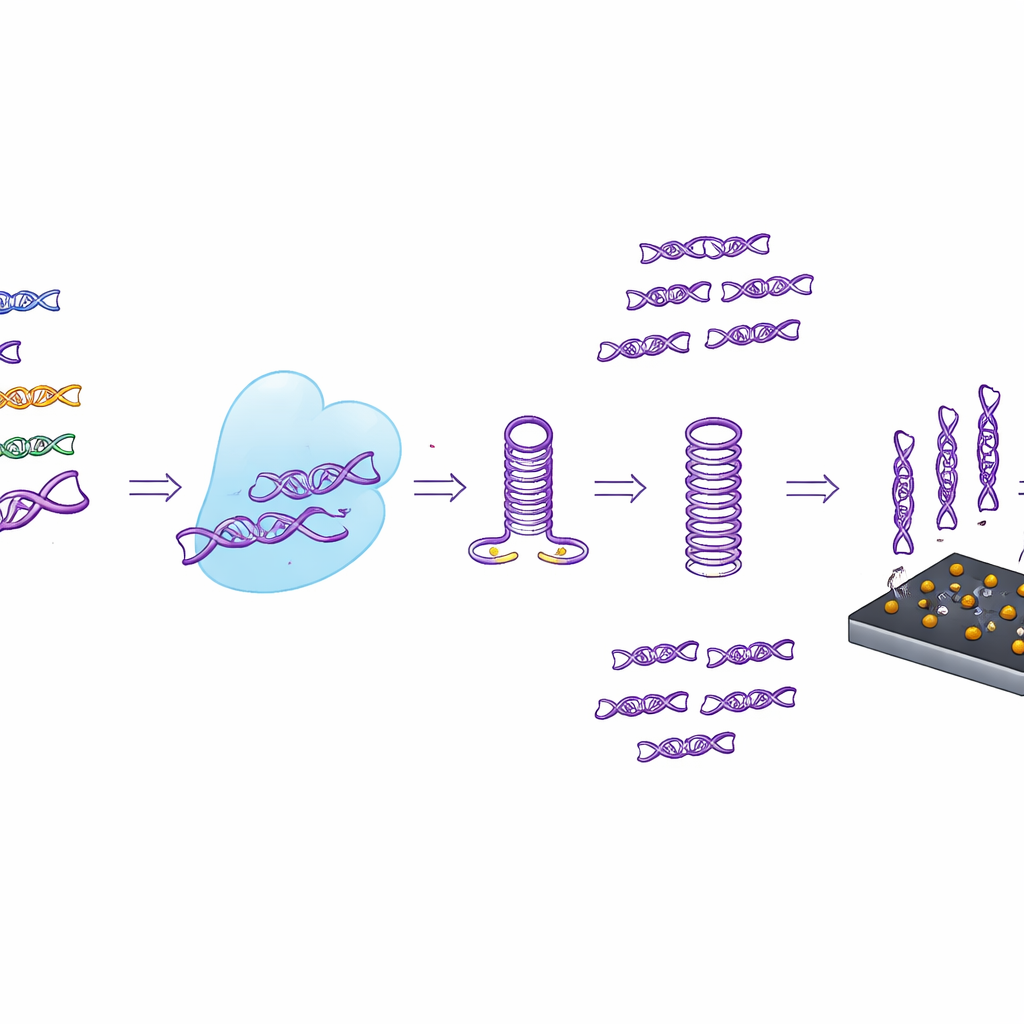
Du tube au capteur portable
Plutôt que de se limiter aux lectures fluorescentes, les chercheurs ont également couplé CASTSA à un capteur électrochimique compact fabriqué à partir de graphène induit par laser. Cette surface carbonée poreuse et hautement conductrice est décorée de nanoparticules d’or portant des brins de capture conçus pour se lier uniquement aux produits d’amplification CASTSA du HPV16. Lorsque ces produits se fixent, le courant électrique à travers le capteur varie de manière mesurable. En utilisant une matrice à quatre électrodes — trois points de mesure et un contrôle d’arrière-plan intégré — l’appareil peut soustraire le bruit dû aux adhérences non spécifiques. Lors d’essais, ce système intégré a détecté aussi peu que 18 copies de la cible HPV16 par réaction, surpassant la sensibilité de la fluorescence seule et conservant une excellente répétabilité.
Comment cela pourrait transformer le dépistage du HPV
Pour évaluer le fonctionnement de la méthode en conditions réelles, l’équipe a testé 20 échantillons cliniques connus positifs pour le HPV16 et 10 échantillons de donneurs sains. CASTSA, tant en version fluorescente que couplée au capteur à base de graphène, était en parfait accord avec les tests PCR hospitaliers standards. Dans le même temps, il a montré une meilleure capacité à ignorer d’autres types HPV à haut risque qui causent souvent de la confusion. Pour les patients, cela pourrait signifier moins de résultats ambigus et des décisions de suivi et de traitement plus confiantes. Plus largement, la stratégie CASTSA — reconnaissance par CRISPR d’abord, amplification ensuite, le tout dans un tube scellé — offre une feuille de route pour des tests génétiques hautement spécifiques et à faible risque de contamination, adaptables à de nombreux pathogènes et mutations, en particulier dans des contextes nécessitant des réponses rapides et fiables.
Citation: Chen, Y., Chen, Y., Zhang, C. et al. One-pot CRISPR-based point of care platform for rapid, specific and sensitive detection of HPV 16 without pre-amplification. Microsyst Nanoeng 12, 81 (2026). https://doi.org/10.1038/s41378-025-01130-y
Mots-clés: Détection HPV16, Diagnostics CRISPR, Tests basés sur la PCR, Bio-capteur électrochimique, Test au point de soin