Clear Sky Science · fr
Microscopie de balayage d’image interférométrique pour l’imagerie sans marquage à 120 nm de résolution latérale à l’intérieur de cellules vivantes
Observer des cellules vivantes sans colorants ajoutés
La biologie moderne s’appuie souvent sur des marqueurs fluorescents pour révéler l’architecture cachée à l’intérieur des cellules. Mais ces marqueurs peuvent stresser les cellules, modifier leur comportement, et parfois ne peuvent tout simplement pas être utilisés sur des échantillons fragiles ou difficiles à manipuler. Cet article présente une nouvelle manière d’observer la vie à l’intérieur de cellules vivantes avec un niveau de détail élevé — sans ajouter de colorants ni d’étiquettes génétiques — promettant des observations plus douces, plus longues et plus naturelles du fonctionnement réel des cellules.
Regarder les cellules par leur diffusion de la lumière
La méthode s’appuie sur une famille de techniques qui ne dépendent pas de la fluorescence, mais mesurent plutôt la façon dont de petites structures diffusent la lumière. Une de ces méthodes, la microscopie de diffusion interférométrique (iSCAT), mélange la lumière diffusée par un objet nanoscopique avec une réflexion de référence provenant d’une surface en verre. Le motif d’interférence résultant est extrêmement sensible à des particules très petites comme des protéines, des virus ou des vésicules. L’iSCAT a jusqu’ici donné les meilleurs résultats sur des échantillons simples et propres, par exemple des particules isolées sur du verre. En revanche, l’appliquer profondément à l’intérieur de cellules vivantes a été difficile parce que les cellules sont denses et désordonnées : de nombreux événements de diffusion qui se chevauchent produisent un fond ponctué qui masque les détails fins.
Combiner deux idées pour une imagerie plus nette et plus douce
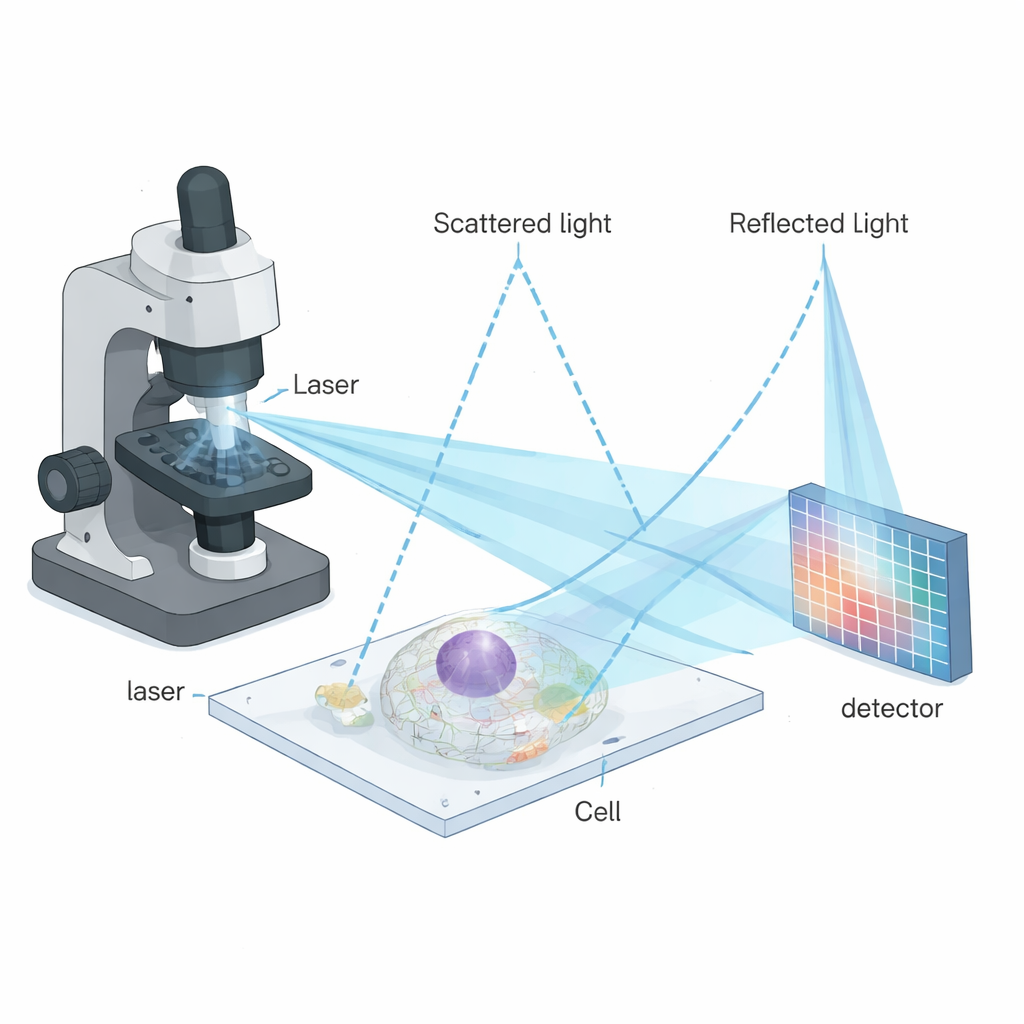
Pour surmonter ces limites, les auteurs ont combiné l’iSCAT avec une stratégie d’imagerie puissante appelée microscopie de balayage d’image (ISM). En ISM, l’échantillon est balayé point par point par un faisceau focalisé, et au lieu d’utiliser un unique détecteur, une matrice de pixels détecteurs enregistre de nombreuses vues légèrement décalées de chaque point. En réalignant et en combinant astucieusement ces vues, on peut affiner l’image finale sans perdre de photons précieux. La nouvelle technique — microscopie de balayage d’image interférométrique, ou iISM — adapte cette idée aux signaux plus complexes et sensibles à la phase de la diffusion interférométrique. Le microscope utilise un laser bleu, des optiques spéciales pour symétriser la polarisation de la lumière, et une caméra sensible pour enregistrer la lumière diffusée et réfléchie à chaque position de balayage. Un flux de traitement informatique sur mesure réaffecte ensuite l’information des pixels d’une manière qui respecte la nature ondulatoire du signal, produisant des images d’environ 120 nanomètres de résolution latérale, soit approximativement deux fois plus fines que l’optique limitée par diffraction standard.
Des algorithmes intelligents transforment des motifs bruités en images nettes
Parce que les signaux interférométriques véhiculent à la fois l’intensité et l’information de phase, les traitements habituels de l’imagerie par fluorescence ne suffisent pas. Les auteurs ont conçu une procédure adaptative de réaffectation des pixels (APR) spécifiquement adaptée à la lumière cohérente. D’abord, ils transforment chaque petit motif interférométrique en une carte de « variance radiale » qui met en évidence les centres de symétrie sans tenir compte du fait que le signal soit positif ou négatif. Cette étape convertit effectivement des franges d’interférence compliquées en images qui se comportent davantage comme des images d’intensité conventionnelles. Ensuite, en utilisant un logiciel open source, ils déterminent de combien l’image fournie par chaque pixel du détecteur est décalée par rapport au centre, puis les recentrent avant de les additionner. Cet alignement affiné concentre le signal utile tout en moyenne le bruit, augmentant le rapport contraste-sur-bruit d’environ un facteur quatre par rapport à une image iSCAT confocale fortement diaphragmatée, et ce au même niveau d’illumination.
Observer organites et cytosquelettes en action
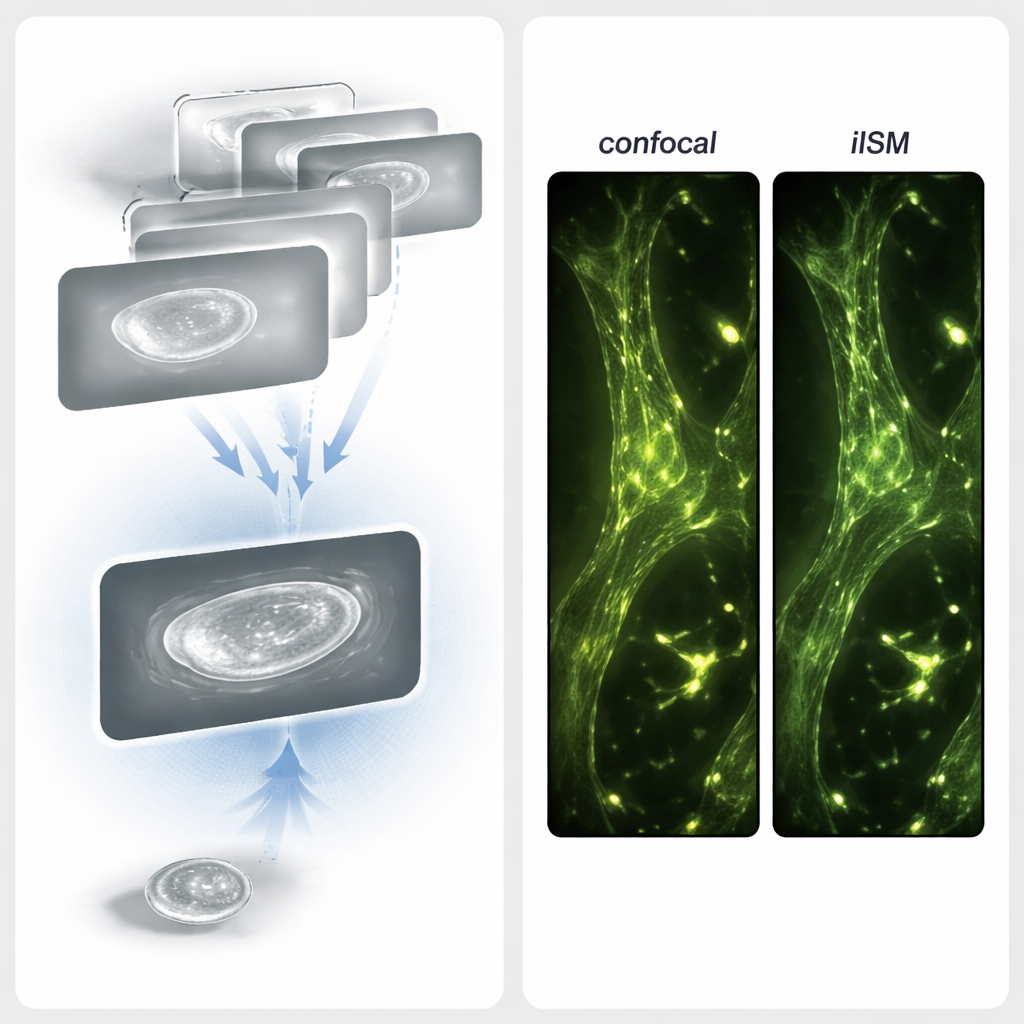
Grâce à ces avancées techniques, l’équipe a testé l’iISM sur des cellules COS-7 vivantes pour évaluer ses performances en conditions pratiques. À une puissance d’illumination très faible — environ dix fois moindre par point focalisé que ce que les confocaux conventionnels utilisent typiquement — ils ont pu distinguer clairement des organites clés : le réticulum endoplasmique, les mitochondries, des vésicules, le cytosquelette d’actine, la membrane plasmique et de fines structures en bord d’avance appelées lamellipodes. Parce que le contraste interférométrique dépend fortement de la position verticale, des organites semblables pouvaient apparaître avec un contraste positif ou négatif, révélant des différences de hauteur subtiles de seulement quelques centaines de nanomètres. En enregistrant des séquences temporelles, ils ont suivi des vésicules en mouvement et la remodelage des tubules du réticulum endoplasmique sur plusieurs minutes, sans dommages phototoxiques évidents et sans signe que l’imagerie perturbait le comportement des cellules.
Faire correspondre les vues sans marquage aux cartographies fluorescentes
Pour vérifier que les images sans marquage reflètent réellement des structures cellulaires, les chercheurs ont également réalisé des mesures combinées iISM et ISM en fluorescence sur des cellules fixées. Ils ont marqué le cytosquelette d’actine avec un colorant fluorescent rouge et enregistré des images de fluorescence super-résolues parallèlement aux images iISM sans marquage de la même région. Lors de la superposition des deux canaux, les filaments d’actine brillants du canal de fluorescence coïncidaient étroitement avec des structures filamenteuses dans les images iISM. Dans certaines régions, l’iISM a même révélé des détails de diffusion supplémentaires — comme des variations le long des filaments ou des structures voisines non marquées, telles que des adhésions focales — invisibles dans le canal de fluorescence. Ensemble, ces résultats montrent que l’iISM peut confirmer des structures connues tout en dévoilant des informations complémentaires sur l’environnement non marqué.
Une nouvelle fenêtre sur les cellules, avec moins de perturbation
Pour les non-spécialistes, le message principal est que l’iISM offre un moyen de voir des détails fins à l’intérieur de cellules vivantes sans les rendre artificiellement luminescentes. Elle combine la sensibilité de la diffusion interférométrique avec le pouvoir d’affinement de la microscopie de balayage d’image, atteignant environ 120 nanomètres de résolution tout en utilisant beaucoup moins de lumière que de nombreux microscopes existants. Parce qu’elle est construite à partir de composants déjà courants dans les systèmes confocaux avancés, elle peut en principe être ajoutée à des instruments commerciaux. À l’avenir, l’iISM pourrait être associée à la fluorescence traditionnelle, à des détecteurs rapides ou même à des « colorations virtuelles » par apprentissage automatique pour suivre des infections, le transport de cargo ou des réarrangements du cytosquelette dans des cellules dans des conditions plus proches de leur état naturel non perturbé.
Citation: Küppers, M., Moerner, W.E. Interferometric Image Scanning Microscopy for label-free imaging at 120 nm lateral resolution inside live cells. Light Sci Appl 15, 129 (2026). https://doi.org/10.1038/s41377-026-02210-y
Mots-clés: imagerie sans marquage, microscopie de cellules vivantes, diffusion interférométrique, super-résolution, organites cellulaires