Clear Sky Science · fr
Létalité synthétique de l’inhibition de MCL-1 et de la thérapie CAR-T dans les lymphomes B agressifs
Pourquoi cela compte pour le traitement du cancer
Les lymphomes B agressifs sont des cancers du sang à croissance rapide qui rechutent souvent après traitement. Même des approches puissantes et récentes comme la thérapie CAR-T, qui reprogramme les propres cellules immunitaires du patient pour attaquer la tumeur, échouent chez environ la moitié des patients à terme. Cette étude explore une façon de retourner cette faiblesse en avantage : utiliser un médicament ciblant une protéine clé de survie des cellules lymphomateuses pour à la fois tuer la tumeur et rendre les cellules résiduelles plus faciles à éliminer par les CAR-T.
Le problème des cellules lymphomateuses rebelles
Les lymphomes B agressifs sont souvent entraînés par une activité excessive d’un gène appelé MYC, qui pousse les cellules à se diviser rapidement et les aide aussi à se dissimuler du système immunitaire. Les traitements standards et même la thérapie CAR-T peuvent laisser derrière eux de petites poches de cellules lymphomateuses qui tolèrent les médicaments et provoquent ensuite des rechutes. Ces cellules « persistantes » et résistantes vivent dans un microenvironnement tumoral encombré par des cellules immunitaires suppressives qui tiennent les lymphocytes tueurs à distance. Les auteurs se sont demandé si bloquer MCL-1, une protéine dont les cellules lymphomateuses dépendent pour éviter l’autodestruction, pouvait révéler une faiblesse cachée de ce système.
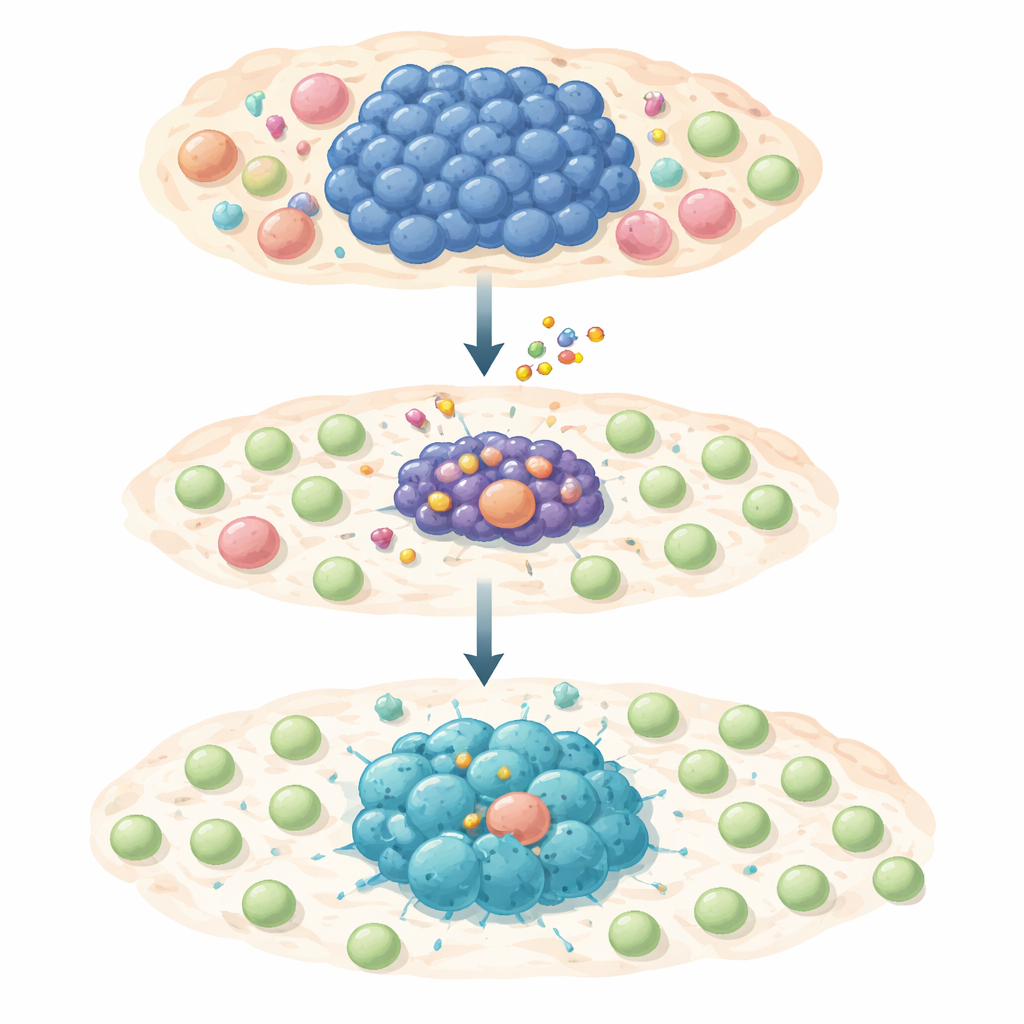
Une attaque en deux temps contre la survie et la dissimulation tumorales
L’équipe a testé un inhibiteur sélectif de MCL-1, S63845, sur un large panel de lignées cellulaires humaines de lymphome dépendantes de MYC. La plupart de ces cellules cancéreuses étaient très sensibles au médicament et déclenchaient l’apoptose lorsque MCL-1 était bloqué. Cependant, une petite fraction a survécu à une exposition de court ou long terme et est devenue tolérante au traitement ou totalement résistante. En examinant ces survivantes en détail, les chercheurs ont observé que l’activité de MYC était diminuée tandis qu’une autre molécule, STAT1, et sa voie d’alerte par interférons étaient activées. Ce basculement a induit l’expression de gènes responsables de signaux inflammatoires et de chimiokines — des « fumées » moléculaires qui peuvent attirer des lymphocytes T dans la zone tumorale.
Réveiller le voisinage immunitaire
Pour voir comment cela se traduit in vivo, les auteurs ont traité des souris porteuses de lymphomes pilotés par MYC avec une faible dose de l’inhibiteur de MCL-1. Le médicament a réduit la charge tumorale tout en épargnant les cellules B normales, mais son effet allait au-delà d’un simple amaigrissement tumoral. Les tumeurs traitées présentaient davantage de lymphocytes T CD4 et CD8, moins de lymphocytes T épuisés, moins de lymphocytes T régulateurs et moins de cellules myéloïdes suppressives, autant de signes d’un microenvironnement plus favorable à l’immunité. Le séquençage ARN unicellulaire des cellules tumorales et environnantes a confirmé que les cellules lymphomateuses résiduelles avaient un MYC réduit, un STAT1 augmenté et des signaux d’interféron et inflammatoires renforcés, tandis que le tissu environnant était repeuplé de cellules T et de cellules NK actives plutôt que de cellules suppressives.
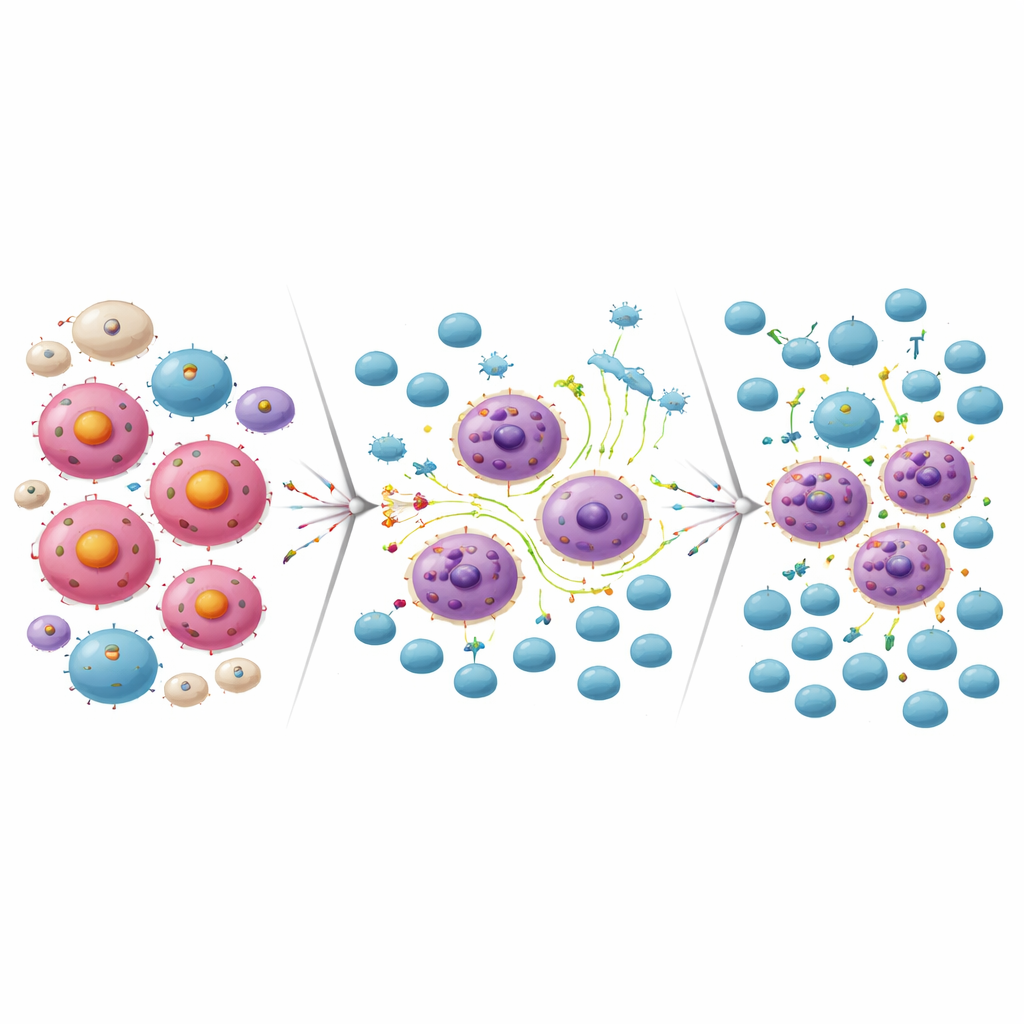
Transformer la résistance en une ouverture pour les CAR-T
La même reprogrammation inflammatoire qui a aidé certaines cellules lymphomateuses à survivre au blocage de MCL-1 les a aussi rendues plus vulnérables à l’attaque immunitaire. En laboratoire, des CAR-T ciblant CD19 ont efficacement tué des cellules lymphomateuses devenues résistantes au médicament anti–MCL-1. À l’inverse, des cellules lymphomateuses rendues résistantes à la thérapie CAR-T anti‑CD19 étaient très sensibles à l’inhibiteur de MCL-1. Lorsque les chercheurs ont combiné une dose sous-létale de l’inhibiteur de MCL-1 avec des CAR-T en culture cellulaire, les deux traitements ensemble ont éliminé beaucoup plus de cellules lymphomateuses que chacun séparément. Dans des modèles murins, administrer l’inhibiteur de MCL-1 suivi de CAR-T anti‑CD19 a conduit à une clairance tumorale quasi complète et à une survie nettement prolongée par rapport aux traitements individuels.
Un coup de poing en un-deux avec potentiel curatif
En résumé, l’étude suggère une stratégie « un‑deux ». D’abord, un médicament bloquant MCL-1 réduit la majorité du lymphome et force les cellules cancéreuses survivantes dans un état inflammé et hautement visible qui attire les lymphocytes T et dépouille les défenses immunitaires protectrices. Ensuite, les CAR-T anti‑CD19 exploitent cette faiblesse nouvellement exposée pour éradiquer la maladie résiduelle. En frappant à la fois le câblage interne de survie de la tumeur et son voisinage protecteur, cette approche combinée pourrait réduire les rechutes et rapprocher les lymphomes B agressifs d’une rémission durable.
Citation: Gao, J., Zhao, X., Yin, Q. et al. Synthetic lethality of MCL-1 inhibition and CAR-T therapy in aggressive B-cell lymphoma. Leukemia 40, 638–648 (2026). https://doi.org/10.1038/s41375-026-02884-8
Mots-clés: Lymphome B, Thérapie CAR-T, Inhibition de MCL-1, Microenvironnement tumoral, Résistance aux médicaments