Clear Sky Science · fr
JAK2V617F reprogramme HIF‑1 pour induire un régulon hypoxique non canonique dans les néoplasies myéloprolifératives
Pourquoi c’est important pour les cancers du sang
Certaines hémopathies à évolution lente, dites néoplasies myéloprolifératives, peuvent couver discrètement pendant des années avant de basculer soudainement en leucémie agressive. Cette étude pose une question simple mais cruciale : comment une mutation oncogénique fréquente détourne‑t‑elle le système cellulaire de détection de l’oxygène, et peut‑on cibler ce détournement spécifiquement sans nuire aux cellules saines ? Les réponses pourraient ouvrir une nouvelle voie pour traiter les patients à haut risque tout en préservant les tissus normaux qui dépendent aussi des signaux de détection de l’oxygène.
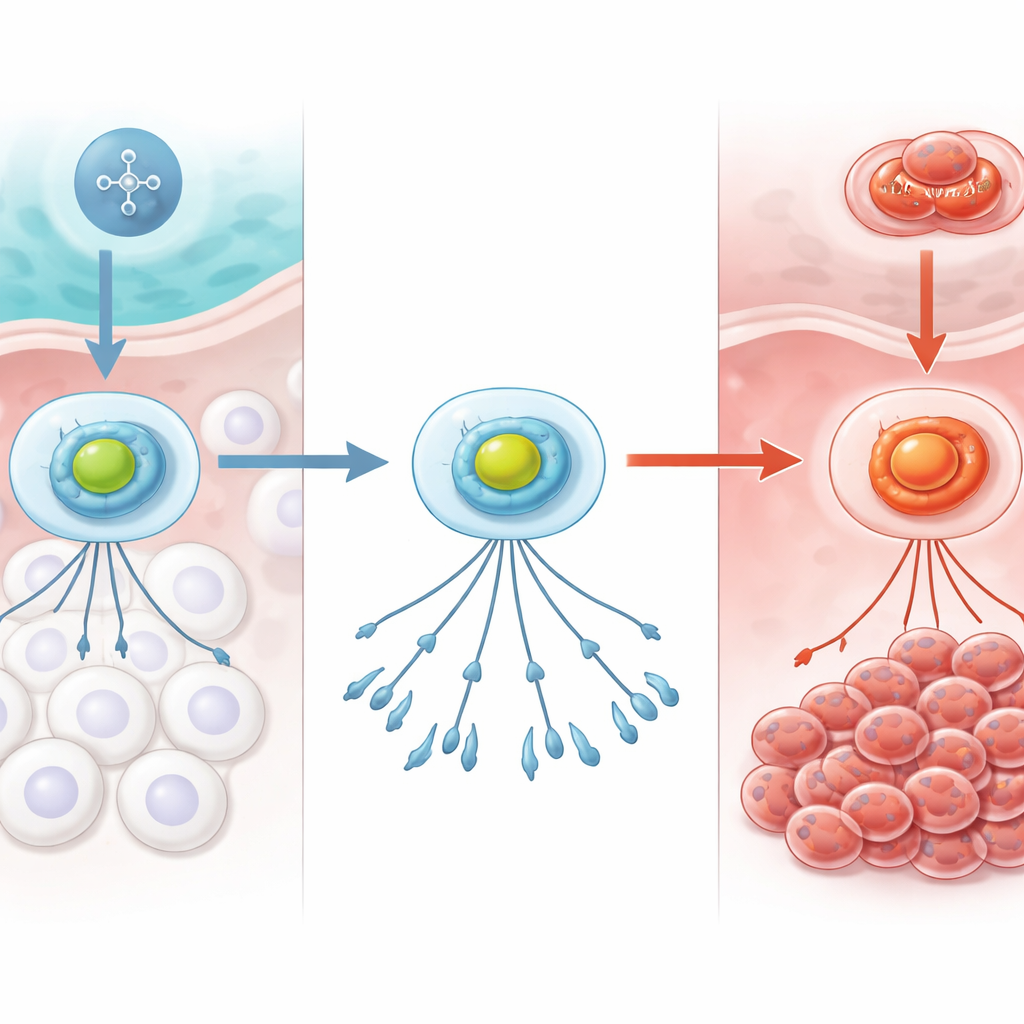
Le système d’alarme oxygène de l’organisme
Les cellules surveillent en permanence la quantité d’oxygène disponible. Au cœur de ce système se trouve un complexe protéique appelé HIF‑1, qui fonctionne comme une alarme de présence d’oxygène. Dans des conditions normales et bien oxygénées, une sous‑unité de HIF‑1 est rapidement dégradée, maintenant l’alarme hors service. Quand l’oxygène diminue, cette dégradation s’arrête, HIF‑1 se stabilise, se fixe sur l’ADN de la cellule et active des gènes qui aident à l’adaptation, par exemple en modifiant l’usage de l’énergie ou en favorisant la formation de nouveaux vaisseaux. Dans le cancer, ce même système peut être détourné au profit de la tumeur, aidant les cellules malignes à résister à des environnements stressants comme la moelle osseuse pauvre en oxygène.
Quand une mutation recâble l’alarme
Les chercheurs se sont intéressés à une mutation appelée JAK2V617F, très fréquente dans les néoplasies myéloprolifératives. Des travaux antérieurs montraient que cette mutation maintient l’alarme HIF‑1 activée même lorsque l’oxygène est abondant. À l’aide de lignées cellulaires modifiées, l’équipe a comparé la liaison de HIF‑1 à l’ADN dans deux conditions : une vraie hypoxie, et des conditions normales d’oxygène en présence de la mutation JAK2V617F. Ils ont constaté que dans les cellules mutées HIF‑1 se lie à moins de régions du génome, est moins réactif aux variations d’oxygène, et interagit avec un ensemble différent de protéines partenaires, beaucoup étant impliquées dans le traitement de l’ARN. Autrement dit, la mutation ne se contente pas de laisser HIF‑1 « activé » en permanence — elle réaccorde l’alarme sur un ensemble différent de cibles.
Un programme génique spécifique au cancer
À partir de ces expériences, les auteurs ont défini plusieurs ensembles de gènes dépendants de HIF‑1, dont un qu’ils appellent la signature hypoxique JAK2V617F. Ils ont ensuite évalué l’intensité de ces signatures dans des cellules sanguines de 172 patients porteurs de JAK2V617F. De manière surprenante, les programmes géniques HIF‑1 habituels liés à la faible oxygénation ne prévoyaient ni la sévérité de la maladie ni la survie des patients. En revanche, la signature hypoxique spécifique à la mutation séparait clairement les patients ayant une maladie plus grave et était associée à une survie globale plus médiocre. Beaucoup de gènes de cet ensemble étaient particulièrement actifs dans les progéniteurs mégacaryocytaires, les cellules médullaires qui prolifèrent et conduisent à la fibrose dans ces maladies, et certains participaient à la réparation de l’ADN — un processus qui peut aider les cellules cancéreuses à survivre à des stress nuisibles.
Indices sur l’aggravation soudaine de la maladie
Une inquiétude majeure pour les patients est la transformation soudaine d’une maladie chronique en une leucémie agressive dite « phase blastique ». En analysant des échantillons appariés de patients avant et après ce changement, l’équipe a distillé un sous‑ensemble plus petit de 13 gènes, baptisé signature HIF1‑MPN‑BP, dont l’expression augmentait ou diminuait avec la transformation. Ce sous‑ensemble était fortement associé à des scores de risque plus élevés, à une survie plus courte et à une fibrose médullaire plus sévère. Fait important, ce profil semblait spécifique à la maladie entraînée par JAK2V617F, et non une caractéristique générique de toutes les leucémies. Beaucoup de gènes de ce groupe sont des cibles médicamenteuses plausibles, suggérant une liste ciblée de candidats pour des thérapies futures visant à bloquer la progression.
Trouver l’auxiliaire caché de la mutation
Comment JAK2V617F maintient‑il HIF‑1 actif indépendamment de l’oxygène ? Grâce à des approches de biochimie des protéines, les auteurs ont découvert que dans les cellules mutées HIF‑1 porte deux marques chimiques jusque‑là inconnues (phosphorylations) dans une région qui contrôle normalement sa dégradation. Ils ont attribué ces modifications à PIM1, une kinase activée en aval de la mutation JAK2. Bloquer PIM1 avec des composés expérimentaux faisait chuter les niveaux de HIF‑1 dans les cellules mutées, tout en laissant en grande partie intacte la réponse normale à la faible oxygénation. L’inhibition de PIM1 réduisait également de façon sélective l’expression des gènes à risque HIF1‑MPN‑BP et poussait les cellules mutées vers la mort cellulaire, tout en épargnant leurs homologues non mutées.
Ce que cela signifie pour les patients
Ce travail montre que la même protéine détectrice d’oxygène, HIF‑1, se comporte très différemment selon le mode d’activation. Dans les néoplasies myéloprolifératives pilotées par JAK2V617F, un axe de signalisation JAK2–PIM1 stabilise HIF‑1 d’une manière qui le détache du contrôle normal par l’oxygène et concentre son activité sur un ensemble de gènes favorisant la maladie. Parce que ce programme altéré est étroitement lié à la gravité de la maladie et au risque de transformation, et peut être atténué par le blocage de PIM1, il offre une voie prometteuse pour cibler l’activité maligne de HIF‑1 tout en préservant son rôle essentiel dans les tissus sains. Des thérapies exploitant cette différence pourraient un jour aider à empêcher que des cancers du sang à évolution lente ne basculent en une leucémie menaçant le pronostic vital.
Citation: Kealy, D., Ellerington, R., Bansal, S. et al. JAK2V617F reprograms Hypoxia Inducible Factor-1 to induce a non-canonical hypoxia regulon in myeloproliferative neoplasms. Leukemia 40, 609–621 (2026). https://doi.org/10.1038/s41375-025-02843-9
Mots-clés: néoplasies myéloprolifératives, JAK2V617F, HIF-1, kinase PIM1, transformation en phase blastique