Clear Sky Science · fr
Alnuctamab, un engageur de cellules T bivalent ciblant l’antigène de maturation des cellules B pour les patients atteints de myélome multiple en rechute ou réfractaire : résultats d’une phase 1, première étude chez l’humain
Pourquoi ce nouveau médicament contre le cancer compte
Pour les personnes vivant avec un myélome multiple, un cancer du sang qui récidive presque toujours après le traitement, chaque nouvelle option peut signifier plus de temps et une meilleure qualité de vie. Cette étude évalue une immunothérapie de nouvelle génération appelée alnuctamab, conçue pour aider les cellules de défense de l’organisme à repérer et éliminer les cellules myélomateuses. La recherche pose une question pratique importante pour les patients et les médecins : ce traitement puissant peut‑il être administré par une simple injection sous‑cutanée, tout en conservant de forts effets anti‑tumoraux mais avec moins d’effets indésirables graves ?
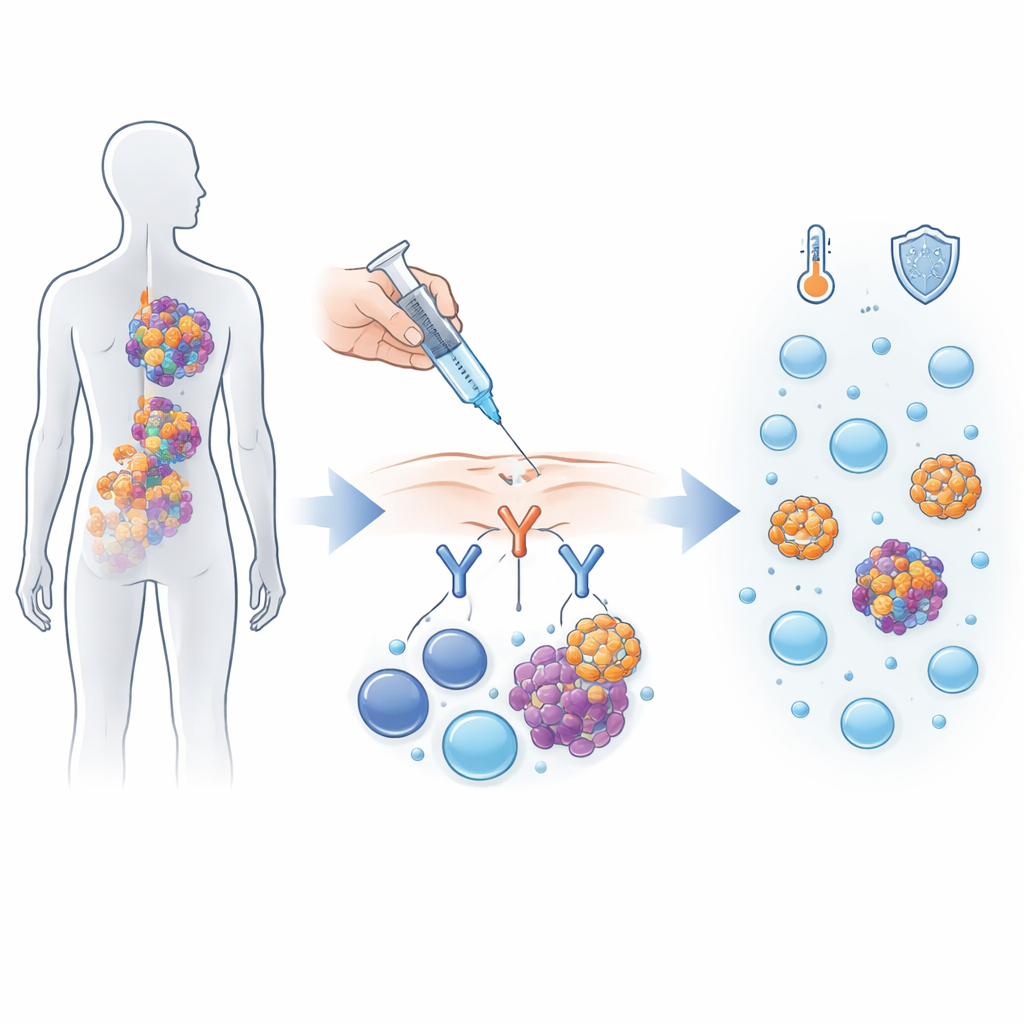
Une manière astucieuse de rediriger le système immunitaire
Alnuctamab appartient à une nouvelle classe de médicaments qui font office d’intermédiaires moléculaires entre les cellules cancéreuses et les cellules immunitaires. Les cellules du myélome présentent un marqueur appelé BCMA à leur surface, tandis que les cellules T portent un autre marqueur, le CD3. Alnuctamab est construit avec deux « bras » qui se fixent sur BCMA et un bras qui se fixe sur CD3, rapprochant ainsi les cellules T des cellules myélomateuses pour qu’elles les attaquent. Dans cet essai de première administration chez l’humain, 165 personnes atteintes d’un myélome revenu après au moins trois types de traitement ont reçu alnuctamab, soit par perfusion intraveineuse, soit par injection sous‑cutanée.
De la perfusion à l’injection
Au départ, le médicament était administré par voie intraveineuse, mais cette approche a entraîné des réactions immunitaires plus intenses, y compris un épisode potentiellement mortel d’un syndrome de libération de cytokines, où le système immunitaire libère soudainement de grandes quantités de signaux inflammatoires. En raison de ces problèmes de sécurité et de bénéfices seulement modestes, l’étude est passée à l’administration sous‑cutanée, qui libère le médicament plus progressivement. Quatre‑vingt‑quinze patients ont été traités de cette façon selon un schéma « d’escalade progressive » : de petites doses initiales suivies de doses cibles plus élevées, la fréquence des injections diminuant lentement au fil du temps, de hebdomadaire à une fois toutes les quatre semaines si le traitement se poursuivait.
Comment les patients ont réagi et ce à quoi ils ont été confrontés
Parmi tous les patients ayant reçu les injections sous‑cutanées, environ 59 % ont vu leur cancer diminuer d’au moins moitié, et près de la moitié sont devenus « négatifs en maladie résiduelle minimale », ce qui signifie que des tests très sensibles n’ont plus pu détecter de cellules myélomateuses dans leur moelle osseuse. À la dose recommandée de 30 milligrammes, les réponses étaient encore plus marquées : environ 71 % ont répondu et plus de la moitié ont atteint la négativité en maladie résiduelle minimale. De nombreux patients ont maintenu le contrôle de leur maladie près d’un an ou plus, même lorsque le calendrier de dosage devenait moins intense. Les effets secondaires étaient fréquents mais le plus souvent gérables. Des réactions immunitaires de type fièvre sont survenues chez environ trois patients sur cinq, mais toutes étaient bénignes ou modérées. Des baisses des globules blancs et des infections sont apparues, reflétant à la fois la puissance du médicament et la fragilité du système immunitaire des patients ; toutefois, les infections graves étaient moins fréquentes que celles rapportées avec plusieurs médicaments similaires.
Pourquoi la voie sous‑cutanée était plus sûre
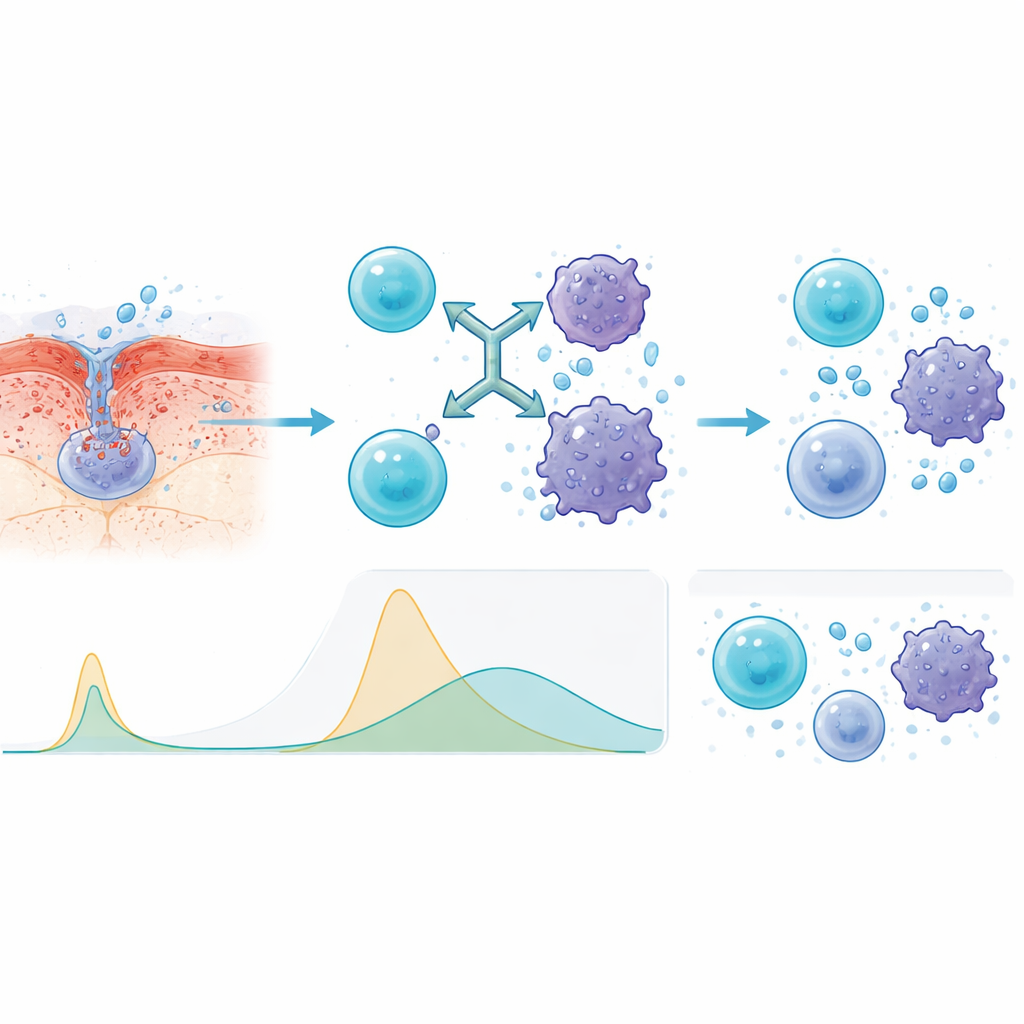
Pour comprendre pourquoi la méthode sous‑cutanée se comportait mieux, les chercheurs ont mesuré les molécules de signalisation immunitaire dans le sang. Par rapport à la perfusion intraveineuse, les injections ont produit des pics plus lents et plus faibles de signaux inflammatoires clés tels que certaines interleukines et le facteur de nécrose tumorale. Ce profil plus aplati signifie que le système immunitaire est toujours activé contre le cancer, mais sans la même poussée brutale qui peut rendre les patients gravement malades. L’équipe a également constaté que les personnes dont le sang montrait des taux plus faibles de BCMA libéré au départ — signe d’une maladie moins agressive ou moins avancée — avaient tendance à mieux répondre et à rester en rémission plus longtemps.
Ce que cela signifie pour les soins futurs du myélome
Bien que la société ait depuis décidé de ne pas poursuivre le développement d’alnuctamab pour des raisons stratégiques, les enseignements de cet essai sont importants. L’étude montre qu’un engageur immunitaire soigneusement conçu peut être administré par une simple injection, selon un calendrier devenant moins contraignant au fil du temps, tout en produisant des réponses profondes et durables chez de nombreuses personnes atteintes d’un myélome difficile à traiter. Elle suggère aussi que l’augmentation progressive de la dose et l’évitement de pics brusques d’activation immunitaire peuvent limiter les réactions graves sans diminuer l’efficacité anti‑tumorale. Ces enseignements devraient guider la conception de futurs traitements immunitaires, offrant l’espoir que davantage de patients en rechute de myélome disposeront de thérapies efficaces, à la fois puissantes, plus sûres et plus faciles à vivre au quotidien.
Citation: Bar, N., Martin, T., Hofmeister, C.C. et al. Alnuctamab, a bivalent B-cell maturation antigen-targeting T cell engager for patients with relapsed or refractory multiple myeloma: results from a phase 1, first-in-human study. Leukemia 40, 481–490 (2026). https://doi.org/10.1038/s41375-025-02841-x
Mots-clés: myélome multiple, immunothérapie, anticorps bispécifique, BCMA, engageur de cellules T