Clear Sky Science · fr
Un agoniste Notch soluble permet la maturation des améloblastes humains et la formation d’un tissu semblable à l’émail pour la régénération dentaire
Pourquoi réparer l’émail dentaire est si difficile
L’émail, la coque blanche et vitreuse qui recouvre nos dents, est le matériau le plus dur du corps humain — mais une fois perdu, il ne repousse pas. Plus de 90 % des adultes présentent une perte ou une détérioration de l’émail, et pourtant nos dents n’ont aucun mécanisme naturel pour reconstruire cette armure protectrice. Cette étude décrit une méthode pour cultiver en laboratoire des cellules humaines productrices d’émail, les pousser jusqu’à un état de maturité complet, et même les inciter à former un minéral semblable à l’émail chez l’animal. Ce travail ouvre une voie vers de futures thérapies qui pourraient un jour réparer les dents avec du tissu vivant plutôt qu’avec des plombages ou des couronnes.
Construire l’émail dentaire à partir de cellules souches
L’émail est fabriqué par des cellules spécialisées appelées améloblastes, qui disparaissent une fois la dent sortie des gencives. Sans elles, les dents adultes ne peuvent pas fabriquer de nouvel émail. Les chercheurs utilisent des cellules souches pluripotentes induites humaines — des cellules adultes reprogrammées dans un état flexible proche de l’embryon — pour créer des « améloblastes induits ». Dans des travaux antérieurs, ces cellules cultivées en laboratoire pouvaient commencer à ressembler à de véritables cellules productrices d’émail mais s’arrêtaient avant d’atteindre la pleine maturité, et ne fonctionnaient correctement que lorsqu’elles étaient cultivées en contact étroit avec des odontoblastes, les cellules formant la dentine sous-jacente. Cela posait une question clé : qu’apportent exactement les odontoblastes aux améloblastes pour leur permettre d’achever leur développement ?
La conversation manquante entre cellules dentaires
Pour décoder ce dialogue cellulaire, l’équipe a exploité des cartes d’expression génique cellule par cellule de dents humaines et de souris en développement. Ils ont recherché les voies de signalisation s’exprimant spécifiquement des odontoblastes vers les améloblastes pendant la fenêtre critique de formation de l’émail. Une voie s’est imposée : Notch, un système de communication directe cellule‑à‑cellule largement utilisé durant le développement embryonnaire. Dans ces cartes dentaires, les ligands de type Delta (en particulier DLL1 et DLL4) se trouvaient principalement sur les odontoblastes, tandis que les récepteurs Notch étaient concentrés sur les améloblastes en maturation. Lorsque les chercheurs ont bloqué l’activité de Notch avec un médicament dans leur système de co‑culture, les améloblastes ont fortement réduit la production d’enameline, une protéine majeure de l’émail — preuve solide que la signalisation Notch est essentielle pour que les cellules productrices d’émail atteignent leur maturité. 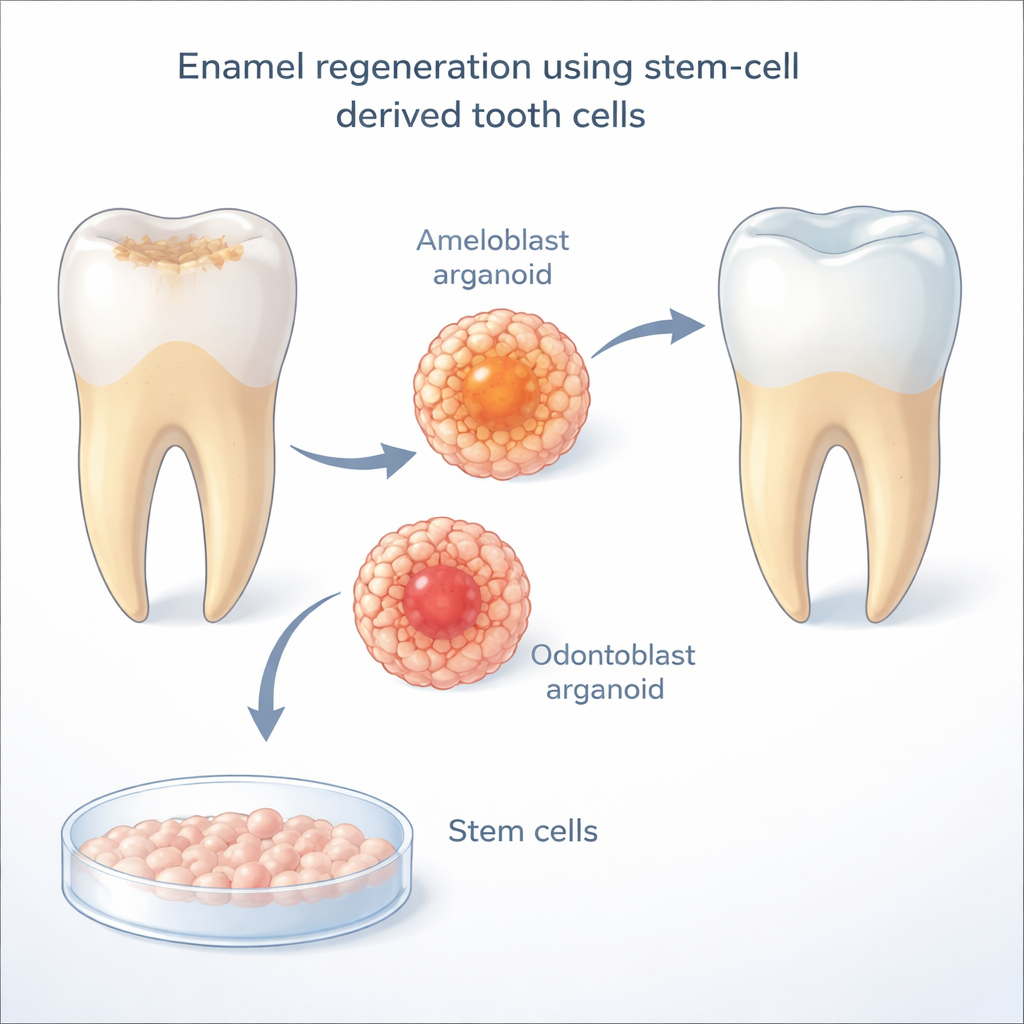
Un commutateur protéique conçu par IA pour les cellules de l’émail
Pour aller plus loin, l’équipe a voulu activer Notch de manière précise et contrôlable, sans dépendre d’odontoblastes réels. Ils ont utilisé une protéine artificielle appelée C3‑DLL4, conçue à l’aide d’outils computationnels. Cette molécule soluble arrange trois copies du domaine de signalisation DLL4 sur un échafaudage rigide à trois branches, lui permettant d’agréger et d’activer les récepteurs Notch des cellules voisines comme le ferait une cellule voisine naturelle. Dans des lignées rapportrices, C3‑DLL4 a fortement activé les gènes dépendants de Notch. Lorsqu’on l’a ajouté à des organoïdes d’améloblastes précoces — de petits amas cellulaires 3D issus de cellules souches — il a provoqué un basculement massif du profil d’expression génique. Les organoïdes sont passés d’un profil immature à un profil correspondant à des améloblastes sécrétoires et pleinement matures, en activant des gènes emblématiques tels que AMELX, ENAM, MMP20, ODAM, KLK4, TUFT1 et WDR72. L’inhibition de l’activité Notch avait l’effet inverse, bloquant la maturation et perturbant la production des protéines de l’émail.
Des organoïdes à un tissu ressemblant à l’émail
Fait remarquable, lorsque ces organoïdes d’améloblastes activés par Notch ont été transplantés sous la capsule rénale de souris immunodéprimées — un niche sûre et bien vascularisée souvent utilisée pour tester des tissus humains — ils ont commencé à déposer un matériau dense et minéralisé. Des micro‑scans CT à haute résolution et des techniques classiques de coloration osseuse ont confirmé la présence de nodules calcifiés là où un tel tissu n’existe normalement pas. La microscopie a montré des couches organisées et polarisées de cellules humaines exprimant des protéines clés de l’émail et WDR72, un facteur lié à la minéralisation correcte de l’émail. Bien que ce matériau soit mieux décrit comme « semblable à l’émail » plutôt que comme de l’émail pleinement naturel, il démontre que des améloblastes humains ingénierés peuvent, en principe, déposer du minéral dur dans un organisme vivant. 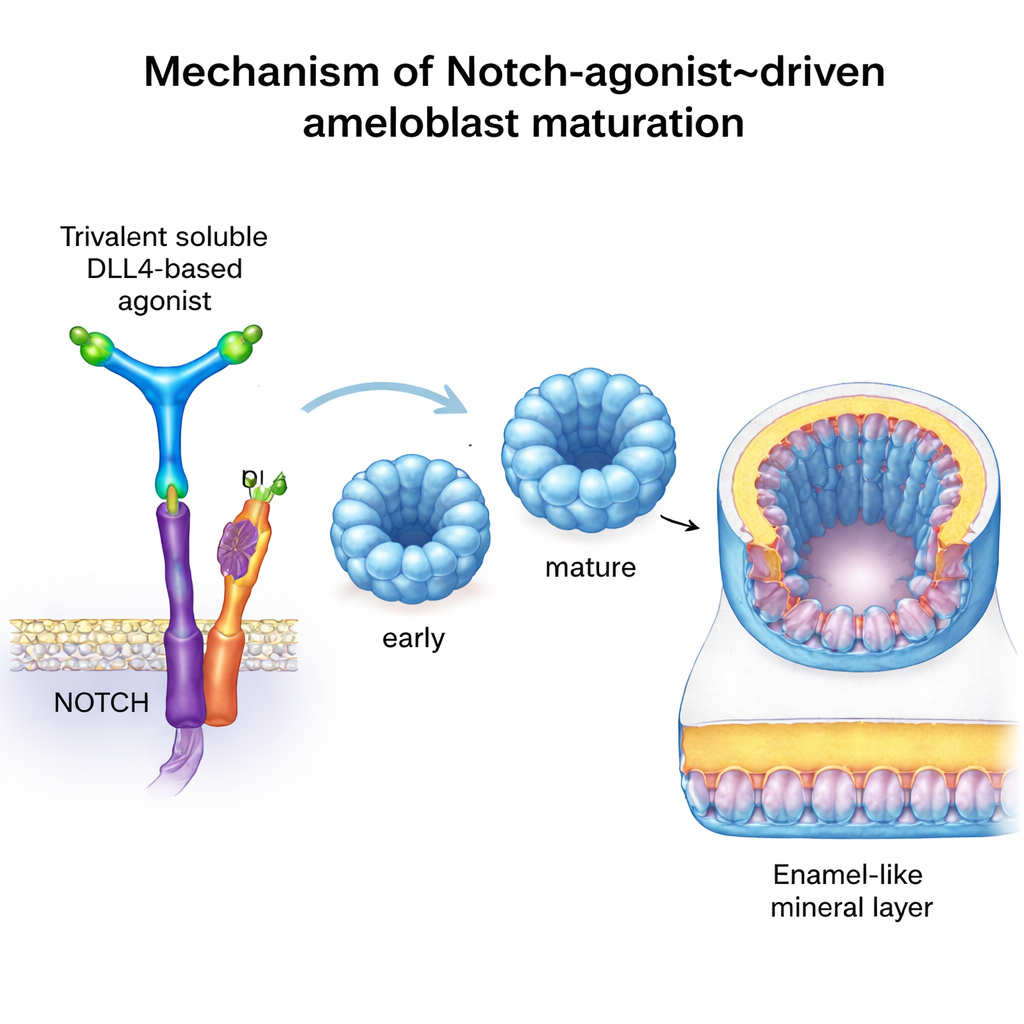
Élucider une énigme génétique derrière un émail fragile
L’étude aborde aussi une énigme de longue date autour du gène DLX3, dont les mutations provoquent certains défauts héréditaires de l’émail et augmentent le risque de caries. DLX3 est actif à la fois dans les améloblastes et les odontoblastes, ce qui rend difficile de savoir quel type cellulaire est principalement affecté en cas d’anomalie. En utilisant leur système d’organoïdes sans odontoblastes et l’édition génomique CRISPR, les chercheurs ont supprimé DLX3 spécifiquement dans la lignée des améloblastes. Les étapes précoces de formation des améloblastes se sont encore produites, mais la phase finale de maturation s’est effondrée : des protéines clé de l’émail telles que l’enameline, AMELX, MMP20, KLK4, TUFT1 et WDR72 ont été fortement réduites tant au niveau de l’ARN que des protéines. Cela montre que DLX3 est requis directement à l’intérieur des améloblastes humains pour achever le programme de fabrication de l’émail, contribuant à expliquer pourquoi des variantes près de ce gène sont liées à des dents fragiles et sujettes aux caries.
Ce que cela pourrait signifier pour les soins dentaires futurs
Ensemble, ces résultats dessinent une feuille de route pas à pas allant des cellules souches aux organoïdes producteurs d’émail jusqu’à un tissu semblable à l’émail in vivo, contrôlée par un « interrupteur » Notch modulable et par le gène DLX3. Si la régénération clinique des dents reste encore lointaine, ce travail fournit un terrain d’essai puissant pour comprendre les maladies dentaires génétiques, tester de nouveaux traitements et affiner des stratégies visant à reconstruire l’émail perdu avec des cellules vivantes plutôt qu’avec des matériaux inertes. Pour les patients, l’espoir à long terme est que les visites chez le dentiste puissent un jour consister à réparer des dents usées ou cariées avec un émail bioingénieré se comportant beaucoup plus comme l’émail naturel.
Citation: Patni, A.P., Mout, R., Alghadeer, A. et al. Soluble Notch agonist enables human ameloblast maturation and enamel-like tissue formation for tooth regeneration. Int J Oral Sci 18, 25 (2026). https://doi.org/10.1038/s41368-026-00429-4
Mots-clés: régénération de l'émail, organoïdes d'améloblastes, signalisation Notch, DLX3, cellules souches dentaires