Clear Sky Science · fr
ANKRD1 soutient une niche néurogène des CSMO et lutte contre le vieillissement cognitif
Pourquoi la mâchoire pourrait compter pour un esprit vieillissant
La plupart des gens pensent que l’os de la mâchoire sert surtout à la mastication et aux soins dentaires, pas à la mémoire. Cette étude suggère un lien surprenant : des cellules souches nichées dans la moelle osseuse de la mâchoire pourraient aider à protéger le cerveau de la perte de mémoire liée à l’âge. Les chercheurs se sont concentrés sur une protéine appelée ANKRD1, montrant qu’elle aide ces cellules souches d’origine mandibulaire à conserver leur potentiel « neuronal » et, par conséquent, soutient la santé cérébrale et la mémoire spatiale chez des animaux âgés.
Une niche dissimulée favorable aux nerfs dans l’os de la mâchoire
La moelle osseuse de la mâchoire contient des cellules stromales mésenchymateuses — des cellules souches polyvalentes surtout connues pour produire os et cartilage. Comme la mâchoire se développe à partir d’une structure appelée la crête neurale, les auteurs ont émis l’hypothèse que ses cellules souches pourraient conserver une certaine aptitude à former des cellules nerveuses. À l’aide du séquençage d’ARN unicellulaire, ils ont cartographié des milliers de cellules souches mandibulaires individuelles et découvert une sous-population distincte ressemblant à des progéniteurs neuronaux : très proliférative, riche en gènes liés au développement neuronal et prête à devenir des cellules de type nerveux. Dans cette niche, ANKRD1 est apparue comme un marqueur remarquable, fortement associée tant à la croissance qu’au potentiel neurogénique.
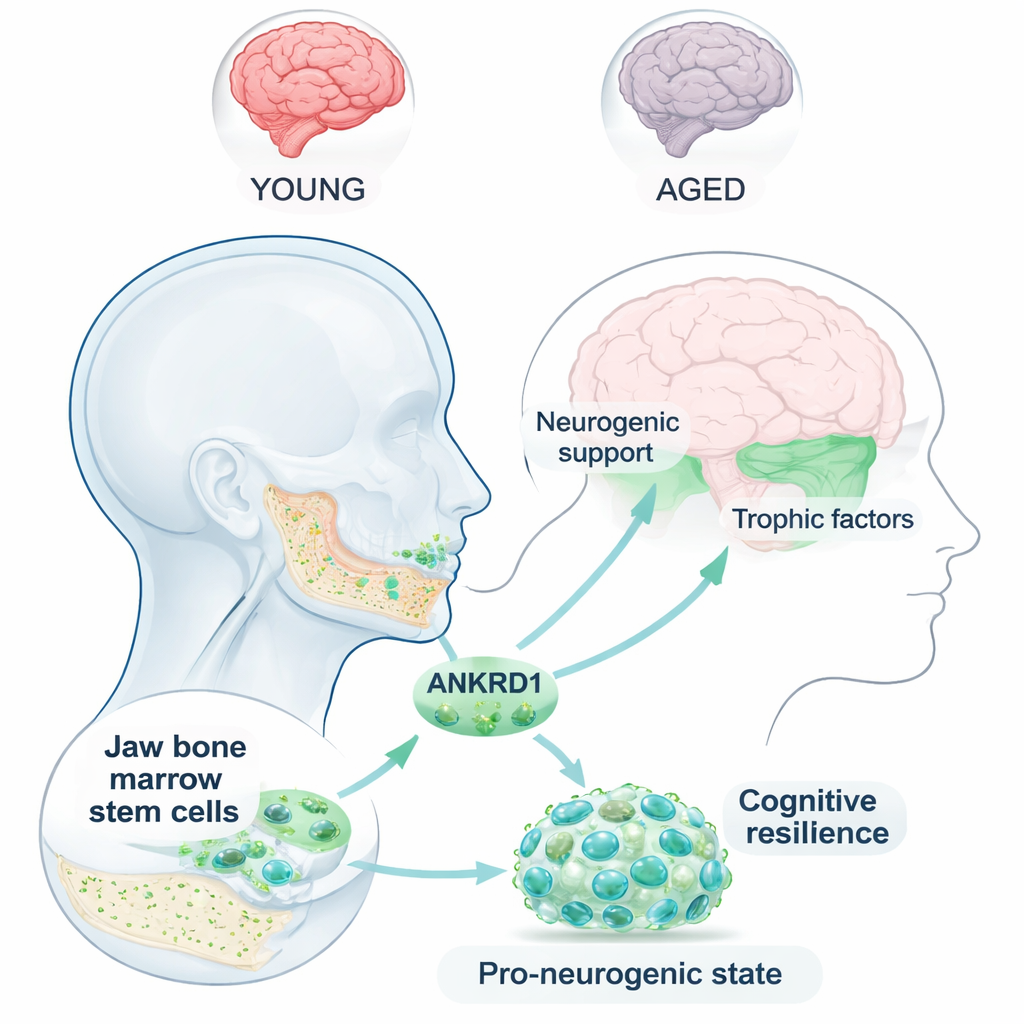
ANKRD1, gardien contre le vieillissement et la spécialisation prématurée
Avec l’âge, de nombreuses cellules souches perdent leur plasticité et s’épuisent. L’équipe a montré que les niveaux d’ANKRD1 chutent brutalement dans les cellules souches mandibulaires de donneurs âgés et dans des cellules cultivées en laboratoire soumises à un état sénescent. Quand ANKRD1 était réduit expérimentalement dans des cellules jeunes, des marqueurs classiques du vieillissement augmentaient et les cellules se comportaient comme vieilles. À l’inverse, augmenter ANKRD1 dans des cellules âgées atténuait ces signaux de sénescence. La protéine empêchait aussi les cellules de se spécialiser trop vite en lignées osseuses ou adipeuses : un faible ANKRD1 augmentait les marqueurs osseux et adipeux, tandis qu’un ANKRD1 élevé les réprimait. En termes simples, ANKRD1 aide les cellules souches mandibulaires à rester jeunes et polyvalentes au lieu de s’épuiser ou de se verrouiller dans un seul destin.
Maintenir les gènes neuronaux accessibles au niveau de l’ADN
Les auteurs se sont alors demandé comment ANKRD1 exerce un contrôle aussi large. En cartographiant les sites de liaison d’ANKRD1 sur le génome, ils ont trouvé qu’elle se fixe fortement sur des régions régulatrices puissantes appelées super-amplificateurs (super-enhancers), en particulier celles contrôlant deux gènes clés des cellules souches neuronales, SOX2 et NESTIN. Dans les cellules jeunes et indifférenciées, la présence d’ANKRD1 à ces sites coïncidait avec une chromatine ouverte et accessible — une architecture de l’ADN relâchée qui permet l’activation des gènes. Au fur et à mesure que les cellules se différaient ou vieillaient, la liaison d’ANKRD1 aux régions de contrôle distantes diminuait, la chromatine devenait plus compacte et les voies neuronales s’activaient moins. Des tests rapporteurs ont confirmé qu’ANKRD1 peut directement augmenter l’activité des éléments régulateurs de SOX2 et NESTIN. Combinés à une cartographie 3D du génome, ces résultats suggèrent qu’ANKRD1 maintient un « réservoir neurogénique » dans les cellules souches de la mâchoire en conservant des gènes neuronaux clés dans une configuration ouverte et prête à l’emploi.
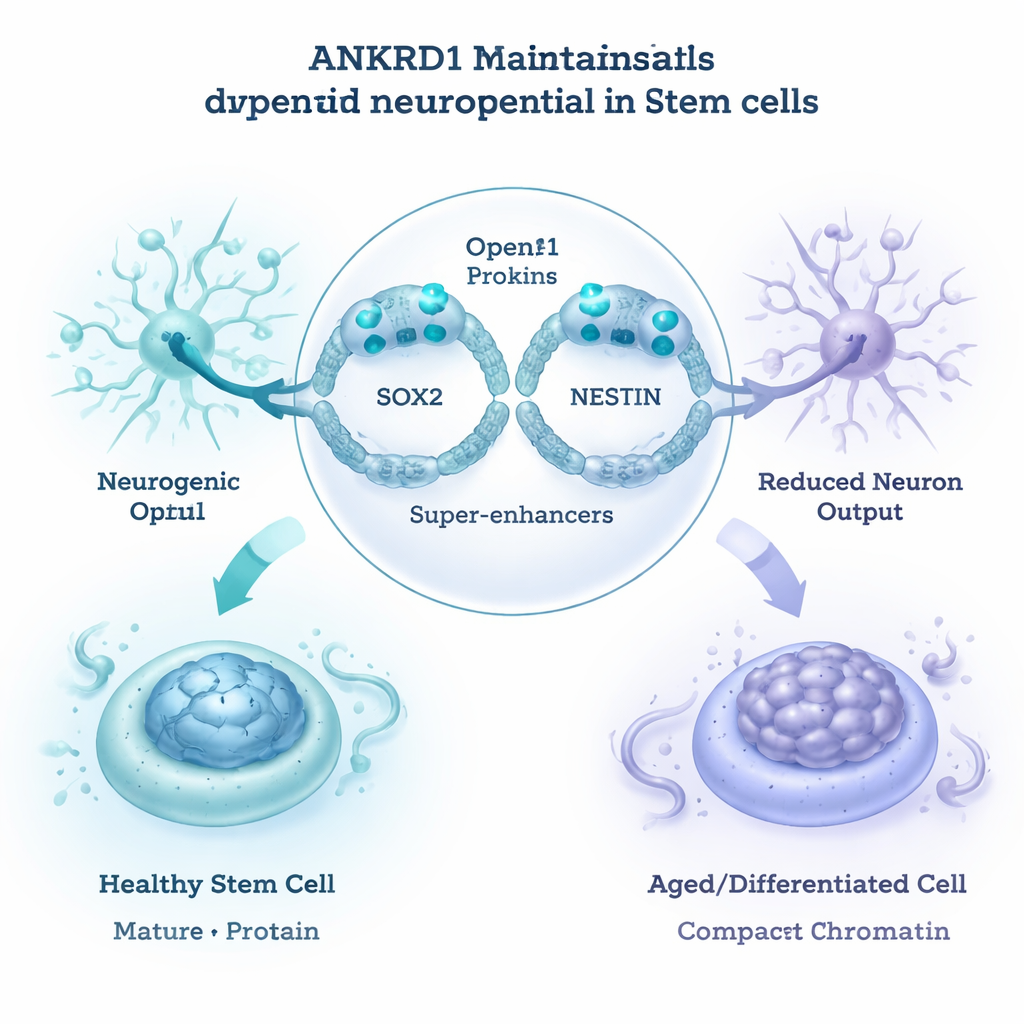
Des cellules souches mandibulaires à une meilleure mémoire chez les souris âgées
Si ANKRD1 garde ouvertes les options neuronales des cellules souches, peut‑il réellement améliorer la fonction cérébrale ? Pour le vérifier, les chercheurs ont délivré ANKRD1 spécifiquement aux neurones de souris naturellement âgées à l’aide d’un vecteur viral conçu pour traverser la barrière hémato‑encéphalique. Le traitement n’a pas modifié la locomotion ni le comportement anxieux, mais il a significativement amélioré les performances dans le labyrinthe aquatique de Morris, un test classique d’apprentissage et de mémoire spatiale. Les souris traitées ont appris plus rapidement la localisation de la plateforme et ont cherché de façon plus précise dans le quadrant correct. Dans des expériences cellulaires parallèles, augmenter les niveaux d’ANKRD1 a rendu les cellules souches mandibulaires plus expressives de marqueurs neuronaux, leur a donné des morphologies proches des neurones et a augmenté la sécrétion de facteurs trophiques soutenant le cerveau tels que NGF et BDNF, suggérant un bénéfice double : une meilleure capacité neurogénique intrinsèque et un environnement de soutien enrichi.
Reconfigurer les motifs d’activité cérébrale dans des régions clés de la mémoire
Pour comprendre comment ANKRD1 remodelait la fonction cérébrale, l’équipe a cartographié l’activité neuronale dans tout le cerveau de la souris en utilisant la protéine c‑Fos, qui s’active dans les cellules récemment actives. Les souris traitées par ANKRD1 ont montré une activation plus forte dans des régions cruciales pour la cognition, y compris la formation hippocampique, l’hypothalamus et le cortex extérieur. Ces zones sont non seulement devenues plus actives mais aussi plus synchronisées entre elles, passant de motifs fragmentés à des réseaux plus intégrés et corrélés positivement. Ce schéma d’activation coordonnée est considéré comme favorable à un traitement efficace de l’information et pourrait sous-tendre l’amélioration de la mémoire observée dans les tests comportementaux.
Ce que cela signifie pour la santé cérébrale future
Dans l’ensemble, l’étude présente ANKRD1 comme un interrupteur moléculaire clé qui préserve la capacité de former des neurones dans la moelle osseuse mandibulaire et aide à stabiliser les réseaux cérébraux pendant le vieillissement. En maintenant l’accessibilité de gènes neuronaux cruciaux et en favorisant à la fois la production de neurones et la libération de facteurs protecteurs, ANKRD1 soutient la résilience des circuits de la mémoire. Si la traduction chez l’humain nécessitera de la prudence, ce travail ouvre la porte à des thérapies tirant parti des origines développementales uniques des cellules souches mandibulaires et de leur « mémoire » chromatinienne pour combattre le vieillissement cognitif.
Citation: Wang, Z., Liu, X., Zhen, W. et al. ANKRD1 sustains a neurogenic BMSC niche and counters cognitive aging. Int J Oral Sci 18, 23 (2026). https://doi.org/10.1038/s41368-026-00428-5
Mots-clés: vieillissement cognitif, cellules souches de la moelle osseuse de la mâchoire, ANKRD1, neurogénèse, mémoire spatiale