Clear Sky Science · fr
Atlas transcriptionnel unicellulaire révèle des mécanismes distincts de crosstalk immuno‑chondrocytaire dans l’arthrose de l’articulation temporo‑mandibulaire induite par différents types de trouble occlusal
Pourquoi votre articulation de la mâchoire compte
Les petites articulations situées devant les oreilles, appelées articulations temporo‑mandibulaires (ATM), vous permettent de parler, mâcher, bâiller et rire. Lorsqu’elles développent une arthrose, les gestes quotidiens peuvent devenir douloureux et difficiles. Cette étude utilise l’analyse génétique unicellulaire de pointe chez la souris pour examiner ces articulations cellule par cellule, révélant comment différents problèmes d’occlusion déclenchent divers types de dommages — et comment cela pourrait orienter des traitements plus précis.
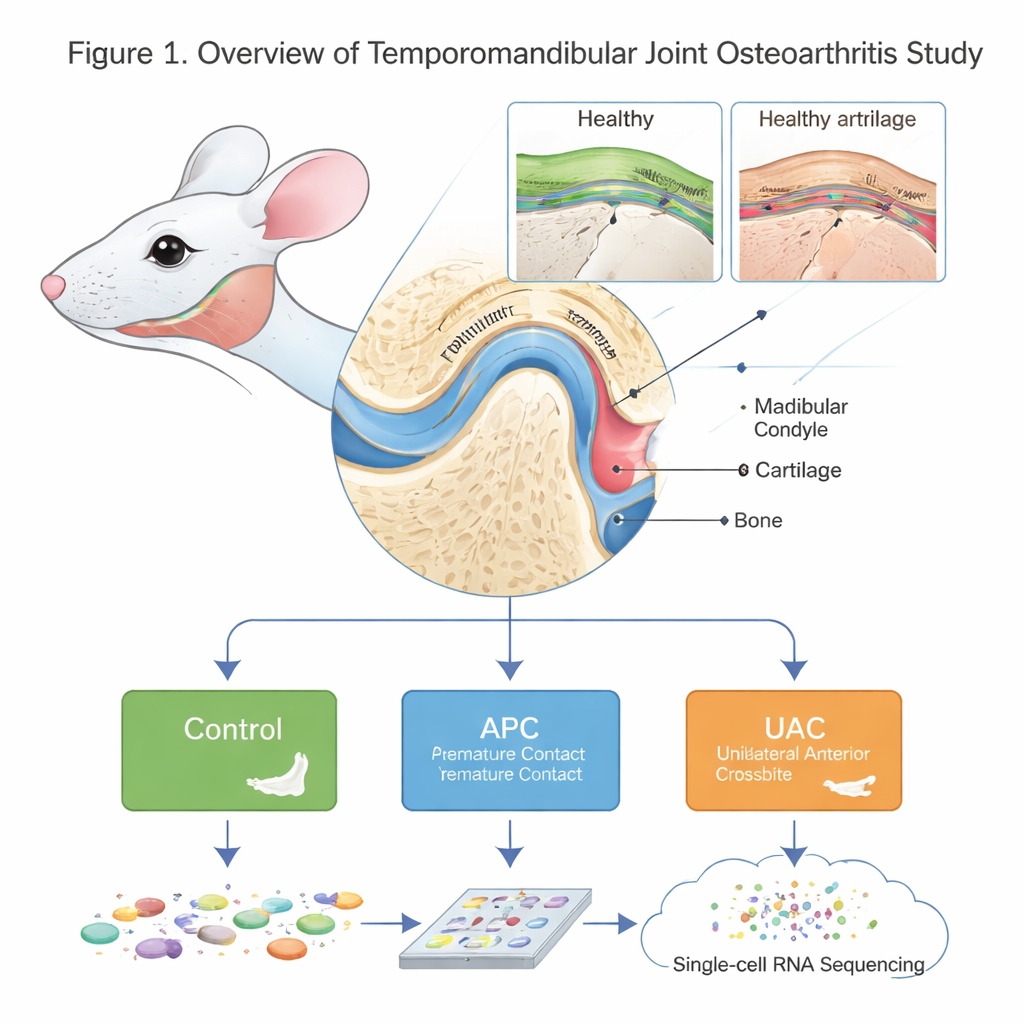
Observer de près une petite mais complexe articulation
L’ATM n’est pas une simple charnière. Son extrémité arrondie, le condyle mandibulaire, est recouverte d’un type particulier de cartilage et soutenue par l’os sous‑jacent. L’arthrose de cette articulation (ATMO) provoque douleur, raideur et perte de fonction, mais ses causes microscopiques et moléculaires ont été difficiles à démêler. Les auteurs ont créé un « atlas cellulaire » détaillé du condyle de la souris, en santé et en maladie, à l’aide du séquençage ARN unicellulaire, une technique qui lit quels gènes sont actifs dans des milliers de cellules individuelles. Ils ont comparé des souris saines avec deux modèles de déséquilibre occlusal — contact prématuré antérieur (APC), où les dents de devant se rencontrent trop tôt, et chévauchement antérieur unilatéral (UAC), où un côté des dents de devant s’occlut de façon anormale — deux situations connues pour surcharger l’articulation mandibulaire.
Plusieurs types de cellules cartilagineuses, pas une seule
Traditionnellement, le cartilage condylien a été décrit en larges couches — cellules proliférantes, matures et hypertrophiées. Cette étude montre que la réalité est bien plus variée. L’équipe a identifié plusieurs sous‑types de chondrocytes (cellules du cartilage), chacun avec son activité génique propre et son rôle probable. On trouve des cellules progénitrices proches de la surface qui fonctionnent comme un réservoir de réparation, des chondrocytes fibrosés impliqués dans une matrice cicatricielle et la réparation, des chondrocytes associés à l’inflammation produisant des signaux inflammatoires, des chondrocytes associés à la minéralisation et des chondrocytes hypertrophiés participant à la transformation du cartilage en os, ainsi que des cellules réparatrices qui atténuent le stress et l’inflammation. Dans les articulations saines, ces sous‑types s’organisent selon un schéma spatial ordonné et suivent une « trajectoire » de développement fluide du progéniteur vers des états plus matures.
Quand les problèmes d’occlusion brouillent l’ordre cellulaire de l’articulation
Les deux modèles APC et UAC ont entraîné un amincissement du cartilage, un râpelement de la surface et des lésions typiques de l’arthrose dans le condyle. Au niveau cellulaire, la proportion de chondrocytes diminuait tandis que les cellules immunitaires augmentaient. Dans le modèle APC, on a observé une poussée de certains chondrocytes minéralisants et hypertrophiés et une perturbation de la progression normale des progéniteurs vers les cellules matures. Dans l’UAC, on notait également une augmentation des chondrocytes fibrosés et réparateurs, suggérant une tentative de réparation et de remodelage plus marquée. La microcopie a confirmé que les cellules perdaient leurs couches ordonnées et devenaient compactes et désorganisées dans le cartilage malade, concordant avec les trajectoires de développement perturbées déduites des données d’expression génique.
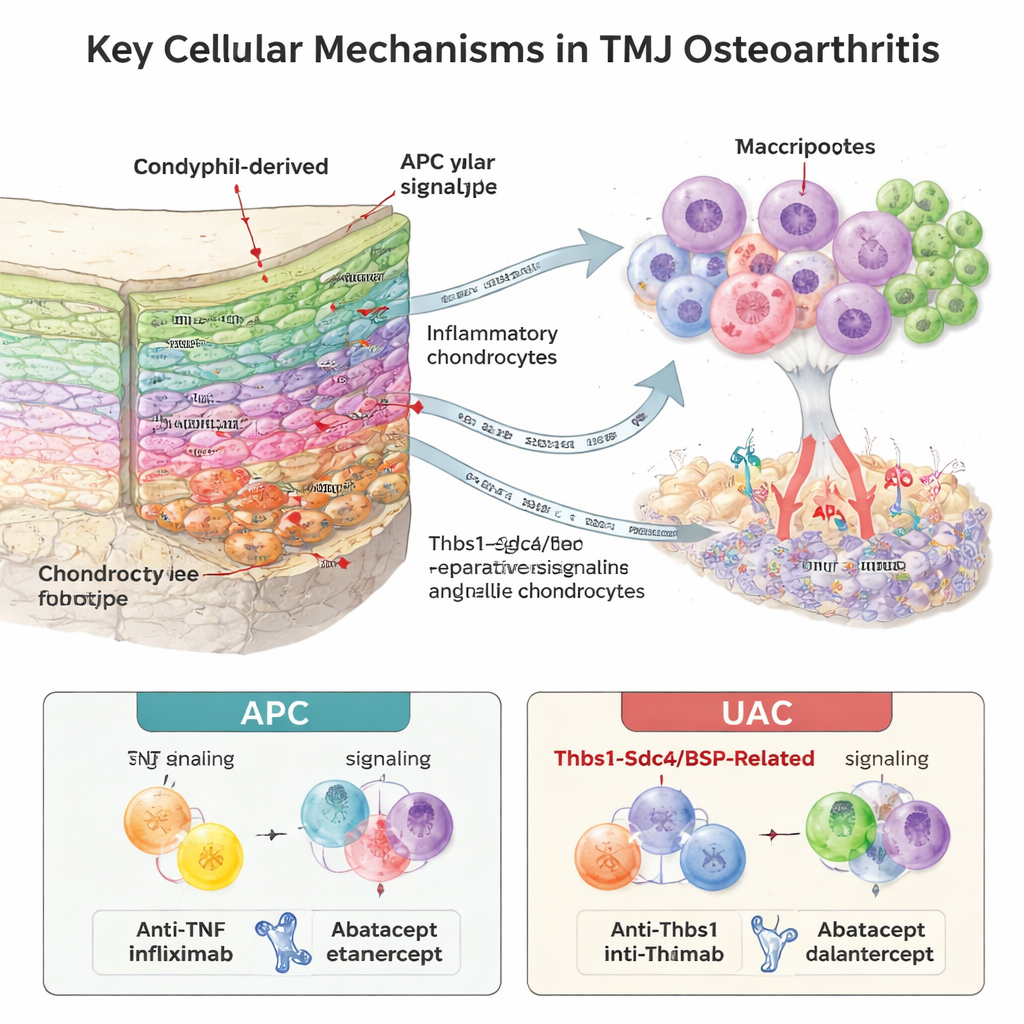
Les cellules immunitaires, les vaisseaux sanguins et le cartilage communiquent
L’os de soutien et la moelle du condyle abritaient un microenvironnement immunitaire étonnamment riche. Les chercheurs ont identifié neuf types de cellules immunitaires, avec une expansion marquée des neutrophiles (un globule blanc réactif) dans les articulations malades, en particulier à un stade de maturation spécifique. En analysant les molécules de signalisation et les récepteurs co‑exprimés, ils ont inféré un intense « crosstalk » entre cellules immunitaires et chondrocytes. Dans le modèle APC, les neutrophiles devenaient la principale source de TNF‑alpha, un signal inflammatoire puissant, envoyant des messages délétères aux cellules cartilagineuses. Dans le modèle UAC, un schéma différent est apparu : des signaux liés à l’os et au cartilage impliquant la sialoprotéine osseuse (BSP) et la voie Thbs1–Sdc4 étaient plus proéminents, étroitement liés à la néo‑vascularisation à la frontière cartilage‑os. Les zones riches en BSP coïncidaient avec des marqueurs d’angiogenèse, suggérant que les vaisseaux envahissants et les cellules immunitaires recrutées conduisent conjointement à l’érosion du cartilage.
Des traitements adaptés aux différents stress articulaires
Pour tester si ces signaux distincts avaient vraiment de l’importance, l’équipe a traité des souris pendant le développement de la maladie avec des médicaments bloquant des voies spécifiques. Dans la TMJOA induite par APC, le blocage du TNF‑alpha avec l’agent étanercept protégeait nettement le cartilage, tandis qu’un médicament ciblant les récepteurs attirant les neutrophiles (Navarixin) présentait peu d’effet. En revanche, dans la TMJOA induite par UAC, Navarixin atténuait significativement les dommages cartilagineux, en accord avec un processus pathologique davantage dépendant de l’invasion vasculaire et du remodelage guidés par les neutrophiles, tandis qu’etanercept avait un effet plus faible. Ces résultats suggèrent que l’arthrose de l’ATM n’est pas une maladie unique mais un ensemble d’affections apparentées façonnées par le type de stress exercé sur l’articulation, et que des thérapies efficaces devront peut‑être être adaptées aux schémas mécaniques et cellulaires spécifiques de chaque patient.
Ce que cela signifie pour les personnes souffrant de douleurs mandibulaires
Pour quelqu’un qui souffre de claquements mandibulaires, de douleur ou d’une ouverture limitée, cette recherche met en évidence deux idées clés. Premièrement, l’articulation de la mâchoire est entretenue par une communauté diverse de cellules cartilagineuses et immunitaires qui peuvent soit protéger soit endommager le tissu selon leur mode d’activation. Deuxièmement, différents problèmes d’occlusion peuvent pousser cette communauté vers des voies nocives distinctes — l’une davantage conduite par l’inflammation classique, l’autre par une croissance vasculaire anormale et le remodelage os‑cartilage. À long terme, ce type de cartographie unicellulaire pourrait aider dentistes et médecins à dépasser les traitements universels pour adopter des approches combinant correction occlusale et médicaments ciblés choisis en fonction du profil de lésion articulaire du patient.
Citation: Wang, K., Li, Y., Xiang, S. et al. Single-cell transcriptional atlas reveals distinct immune-chondrocyte crosstalk mechanisms in temporomandibular joint osteoarthritis induced by different types of occlusal disorder. Int J Oral Sci 18, 22 (2026). https://doi.org/10.1038/s41368-025-00424-1
Mots-clés: arthrose de l’articulation temporo‑mandibulaire, séquençage ARN unicellulaire, chondrocytes, neutrophiles, trouble occlusal