Clear Sky Science · fr
L’implantation réveille le potentiel ostéogénique péri-implantaire via la transduction mécanique médiée par l’axe Snx5–EGFR
Pourquoi conserver l’os mandibulaire après une perte dentaire est important
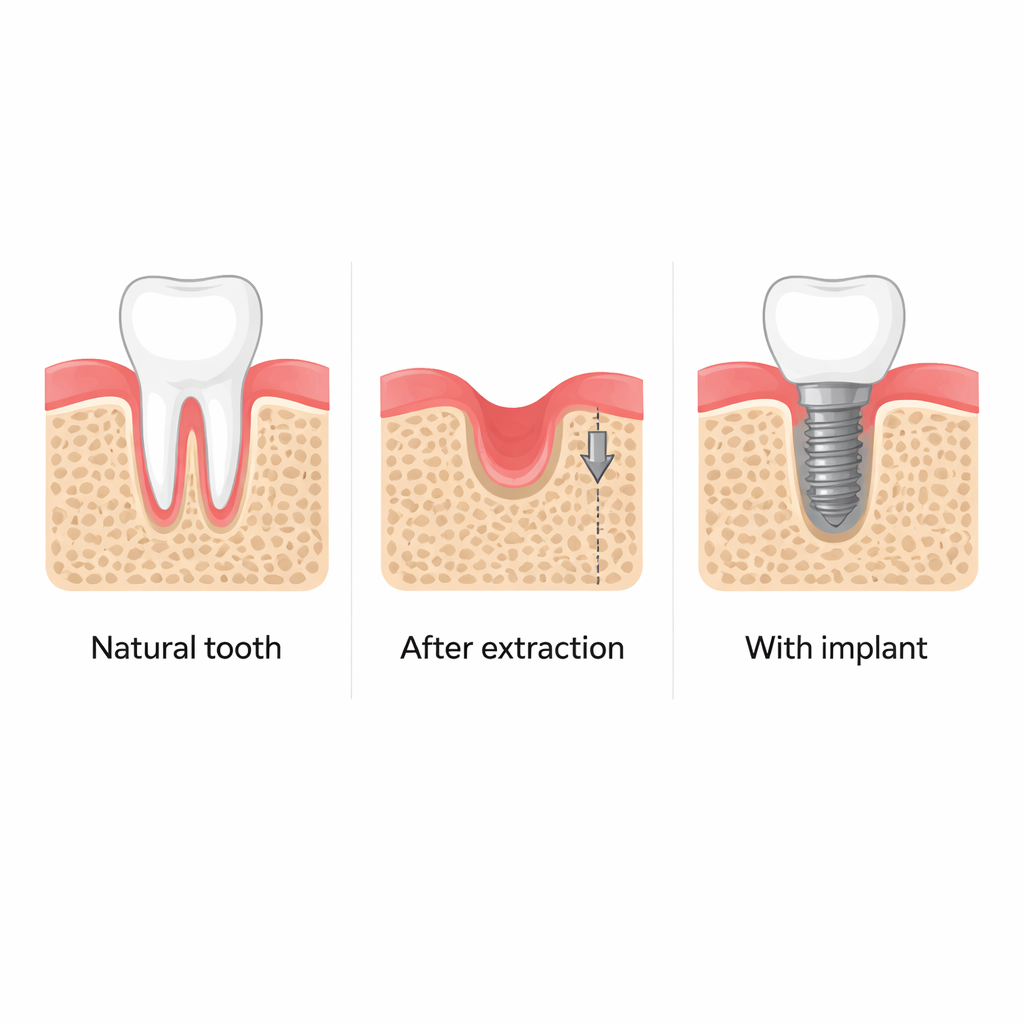
Lorsque l’on extrait une dent, l’os alvéolaire environnant régresse souvent, compliquant la pose ultérieure d’implants dentaires stables et affectant l’apparence du visage. Les cliniciens observent depuis longtemps que le simple fait d’insérer un implant dans une alvéole fraîche semble aider à préserver cet os, même avant que l’implant ne soit mis à contribution pour la mastication. Cette étude pose une question simple mais importante : comment l’acte même de placer un implant « réveille‑t‑il » le système de réparation osseuse, et peut‑on exploiter ce mécanisme pour améliorer la régénération mandibulaire ?
Les implants, protecteurs discrets de l’os
Des examens cliniques chez des patients et des expériences approfondies chez la souris confirment que la pose d’un implant peu de temps après l’extraction aide à maintenir la hauteur et l’épaisseur de l’os alvéolaire adjacent. En revanche, les alvéoles laissées à la guérison naturelle perdent une quantité importante d’os sur plusieurs mois. Autour des implants, les chercheurs ont trouvé davantage de cellules précurseures immatures de l’os (ostéoprogéniteurs), ce qui indique que le tissu voisin de la tige métallique est biologiquement plus actif. Cette activité accrue semble être provoquée non pas par les forces de mastication, mais par les contraintes mécaniques inhabituelles générées lorsqu’un implant ajusté est vissé dans un os légèrement sous‑dimensionné.
Un interrupteur caché à l’intérieur des cellules souches osseuses
L’équipe s’est concentrée sur un groupe particulier de cellules souches de la moelle osseuse marquées par une protéine appelée LepR, connues pour être des fournisseurs clés de nouvel os chez l’adulte. En comparant l’activité génique de ces cellules issues d’os normal, d’os adjacent à un implant et de cellules soumises à un stress mécanique en laboratoire, ils ont identifié une molécule, le sorting nexin 5 (Snx5), dont les niveaux diminuaient systématiquement en présence d’indices mécaniques. Dans les régions autour des implants, les cellules LepR à faible expression de Snx5 étaient plus susceptibles de porter des marqueurs d’ostéogenèse précoce, ce qui suggère que la réduction de Snx5 favorise la transition de ces cellules souches « silencieuses » vers un état actif de formation osseuse.
Lorsque l’interrupteur est défaillant, l’os ne perçoit plus correctement les forces
Pour vérifier la fonction de Snx5, les chercheurs ont utilisé des souris et des cellules souches dépourvues de cette protéine. En l’absence de Snx5, les cellules souches présentaient une tendance marquée et intrinsèque à fabriquer de l’os, même sans stimulation supplémentaire. Mais lorsque les scientifiques ont appliqué une mise en tension mécanique — reproduisant les contraintes proches d’un implant — les cellules normales augmentaient nettement leur activité ostéogénique, alors que les cellules déficientes en Snx5 y répondaient à peine. Chez l’animal vivant, les implants chez des animaux normaux déclenchaient une formation osseuse nette autour de la tige en titane. En revanche, les souris sans Snx5 n’acquéraient pas d’os supplémentaire après implantation, révélant que Snx5 est crucial pour convertir les signaux mécaniques en réparation osseuse supplémentaire plutôt que pour la formation osseuse de base elle‑même.
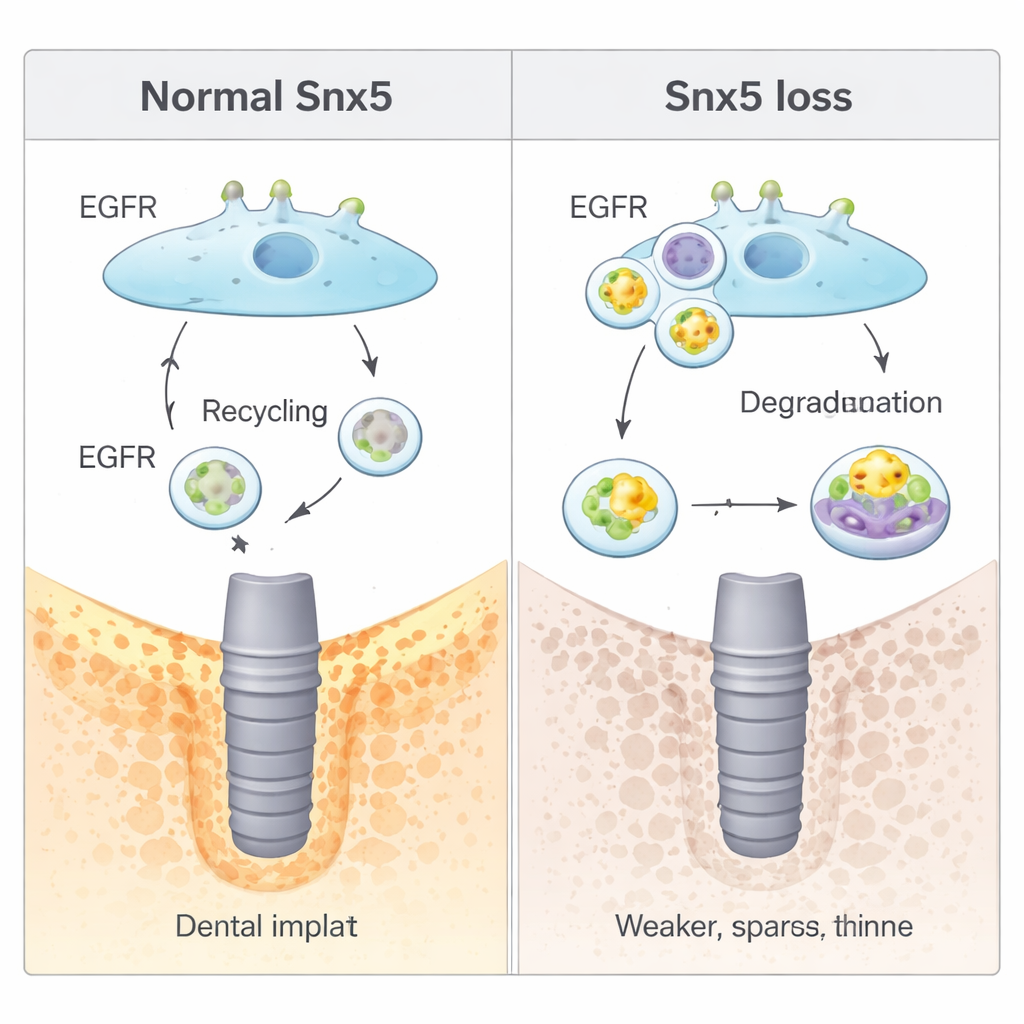
Comment une voie de recyclage contrôle les signaux osseux
L’étude a ensuite mis au jour le mécanisme moléculaire de Snx5. De nombreux signaux de croissance passent par des récepteurs à la surface cellulaire qui sont constamment internalisés puis recyclés ou détruits. Snx5 appartient à une famille de protéines de « tri » qui orientent ce trafic. Ici, Snx5 a été montré comme dirigeant le récepteur du facteur de croissance épidermique (EGFR) — un régulateur clé de la croissance cellulaire et de la différenciation osseuse — de retour vers la membrane après internalisation. En l’absence de Snx5, davantage d’EGFR était envoyé vers des compartiments « digestifs » cellulaires (lysosomes) et dégradé. Cette réduction du signal EGFR augmentait de manière inattendue la formation osseuse de base, mais rendait les cellules moins aptes à ajuster leur comportement lorsque les forces mécaniques changeaient. Des médicaments activant artificiellement l’EGFR atténuaient la formation osseuse supplémentaire observée sans Snx5, tandis que des inhibiteurs de la dégradation lysosomale rétablissaient les signaux EGFR et réduisaient à nouveau la formation osseuse.
Ce que cela signifie pour les futurs patients porteurs d’implants
Pour un non‑spécialiste, ces résultats suggèrent que l’os mandibulaire contient un système intégré capable de détecter la subtile poussée et traction créées quand un implant est placé, et de traduire cela en croissance osseuse supplémentaire. Snx5 agit comme un contrôleur de circulation qui maintient un récepteur de croissance clé, l’EGFR, en cycle à un niveau optimal pour que les cellules souches osseuses puissent « entendre » et répondre à ces murmures mécaniques. Lorsque ce contrôleur est altéré, l’os peut se former plus facilement au repos mais perd sa réponse fine aux forces. Comprendre cet axe Snx5–EGFR ouvre la voie à de nouveaux traitements — médicaments ou revêtements d’implants — susceptibles d’ajuster la sensibilité mécanique de l’os, aidant à préserver la mandibule et à améliorer le succès implantaire dans des situations cliniques difficiles.
Citation: Jiang, X., Weng, Y., Feng, Y. et al. Implantation awakens peri-implant osteogenic potential via Snx5-EGFR axis-mediated mechanical transduction. Int J Oral Sci 18, 18 (2026). https://doi.org/10.1038/s41368-025-00423-2
Mots-clés: implants dentaires, régénération de l’os mandibulaire, mécanotransduction, cellules souches osseuses, signalisation EGFR