Clear Sky Science · fr
La lactylation de ZEB2, pilotée par la voie glycolytique KDM6B/Pdk1, favorise la formation du cément cellulaire
Pourquoi protéger les racines dentaires est important
La maladie des gencives, ou parodontite, est l’une des principales causes de perte de dents chez l’adulte. Au fur et à mesure de son évolution, elle ronge en silence les tissus qui ancrent les dents dans la mâchoire. L’un des plus importants est le cément, une couche mince de type osseux qui recouvre la surface de la racine et permet à la dent de s’attacher au ligament et à l’os environnants. Une fois le cément perdu, les dents se déchaussent et peuvent finir par tomber. Cette étude pose une question simple mais puissante : peut-on comprendre, au niveau moléculaire, comment le cément se construit, afin qu’un jour on puisse aider l’organisme à le reconstruire et à maintenir les dents en place toute la vie ?
Des cellules qui soutiennent la dent vers une cible thérapeutique
Le cément est produit par des cellules spécialisées appelées cémentoblastes, qui reposent sur la surface de la racine et déposent un nouvel élément minéral. Ces cellules se rapprochent beaucoup des ostéoblastes (cellules formatrices d’os), mais les signaux qui leur indiquent quand et comment construire le cément restaient mal connus. Les chercheurs se sont concentrés sur une molécule nommée KDM6B, une enzyme qui modifie des marques chimiques sur les protéines qui emballent l’ADN et peut activer des gènes. En étudiant des dents de souris à différents âges et des cémentoblastes cultivés en laboratoire, ils ont observé que les niveaux de KDM6B augmentent durant la phase active de formation du cément puis diminuent quand la croissance ralentit. Quand KDM6B a été bloquée dans les cellules ou chez la souris, l’activité des cémentoblastes a chuté et la partie « cellulaire » du cément — la portion plus épaisse et vivante proche de l’apex radiculaire — est devenue plus fine, suggérant que KDM6B est un moteur clé d’une croissance saine du cément.
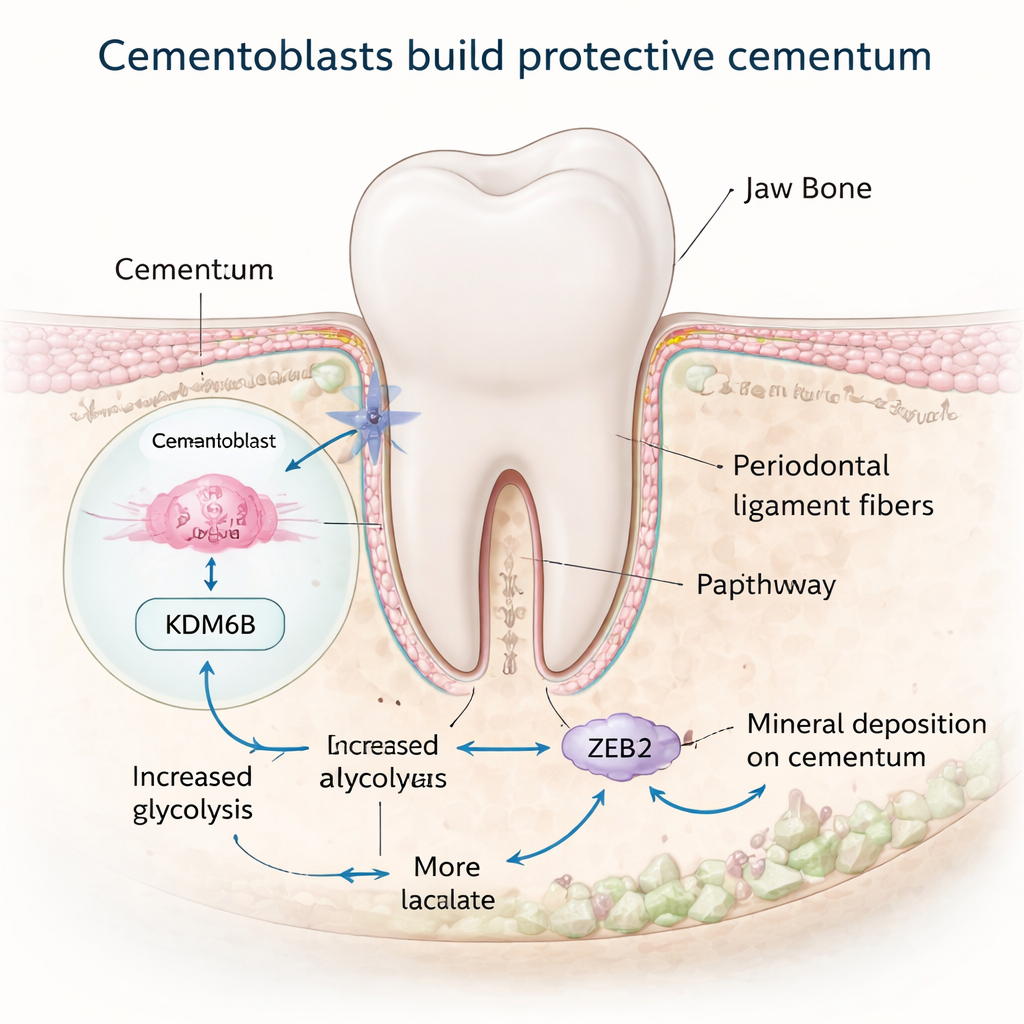
Reconfigurer le métabolisme cellulaire pour construire du minéral
Construire un tissu minéralisé demande beaucoup d’énergie, et de nombreuses cellules adaptent leur métabolisme en un mode haute performance pendant ce processus. L’équipe a découvert que KDM6B aide les cémentoblastes à reconfigurer leur utilisation du glucose. Normalement, ces cellules favorisent une voie appelée glycolyse, qui dégrade rapidement le glucose et produit du lactate. Quand KDM6B était réduit, les gènes impliqués dans la glycolyse étaient réprimés, tandis que ceux associés à une production d’énergie plus lente et dépendante de l’oxygène étaient soit inchangés soit augmentés, et les cellules produisaient moins d’énergie au total. Un acteur central de ce basculement est une enzyme nommée PDK1. Grâce à des outils de cartographie du génome, les chercheurs ont montré que KDM6B enlève physiquement une marque répressive sur la région d’ADN contrôlant le gène Pdk1, permettant ainsi l’augmentation de PDK1. Restaurer PDK1 dans des cellules déficientes en KDM6B a remis en place de nombreux marqueurs de minéralisation, révélant un commutateur métabolique KDM6B–PDK1 qui alimente les cémentoblastes.
Transformer le lactate de déchet en signal utile
Le lactate est souvent perçu comme un produit de déchet des muscles qui travaillent dur, mais des travaux récents montrent qu’il peut aussi agir comme un signal qui modifie des protéines. Ici, une glycolyse accrue pilotée par KDM6B et PDK1 a augmenté la production de lactate dans les cémentoblastes. Les chercheurs ont ensuite suivi un type plus récent de modification des protéines appelé lactylation, dans lequel des groupes dérivés du lactate sont attachés à des sites protéiques spécifiques. Ils ont constaté que les niveaux de lactylation dans les cémentoblastes augmentaient durant les périodes de formation active du cément et diminuaient chez les souris plus âgées et dans les cellules déficientes en KDM6B. L’ajout de lactate sodique simple au système a augmenté la lactylation, réactivé les gènes liés à la minéralisation et restauré la formation de nodules minéraux à la fois en culture cellulaire et dans un modèle murin, même lorsque KDM6B était bloqué. Cela suggère que le lactate lui‑même peut contribuer à rattraper une activité de construction du cément affaiblie.
Un renfort moléculaire pour un régulateur clé du cément
L’équipe s’est ensuite demandée quelles protéines étaient « décorées » par le lactate d’une manière significative pour le cément. Ils ont ciblé ZEB2, une protéine de régulation génétique déjà connue pour promouvoir la minéralisation par les cémentoblastes. En utilisant des techniques de cartographie protéique, ils ont identifié des sites précis sur ZEB2 portant des marques de lactylation et montré que la modification d’un site critique affaiblissait la capacité de la cellule à activer les gènes de minéralisation. Des expériences supplémentaires ont démontré que la voie KDM6B–PDK1 augmente la lactylation de ZEB2 et que l’apport de lactate supplémentaire peut restaurer l’activité de ZEB2 quand PDK1 est bas. En substance, métabolisme et contrôle génétique sont liés : la dégradation du sucre alimente la production de lactate, qui module ensuite finement ZEB2 pour maintenir fortement les programmes de construction du cément.
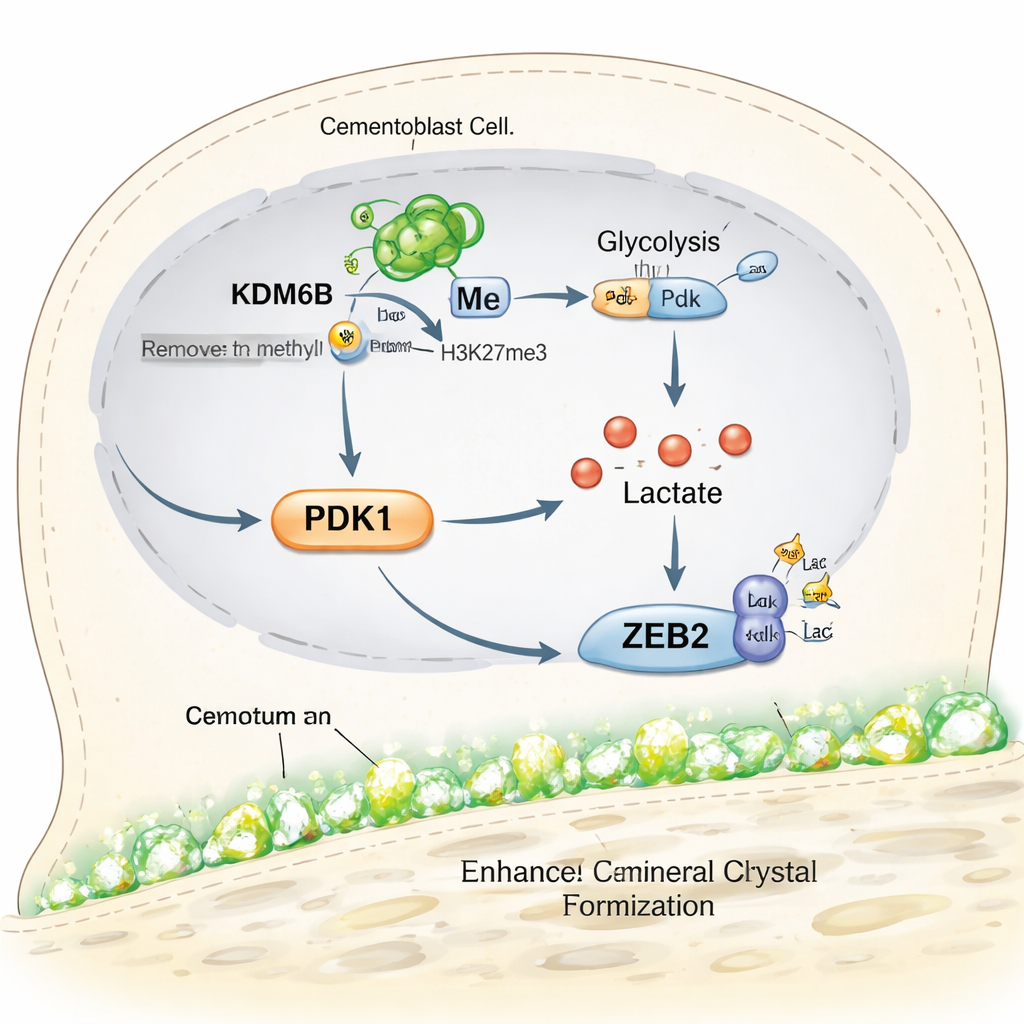
Ce que cela signifie pour de futures thérapies sauvegardant les dents
En termes simples, l’étude révèle une chaîne d’événements au sein des cellules formant le cément : l’enzyme KDM6B ouvre le gène Pdk1, PDK1 pousse les cellules vers un usage rapide du sucre, ce métabolisme génère du lactate, et le lactate module chimiquement la protéine ZEB2 pour stimuler le dépôt minéral. Lorsque n’importe quel maillon de cette chaîne est bloqué, la croissance du cément faiblit, mais l’ajout contrôlé de lactate peut en partie la restaurer. Pour les patients, ces résultats ne constituent pas encore un traitement clinique, mais ils mettent en lumière des cibles précises pour des médicaments ou des biomatériaux visant à régénérer le cément et à stabiliser les dents dans les formes avancées de maladie parodontale. Ils suggèrent aussi que des « commutateurs » métaboliques similaires pourraient être exploités pour favoriser la guérison osseuse ailleurs dans le corps.
Citation: Yang, Z., Wang, H., Xiao, J. et al. KDM6B/Pdk1 glycolytic pathway-driven ZEB2 lactylation promotes cellular cementum formation. Int J Oral Sci 18, 21 (2026). https://doi.org/10.1038/s41368-025-00420-5
Mots-clés: régénération du cément, parodontite, métabolisme des cémentoblastes, déméthylase des histones KDM6B, lactylation des protéines