Clear Sky Science · fr
Identification des cellules souches odontogéniques GLDN+ comme essentielles au développement et à la régénération des dents humaines
Pourquoi il est important de faire repousser des dents
Les traitements de canal sauvent de nombreuses dents, mais ils le font en retirant la pulpe vivante à l’intérieur. Cette pulpe contient des nerfs, des vaisseaux sanguins et des cellules réparatrices qui maintiennent la dent en bonne santé. Une fois supprimée, la dent devient plus fragile et perd une grande partie de son système de défense naturel. Les scientifiques espèrent depuis longtemps régénérer une pulpe vivante plutôt que de la remplacer par des obturations inertes, mais cela exige un contrôle précis des cellules souches qui forment la dentine et la pulpe pendant le développement. Cette étude révèle un groupe de cellules souches jusque-là non reconnu dans les dents humaines en développement, qui semblent être des architectes clés des parties dures et molles de la dent.
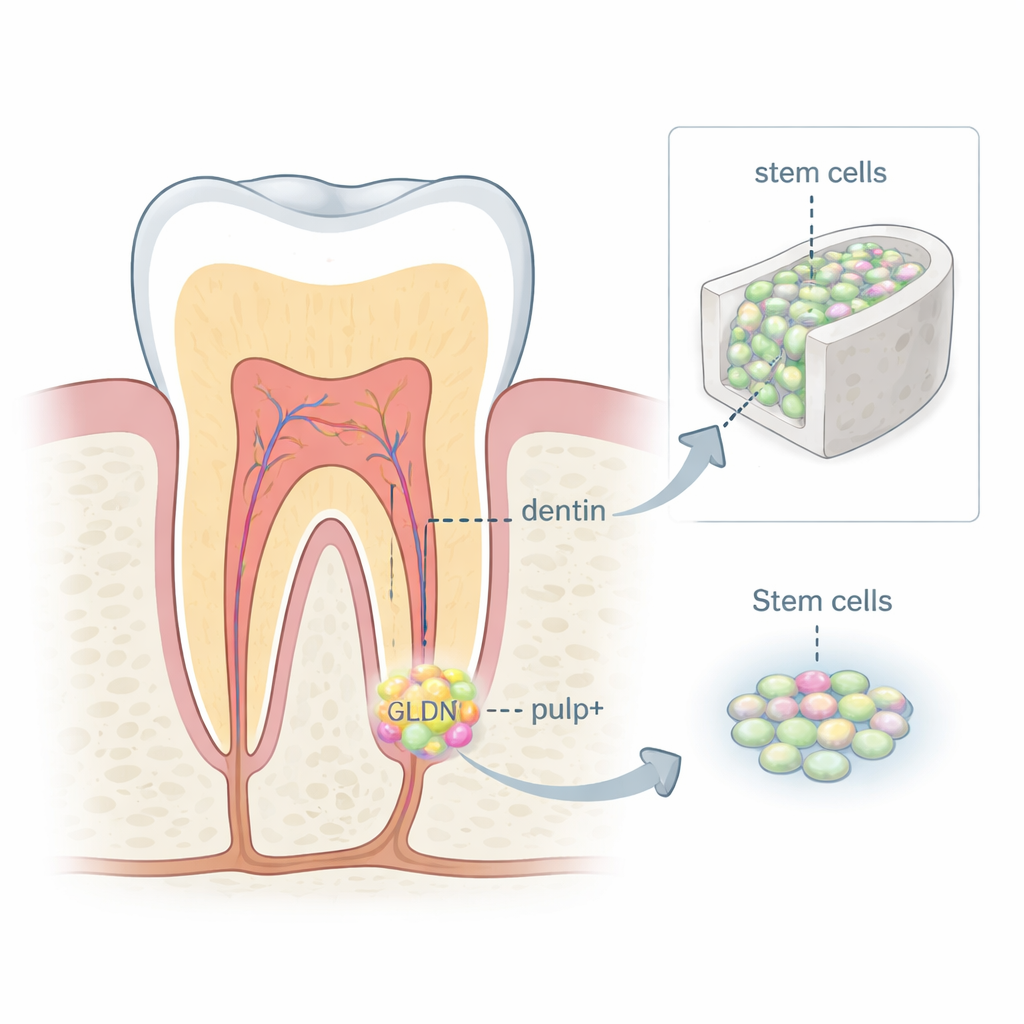
Des bâtisseurs cachés à l’intérieur des jeunes dents
Lors de la formation initiale de la dent, une structure molle appelée papille dentaire se situe sous la future couronne et la racine. Elle est remplie de cellules souches mésenchymateuses qui créent finalement la dentine (la couche dure sous l’émail) et la pulpe dentaire. En utilisant le séquençage ARN unicellulaire, qui mesure l’activité de milliers de gènes dans des cellules individuelles, les chercheurs ont cartographié tous les types cellulaires présents dans la papille dentaire humaine issue de dents de sagesse en développement. Ils ont constaté que ce tissu est loin d’être uniforme : il contient des cellules immunitaires, endothéliales, nerveuses et plusieurs sous-groupes distincts de cellules souches, chacun avec son propre profil génétique et son rôle probable dans la construction dentaire.
Identification du sous-ensemble de cellules souches GLDN+
Parmi les différents clusters de cellules souches, un groupe s’est distingué. Ces cellules exprimaient fortement une protéine de surface appelée gliomédine (GLDN), ainsi que d’autres marqueurs liés aux étapes précoces de la formation dentaire. Les cellules GLDN+ étaient principalement situées autour de la zone où la racine en croissance rencontre la papille molle, près d’une fine structure épithéliale qui guide le façonnage de la racine. L’analyse du développement suggère que ces cellules GLDN+ dérivent de précurseurs encore plus précoces, puis migrent vers la couronne et la racine où elles mûrissent en odontoblastes (cellules productrices de dentine) et en cellules participant à la formation de la matrice pulpaire. La microscopie de tissus dentaires humains à plusieurs stades a montré que les cellules GLDN+ augmentent d’abord près de la dentine en formation, puis déclinent progressivement à mesure que le canal radiculaire mature, ce qui indique qu’elles sont les plus actives pendant la fenêtre où la pulpe et la dentine sont déposées.
Des cellules souches qui construisent et attirent les vaisseaux sanguins
Pour tester l’originalité de ces cellules, l’équipe a isolé des cellules GLDN+ et GLDN− de la papille dentaire humaine par tri cellulaire. Les deux se comportaient comme des cellules souches mésenchymateuses, mais les GLDN+ surpassaient leurs homologues : elles formaient plus de colonies, proliféraient plus vite, migraient plus facilement et produisaient davantage de dépôts minéraux dans des conditions favorisant la formation de tissu dur. Elles produisaient aussi des niveaux plus élevés de protéines clés liées à la dentine. Peut-être plus important encore, lorsque les chercheurs ont prélevé le milieu dans lequel les cellules GLDN+ avaient été cultivées et l’ont appliqué à des cellules endothéliales humaines (les cellules tapissant les vaisseaux sanguins), ces dernières ont migré davantage et formé plus de réseaux vasculaires en tubes. Cela signifie que les cellules GLDN+ non seulement forment elles-mêmes un tissu semblable à la dentine, mais envoient aussi des signaux aidant à assembler l’apport sanguin vital de la pulpe.
Régénérer la pulpe dans un échafaudage dentaire
La preuve la plus convaincante provient d’un modèle animal conçu pour imiter la régénération pulpaire. Les scientifiques ont préparé des tubes de dentine creusés et traités chimiquement à partir de dents humaines extraites, et les ont remplis de gel de collagène contenant soit des cellules GLDN+, soit des cellules GLDN−, soit aucune cellule. Ces constructions ont été implantées sous la peau de souris. Après quatre semaines, le groupe GLDN+ présentait un tissu dense et organisé de type pulpaire à l’intérieur du tube de dentine, avec une couche distincte de cellules ressemblant à des odontoblastes tapissant la surface interne de la dentine et un réseau plus riche de vaisseaux sanguins et de fibres de collagène que dans les autres groupes. Cela a démontré que les cellules GLDN+ peuvent reconstruire un complexe pulpe-dentine vascularisé en milieu vivant, leur valant le nom de « cellules souches odontogéniques GLDN+ ».
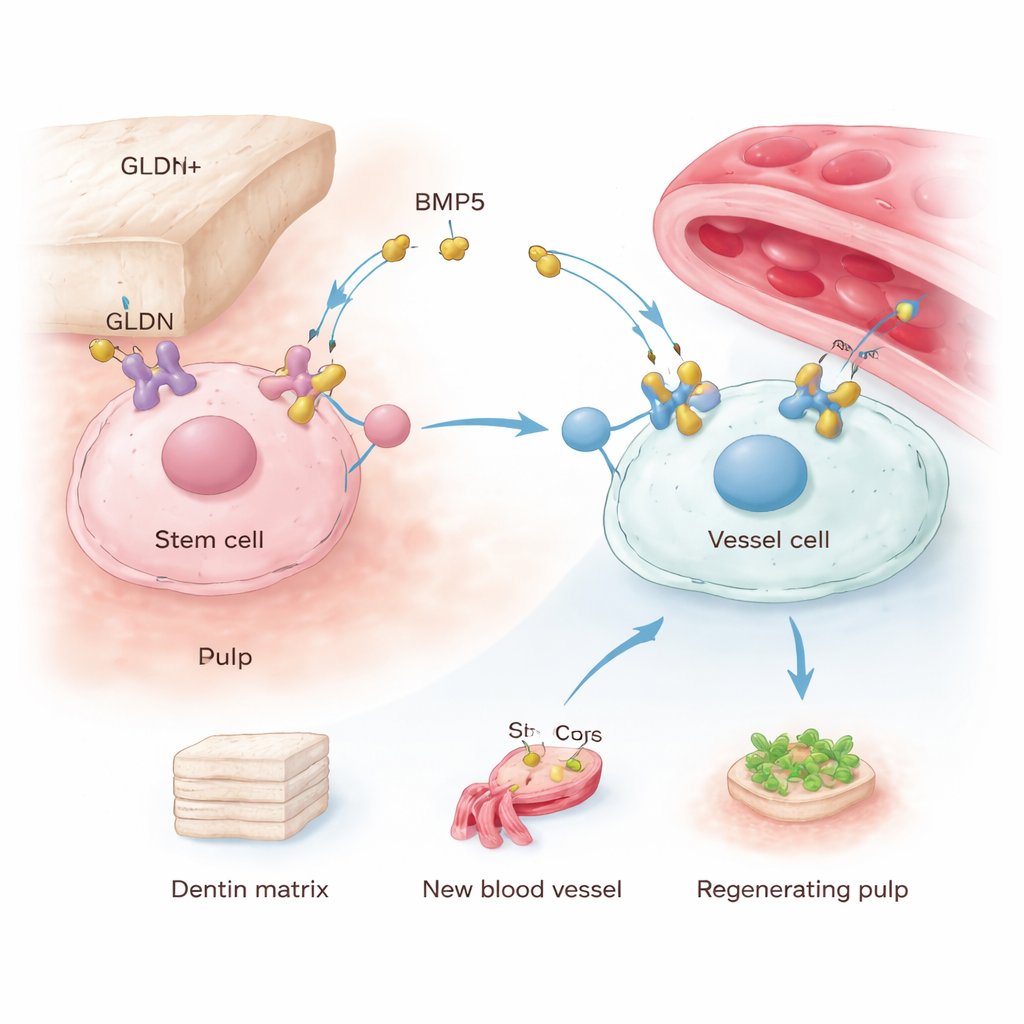
Comment les signaux GLDN pilotent la réparation dentaire
Les chercheurs se sont ensuite intéressés aux raisons de la puissance de ces cellules. En examinant les signaux de communication entre les cellules GLDN+ et les cellules vasculaires voisines, ils ont identifié la protéine morphogénétique osseuse 5 (BMP5) comme un facteur sécrété clé. Les cellules GLDN+ produisaient plus de BMP5 et présentaient une activation plus élevée d’une cascade de signalisation en aval à l’intérieur de la cellule, connue par les protéines SMAD1/5/9, liée à la formation osseuse et vasculaire. Lorsque le GLDN de ces cellules était supprimé, leur croissance, leur mobilité, leur minéralisation et leur capacité à stimuler la formation de vaisseaux diminuaient, ainsi que les niveaux de BMP5 et l’activation des SMAD. La réduction directe de BMP5 avait des effets similaires, tandis que l’ajout de BMP5 supplémentaire à des cellules moins puissantes augmentait leur minéralisation et leur soutien à la croissance vasculaire. Ensemble, ces expériences dévoilent un axe GLDN–BMP5–SMAD qui aide les cellules GLDN+ à conserver leur identité et à orchestrer à la fois la production de dentine et l’angiogenèse.
Ce que cela signifie pour les soins dentaires futurs
Pour le grand public, le message est que les chercheurs ont identifié un sous-ensemble de cellules souches très performant dans les dents humaines en développement, capable de construire à la fois l’enveloppe dure de dentine et la pulpe vivante riche en sang. Ces cellules souches odontogéniques GLDN+ utilisent une voie de signalisation spécifique, centrée sur BMP5, pour se renouveler, former du tissu minéralisé et attirer les vaisseaux sanguins. À long terme, exploiter ces cellules — ou imiter leurs signaux sécrétés — pourrait permettre des traitements visant à reconstruire une pulpe vivante dans des dents abîmées par la carie ou un traumatisme, offrant potentiellement une alternative aux traitements endodontiques traditionnels et ouvrant des perspectives pour la réparation osseuse et neurovasculaire plus large.
Citation: Liao, C., Liu, J., Li, M. et al. Identification of GLDN+ odontogenic stem cells as crucial for human tooth development and regeneration. Int J Oral Sci 18, 20 (2026). https://doi.org/10.1038/s41368-025-00419-y
Mots-clés: régénération de la pulpe dentaire, cellules souches odontogéniques, GLDN, signalisation BMP5, développement dentaire