Clear Sky Science · fr
Aperçus structuraux des mutations associées à des maladies dans la machinerie de traitement des microARN
Comment de minuscules ciseaux à ARN façonnent la santé et la maladie
À l’intérieur de chaque cellule, un système discret d’édition tronque les messages génétiques avant leur lecture. Ce système repose sur de minuscules fragments d’ARN appelés microARN, qui font office de boutons de réglage fin pour des milliers de gènes à la fois. Quand les « machines » moléculaires qui fabriquent les microARN fonctionnent correctement, les cellules croissent, se divisent et se spécialisent de manière contrôlée. Mais lorsque ces machines sont altérées par des mutations, l’équilibre de l’activité génique peut basculer vers le cancer, des maladies du sang ou des troubles du développement cérébral. Cet article explique comment la compréhension des formes 3D de ces machines aide les scientifiques à identifier ce qui déraille et comment on pourrait y remédier.
La boîte à outils cellulaire pour atténuer les gènes
Les microARN sont de courts fragments d’ARN, d’environ 22 nucléotides, qui ne codent pas eux-mêmes des protéines. Au lieu de cela, ils se lient à des ARN messagers plus longs et soit les marquent pour destruction, soit bloquent leur traduction, réduisant ainsi l’expression des gènes plutôt que de l’éteindre complètement. Pour fabriquer ces microARN, les cellules acheminent de longs précurseurs d’ARN à travers une chaîne de montage soigneusement orchestrée. D’abord, l’enzyme DROSHA tranche les longs transcrits primaires dans le noyau en courtes structures en épingle. Ces fragments migrent ensuite vers le cytoplasme, où une autre enzyme, DICER, mesure et coupe ces épingles en duplex de la taille des microARN. Enfin, un brin de chaque duplex est chargé dans une protéine appelée Argonaute 2 (AGO2), qui utilise le microARN comme guide pour trouver les messages correspondants et les réprimer. 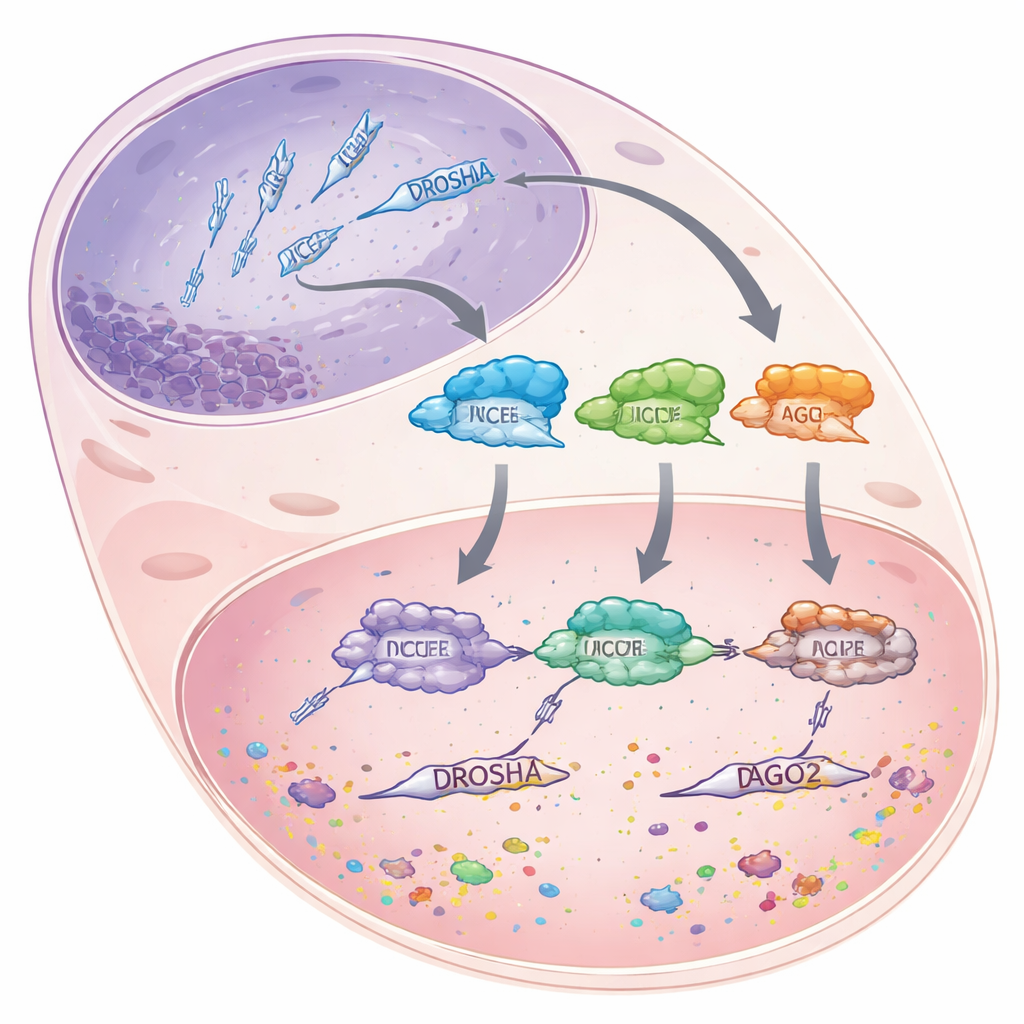
Des formes délicates pour des tâches de précision
DROSHA, DICER et AGO2 ne sont pas de simples ciseaux ; chacun est composé de plusieurs parties interactives qui doivent bouger de manière chorégraphiée. DROSHA travaille avec une protéine partenaire, DGCR8, pour saisir les extrémités d’une épingle primaire de microARN et juger avec précision l’endroit de la coupe. DICER utilise une sorte de règle intégrée formée par ses domaines pour fixer une distance précise entre l’endroit où il tient l’extrémité de l’épingle et le centre catalytique qui effectue la coupure. AGO2 enrobe un seul brin de microARN de sorte que sa région « seed » soit parfaitement exposée pour reconnaître les cibles, tandis que des ions métalliques et des acides aminés clés dans son cœur s’alignent pour sectionner ces cibles lorsque l’appariement est suffisamment fort. Dans les trois protéines, des sillons chargés positivement et des liaisons flexibles guident les brins d’ARN en place, tandis que des poches de liaison aux métaux et des résidus catalytiques réalisent les coupures chimiques.
Quand les ciseaux sont tordus ou émoussés
Des études génétiques chez des patients atteints de cancers, de maladies hématologiques et de syndromes du développement neuro ont mis au jour des grappes de mutations dans ces machines à microARN. Beaucoup des altérations les plus délétères se situent directement dans les centres catalytiques ou sur des surfaces de préhension serrées de l’ARN. Dans DROSHA, par exemple, des substitutions comme E1147K et D1219G se trouvent au cœur du site de coupe et perturbent la capacité à retenir des ions métalliques essentiels, laissant l’enzyme incapable de traiter les microARN primaires. D’autres mutations de DROSHA, telles que des troncatures qui retirent la région catalytique ou des modifications qui déstabilisent ses hélices de support, affaiblissent le complexe entier et entraînent une baisse globale des niveaux de microARN dans le tératome rénal de l’enfant (tumeur de Wilms), des troubles de la moelle osseuse et des maladies du système nerveux. Dans DICER, des mutations récurrentes se regroupent dans l’un de ses deux domaines de coupe, faussant la production de sorte qu’un bras du duplex microARN est perdu, ce qui décale l’équilibre entre signaux favorisant la croissance et signaux la réprimant. 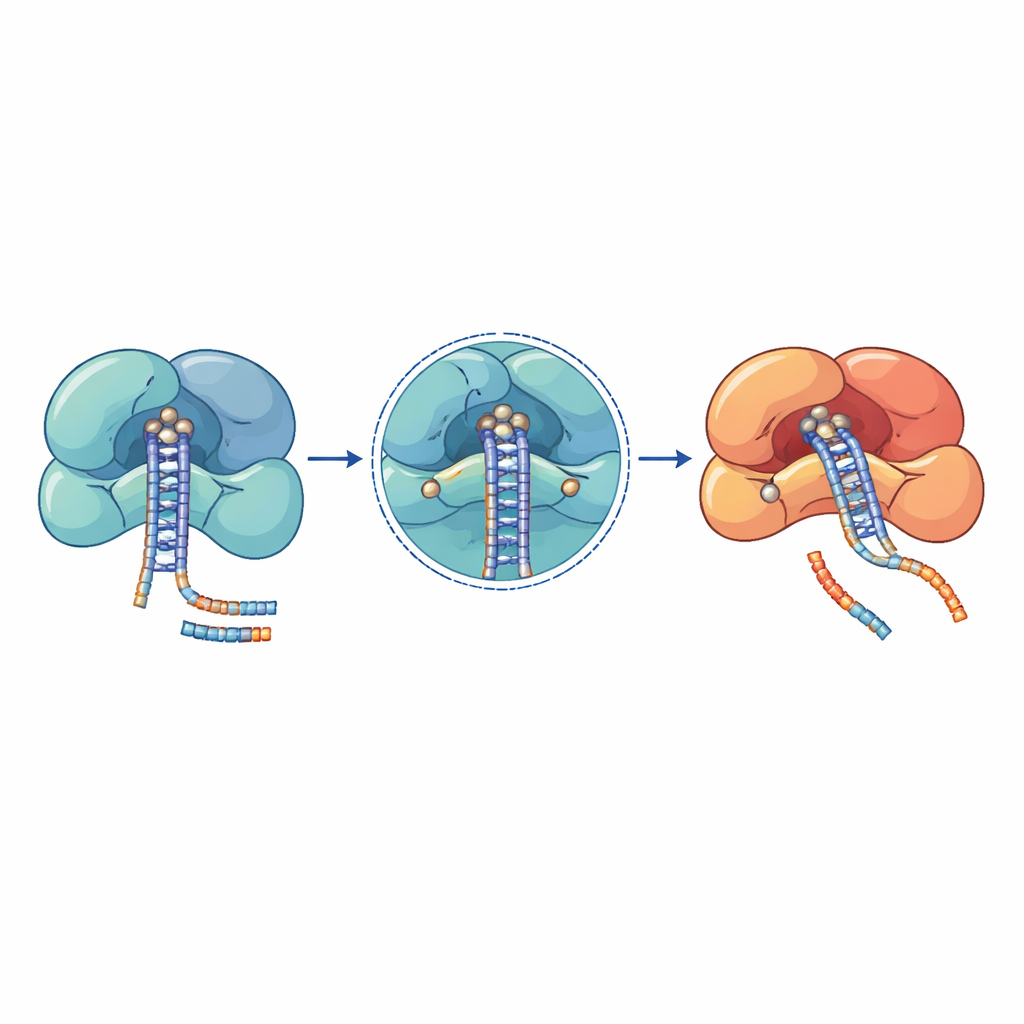
Guides mal alignés dans le cerveau et au-delà
Les mutations d’AGO2 racontent une histoire différente mais apparentée. Les atteintes directes au cœur catalytique sont rares, probablement parce qu’elles seraient létales tôt dans le développement. En revanche, les variants associés à la maladie apparaissent souvent dans des régions de liaison flexibles et aux jonctions de domaines qui maintiennent la forme d’AGO2. Dans le syndrome de Lessel–Kreienkamp, une affection neurodéveloppementale, des mutations dans ces liaisons et sur les surfaces avoisinantes tordent subtilement la manière dont les parties PAZ, MID et PIWI d’AGO2 s’assemblent et se meuvent. Cela peut désaligner le microARN guide ou affaiblir son adhérence aux ARN cibles, brouillant la précision de la répression génique pendant le développement cérébral. Des changements structuraux similaires n’importe où le long de la voie des microARN—que ce soit dans DROSHA, DICER ou AGO2—peuvent se répercuter et modifier des réseaux entiers de gènes impliqués dans la croissance cellulaire, l’hématopoïèse ou le câblage neuronal.
Transformer les indices structurels en traitements futurs
En superposant les mutations liées aux maladies sur des cartes 3D haute résolution de ces protéines, les chercheurs peuvent catégoriser précisément comment chaque altération provoque un dysfonctionnement—que ce soit en émoussant le tranchant catalytique, en relâchant des contacts critiques avec des partenaires protéiques ou en décalant des hélices clés hors alignement. Ces aperçus structuraux ouvrent la voie à des interventions ciblées : de petites molécules qui stabilisent des interfaces affaiblies, des ARN conçus pour réorienter des enzymes partiellement fonctionnelles vers les bons substrats, ou des composés allostériques qui incitent les protéines mutantes à adopter des conformations plus actives. Pour le lecteur non spécialiste, le message à retenir est que de minuscules ajustements structuraux dans les ciseaux à ARN de la cellule peuvent avoir des effets disproportionnés sur la santé, mais ils offrent aussi des points d’appui précis pour concevoir des thérapies de nouvelle génération, tenant compte des mutations.
Citation: Lee, H., Lee, J. & Roh, SH. Structural insights into disease-associated mutations in the microRNA processing machinery. Exp Mol Med 58, 639–649 (2026). https://doi.org/10.1038/s12276-026-01669-4
Mots-clés: microARN, interférence ARN, DROSHA DICER AGO2, génétique du cancer, troubles du développement neuro