Clear Sky Science · fr
Mécanismes de régulation de la stabilité de la protéine Snail : système ubiquitine–protéasome et autophagie médiée par les chaperons
Pourquoi la propagation du cancer dépend d’une protéine fragile
Le cancer devient vraiment menaçant lorsque des cellules se détachent de la tumeur d’origine et migrent vers des organes distants. Cette dissémination, ou métastase, repose en partie sur une puissante « protéine maître » nommée Snail, qui aide les cellules à relâcher leurs liaisons et à gagner en mobilité. Cet article explique comment nos cellules maintiennent normalement Snail sous contrôle en le dégradant rapidement via deux grands systèmes d’élimination des déchets. Comprendre cet équilibre offre de nouvelles pistes pour ralentir ou prévenir les métastases.
De cellules fortement serrées à des envahisseurs mobiles
Dans les tissus sains, les cellules épithéliales forment des couches ordonnées, semblables à des briques, qui restent en place et adhèrent fermement à leurs voisines. Pour qu’une cellule tumorale s’échappe, elle subit souvent une transformation appelée transition épithélio–mésenchymateuse, ou TEM, au cours de laquelle elle perd ses contacts serrés et acquiert la capacité de migrer et d’envahir. Snail est un moteur clé de cette transformation : lorsqu’il est présent dans le noyau, il réprime des gènes qui maintiennent l’adhésion cellulaire et active des gènes favorisant le mouvement et l’invasion. Des niveaux élevés de Snail sont associés à des cancers agressifs et à un mauvais pronostic, si bien que les cellules ont développé des mécanismes pour maintenir Snail rare et de courte durée de vie dans des conditions normales.
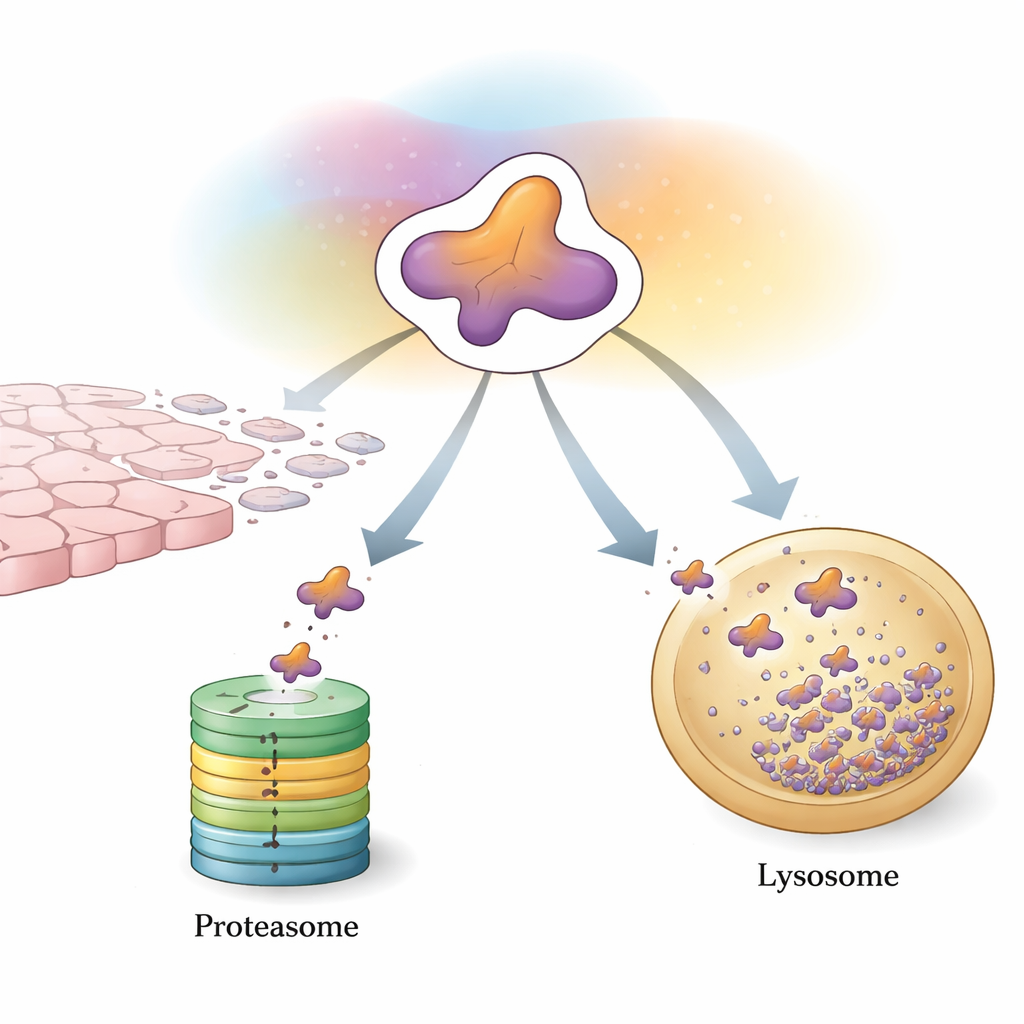
La première ligne de contrôle de la cellule : marquer et broyer
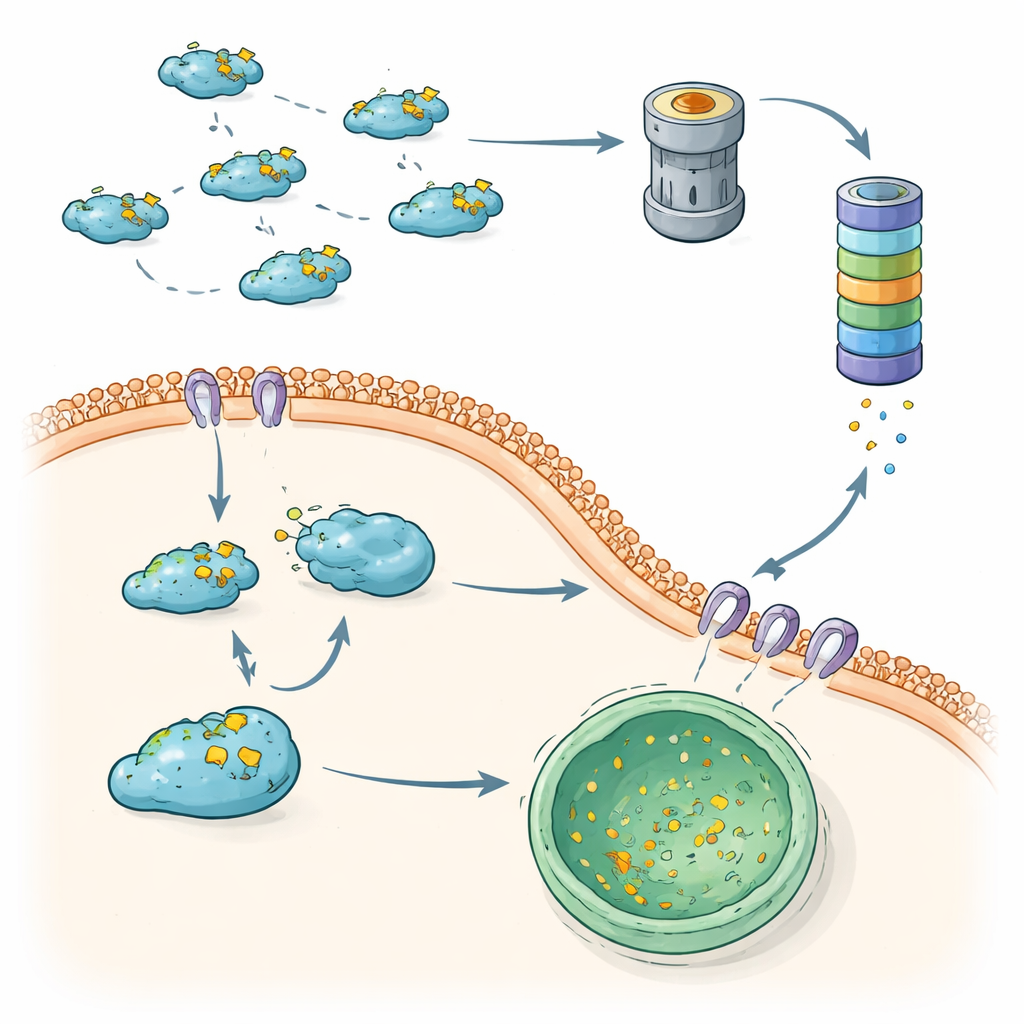
Un des principaux moyens de contrôler Snail est le système ubiquitine–protéasome, une machine qui marque et broie les protéines indésirables. Des enzymes spécialisées fixent de petits « drapeaux » constitués d’une protéine appelée ubiquitine sur Snail. Lorsque suffisamment de ces drapeaux s’accumulent selon un certain motif, Snail est orienté vers le protéasome, un complexe en forme de tonneau qui le découpe en fragments. Une large palette de protéines auxiliaires affine ce processus. Certaines enzymes ajoutent des chaînes favorisant la dégradation qui envoient rapidement Snail au broyeur, contribuant à limiter la croissance tumorale et la dissémination. D’autres ajoutent des chaînes qui stabilisent au contraire Snail ou augmentent indirectement sa production, faisant pencher la balance en faveur de la TEM et des métastases. Des modifications chimiques telles que la phosphorylation et l’acétylation agissent comme des interrupteurs supplémentaires, contrôlant quels auxiliaires peuvent se lier à Snail et si celui-ci sera détruit ou épargné.
Lever le frein : des enzymes qui sauvent Snail
L’histoire ne s’arrête pas au marquage de Snail pour destruction. Un autre groupe d’enzymes, appelé désubiquitinases, peut enlever les drapeaux d’ubiquitine, sauvant ainsi Snail du protéasome. Beaucoup de ces enzymes sont activées ou renforcées dans les cancers, permettant à Snail d’échapper à la dégradation et de persister dans le noyau. Leurs actions dépendent fortement du contexte cellulaire : dans certains cas, elles stabilisent directement Snail, tandis que dans d’autres elles influencent sa localisation dans la cellule ou ses interactions avec des partenaires. Des signaux issus de voies associées au cancer, tels que les facteurs de croissance et les réponses au stress, alimentent ce réseau et décident si Snail sera rapidement éliminé ou autorisé à déclencher le programme de TEM.
Un second filet de sécurité : livraison sélective au centre de recyclage de la cellule
Au-delà du protéasome, les cellules s’appuient sur l’autophagie, un ensemble de voies qui transportent les protéines vers des compartiments acides appelés lysosomes pour y être dégradées. Cette revue met en lumière une forme très sélective connue sous le nom d’autophagie médiée par les chaperons (CMA) comme une deuxième voie majeure de contrôle de Snail. La CMA reconnaît une courte séquence à l’intérieur de Snail et, avec l’aide de protéines d’accompagnement, livre Snail cytoplasmique aux lysosomes pour destruction. Dans des cellules mammaires moins agressives, ce système maintient Snail en grande partie en dehors du noyau et susceptible d’être éliminé par les lysosomes. Dans des cancers du sein plus agressifs, triple négatifs, Snail a tendance à s’accumuler dans le noyau et à échapper à la CMA, renforçant ainsi sa capacité à déclencher la TEM et les métastases.
Quand le contrôle qualité faillit, les métastases prennent l’avantage
Pris ensemble, ces résultats montrent que les cellules utilisent deux axes complémentaires de « contrôle qualité » pour restreindre Snail : la voie ubiquitine–protéasome et la dégradation lysosomale via la CMA. Lorsque les deux fonctionnent correctement, Snail est rapidement éliminé, limitant la TEM et contribuant à empêcher la dissémination des cellules tumorales. Lorsque l’un ou l’autre axe est affaibli—par des altérations des enzymes de marquage, des désubiquitinases ou des composants de la CMA—Snail devient plus stable, s’accumule dans le noyau et favorise fortement le comportement invasif. En cartographiant ces voies interconnectées de dégradation, l’article esquisse de nouvelles possibilités thérapeutiques : des médicaments qui restaurent ou renforcent la dégradation de Snail, ou qui réorientent Snail vers la CMA ou la destruction par le protéasome, pourraient aider à réappliquer les freins sur les métastases sans désactiver complètement ces systèmes essentiels de recyclage des protéines.
Citation: Kim, M., Hong, KS., Kim, T. et al. Regulatory mechanisms for Snail protein stability: ubiquitin–proteasome system and chaperone-mediated autophagy. Exp Mol Med 58, 408–415 (2026). https://doi.org/10.1038/s12276-026-01667-6
Mots-clés: métastase du cancer, transition épithélio–mésenchymateuse, protéine Snail, dégradation des protéines, autophagie