Clear Sky Science · fr
Interactions métaboliques entre fibroblastes associés au cancer, adipocytes et cellules immunitaires comme moteur d’un microenvironnement tumoral immunosuppresseur
Pourquoi le voisinage de la tumeur compte
La tumeur ne se développe pas en isolation. Elle vit dans un environnement animé composé de cellules de soutien, d’adipocytes et de cellules immunitaires qui échangent en permanence nutriments et signaux chimiques. Cet article explique comment le « métabolisme » de ce voisinage — la façon dont les cellules utilisent et partagent leurs combustibles — incline discrètement la balance en faveur de la tumeur et contre le système immunitaire. Comprendre cette économie cachée des sucres, des lipides et des acides aminés ouvre de nouvelles voies pour améliorer les immunothérapies et couper le système de soutien de la tumeur.
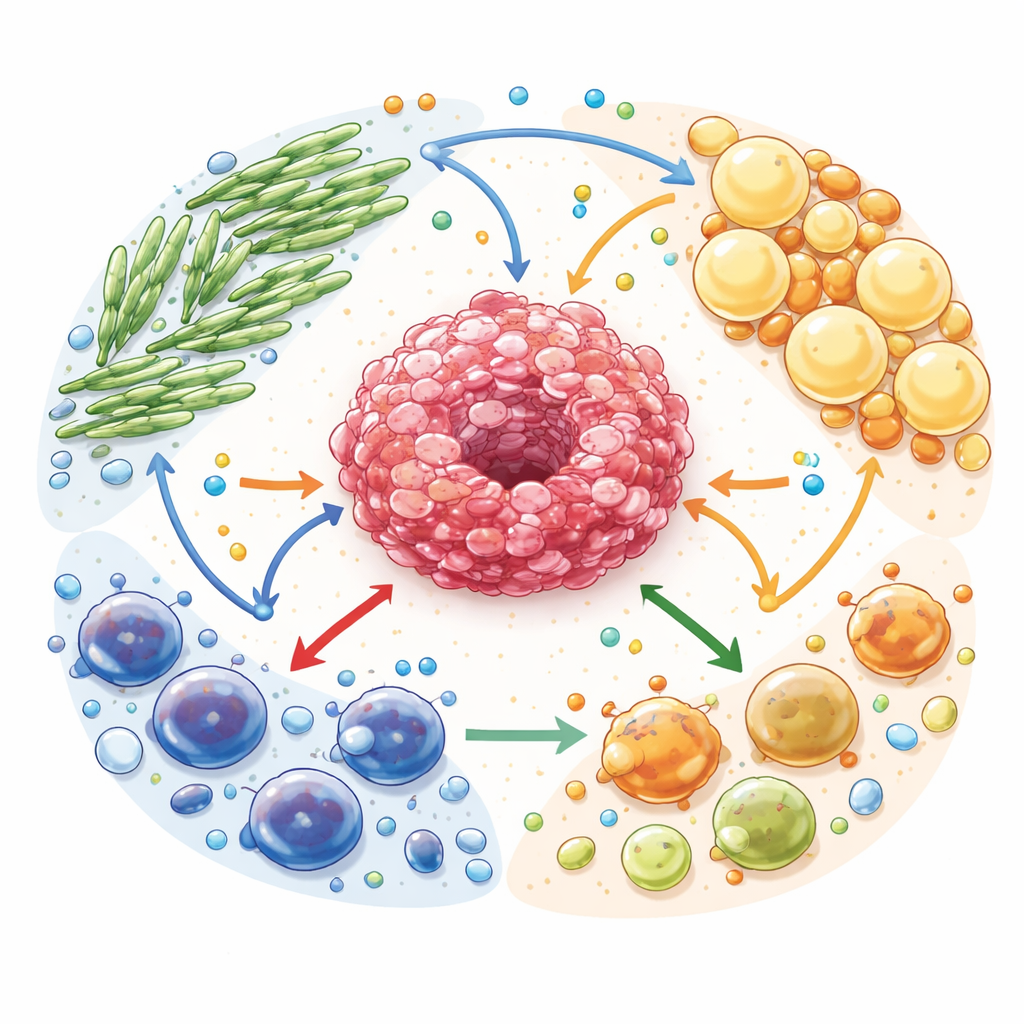
Partage de carburant dans un écosystème tumoral
Les auteurs décrivent le microenvironnement tumoral comme un écosystème complexe. Les cellules cancéreuses sont entourées de fibroblastes associés au cancer (cellules de soutien ressemblant à des cicatrices), d’adipocytes associés au cancer (cellules graisseuses reprogrammées) et de nombreux types de cellules immunitaires. Toutes ces cellules se font concurrence et s’échangent des carburants tels que le glucose, les acides gras et les acides aminés. Mais cet échange n’est pas neutre : les cellules de soutien sont reprogrammées pour mobiliser leurs propres réserves et exporter des molécules riches en énergie qui alimentent les cellules tumorales. Parallèlement, des sous‑produits assimilables à des déchets, notamment le lactate et l’adénosine, s’accumulent et servent de puissants signaux affaiblissant les cellules immunitaires protectrices tout en favorisant celles qui atténuent l’attaque immunitaire.
Comment les adipocytes aident les tumeurs et entravent les défenses
Les dépôts graisseux voisins font bien plus que stocker des calories. Sous l’influence des signaux tumoraux et d’un faible apport en oxygène, les adipocytes ordinaires se transforment en adipocytes associés au cancer. Ils réduisent leurs gouttelettes lipidiques, augmentent la lipolyse et déversent des acides gras libres, des molécules inflammatoires et de petites vésicules chargées de cargo. Les cellules cancéreuses importent avidement ces lipides et les oxydent dans leurs mitochondries, acquérant une source d’énergie flexible et durable qui les aide à survivre au stress, à migrer et à résister aux traitements. Les cellules immunitaires présentes dans les zones riches en lipides s’en sortent moins bien : les lymphocytes T cytotoxiques et les cellules NK s’alourdissent en lipides, subissent un stress oxydatif et sombrent dans un état « d’épuisement » caractérisé par une capacité réduite à détruire les cellules tumorales. En revanche, les lymphocytes T régulateurs et certains myélocytes tirent profit de ces lipides, devenant plus suppressifs et étouffant davantage la réponse immunitaire.
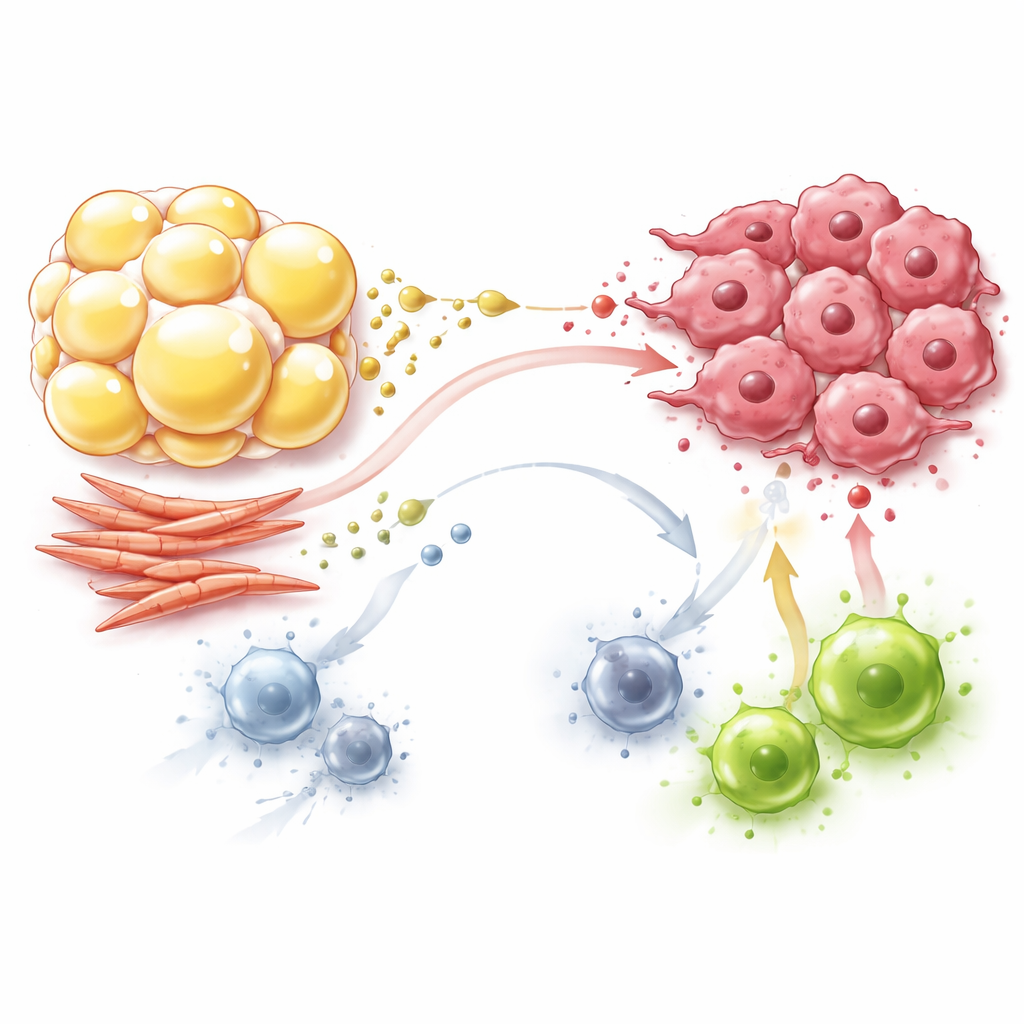
Fibroblastes : des bâtisseurs qui reprogramment aussi le métabolisme
Les fibroblastes, longtemps connus comme les artisans du tissu cicatriciel autour des tumeurs, sont aussi des acteurs actifs de ce drame métabolique. Les fibroblastes associés au cancer basculent vers un comportement très consommateurs de sucre, transformant de grandes quantités de glucose en lactate et en pyruvate même en présence d’oxygène. Ils exportent ces produits dans l’espace environnant, où les cellules tumorales les réutilisent comme carburant pour leurs propres centrales énergétiques, économisant ainsi le glucose pour la croissance. Les fibroblastes synthétisent et échangent aussi des acides aminés tels que la glutamine, la proline et l’asparagine, qui soutiennent à la fois la structure tumorale et sa croissance en situation de stress nutritif. Parallèlement, les fibroblastes consomment des nutriments clés et libèrent du lactate, privant les lymphocytes T effecteurs dépendants du glucose et poussant les macrophages et les lymphocytes T vers des états plus tolérants et moins agressifs.
Cellules immunitaires prises au piège métabolique
Le système immunitaire au sein des tumeurs est façonné autant par la disponibilité des carburants que par les antigènes. Les lymphocytes T cytotoxiques et les cellules NK, qui ont besoin d’une combustion rapide des sucres pour alimenter leur attaque, se retrouvent dans un paysage dépouillé de glucose et inondé de lactate, de lipides et d’autres métabolites suppressifs. Leurs moteurs calment, leurs mitochondries sont endommagées et les « freins » inhibiteurs à leur surface augmentent. Pendant ce temps, les lymphocytes T régulateurs et les macrophages associés à la tumeur sont bien adaptés à cet environnement hostile. Ils favorisent l’oxydation des lipides et le métabolisme oxydatif, ce qui leur permet de prospérer là où d’autres échouent. Soutenues par les fibroblastes et les adipocytes, ces cellules renforcent un état tolérant semblable à la cicatrisation qui protège la tumeur et atténue l’effet des inhibiteurs de points de contrôle et d’autres immunothérapies.
Transformer le métabolisme en cible thérapeutique
La revue met en lumière une boîte à outils grandissante de médicaments expérimentaux conçus pour perturber ce réseau de soutien sans se contenter d’empoisonner les cellules en division. Certaines approches visent à bloquer la libération de lipides par les adipocytes ou la capture et l’oxydation des lipides par les cellules cancéreuses. D’autres ciblent les voies induites par les fibroblastes qui génèrent du lactate, remodelent la matrice ou attirent des myélocytes suppressifs. En réduisant les niveaux de lactate, en bloquant des transporteurs de carburant spécifiques ou en reprogrammant des capteurs lipidiques intracellulaires, ces stratégies cherchent à restaurer l’accès au glucose et la santé mitochondriale des lymphocytes T et des cellules NK épuisés. L’objectif ultime n’est pas seulement d’affamer la tumeur, mais de « rééduquer » son voisinage pour que les cellules immunitaires retrouvent la capacité de repérer, d’atteindre et d’attaquer efficacement les cellules cancéreuses.
Citation: Kim, T.H., Lim, S.H., Lee, H. et al. Metabolic crosstalk among cancer-associated fibroblasts, adipocytes and immune cells as an immunosuppressive tumor microenvironment driver. Exp Mol Med 58, 366–381 (2026). https://doi.org/10.1038/s12276-026-01650-1
Mots-clés: microenvironnement tumoral, métabolisme du cancer, fibroblastes associés au cancer, adipocytes associés au cancer, immunosuppression tumorale