Clear Sky Science · fr
La déficience de la composante du complexe exocyst Exoc5 aggrave la progression de la fibrose rénale
Pourquoi la cicatrisation rénale importe
La maladie rénale chronique touche des centaines de millions de personnes dans le monde, et une des raisons majeures de sa progression est la fibrose — un tissu cicatriciel qui remplace progressivement le tissu rénal fonctionnel. Cette étude explore une machinerie cellulaire peu connue, l’exocyste, et l’un de ses composants appelé Exoc5, pour poser une question concrète : cette protéine aide-t-elle les reins à se réparer proprement après une lésion, ou les pousse-t-elle vers la cicatrisation et l’insuffisance ?
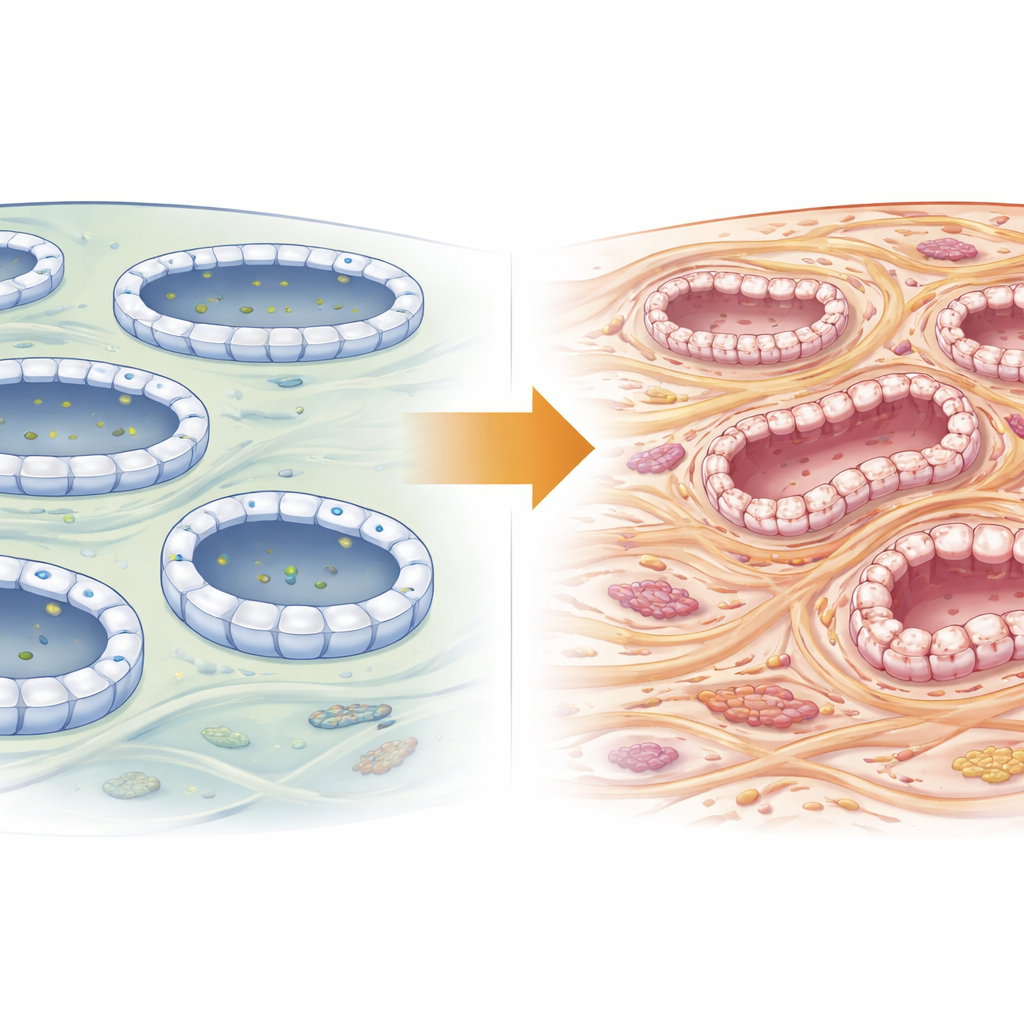
Un centre d’expédition cellulaire dans les cellules tubulaires
Chaque cellule des tubules rénaux est un centre logistique actif, déplaçant en permanence de petites vésicules chargées vers des emplacements précis à la surface cellulaire. Ce trafic est organisé par l’exocyste, un complexe d’amarrage en huit parties. Exoc5 se situe au cœur de cette machinerie, faisant le lien entre le chargement interne et le site d’amarrage à la membrane externe. Des travaux antérieurs ont montré que perturber Exoc5 nuit à divers organes et qu’il aide les cellules des tubules rénaux à maintenir leur structure serrée et ordonnée. Parce que la perte de structure est une caractéristique de la fibrose, les auteurs ont supposé qu’Exoc5 pourrait discrètement décider si les reins endommagés récupèrent ou se cicatrisent.
Tester le rôle d’Exoc5 dans les reins de souris
Les chercheurs ont modifié génétiquement des souris pour supprimer Exoc5 uniquement dans les cellules des tubules proximaux — les segments qui assurent la majeure partie de la filtration et de la réabsorption rénale. De façon surprenante, ces souris se développaient normalement et présentaient une structure rénale, une localisation des transporteurs et une fonction normales en conditions courantes. Pour imiter une lésion localisée et prononcée qui conduit souvent à la fibrose, l’équipe a ensuite ligaturé un uretère, une procédure standard provoquant une accumulation de pression, une inflammation et une fibrose dans le rein affecté sur une semaine. Dans les souris normales et celles déficientes en Exoc5, cette obstruction réduisait les niveaux d’Exoc5, mais les animaux knock-out développaient un rétrécissement tubulaire beaucoup plus sévère, une accumulation de collagène et une invasion accrue de cellules liées à l’inflammation.
Des tubes ordonnés aux cellules migrantes
Les cellules tubulaires saines sont étroitement connectées, avec des faces apicale et basale bien définies. Lors de la fibrose, elles subissent souvent une « transition épithélio-mésenchymateuse » (TEM), un passage d’un état ancré et en feuillet à un état plus mobile et fibreux. Les auteurs ont constaté qu’après l’obstruction, les reins dépourvus d’Exoc5 présentaient une activation plus marquée des principaux moteurs de la TEM et des niveaux plus élevés de protéines typiques de cellules migrantes productrices de fibres, ainsi qu’une perte plus importante des protéines de jonction qui maintiennent normalement la polarité des cellules tubulaires. Ils ont aussi observé la réapparition de Pax2, un régulateur du développement normalement éteint une fois les tubules rénaux matures. Pax2 revenait de manière plus prononcée dans les tubules déficients en Exoc5, en particulier dans les cellules stressées qui ne se divisaient pas avec succès, ce qui suggère que la perte d’Exoc5 pousse les cellules vers un état partiellement réparé et dédifférencié, prédisposé à la cicatrisation.
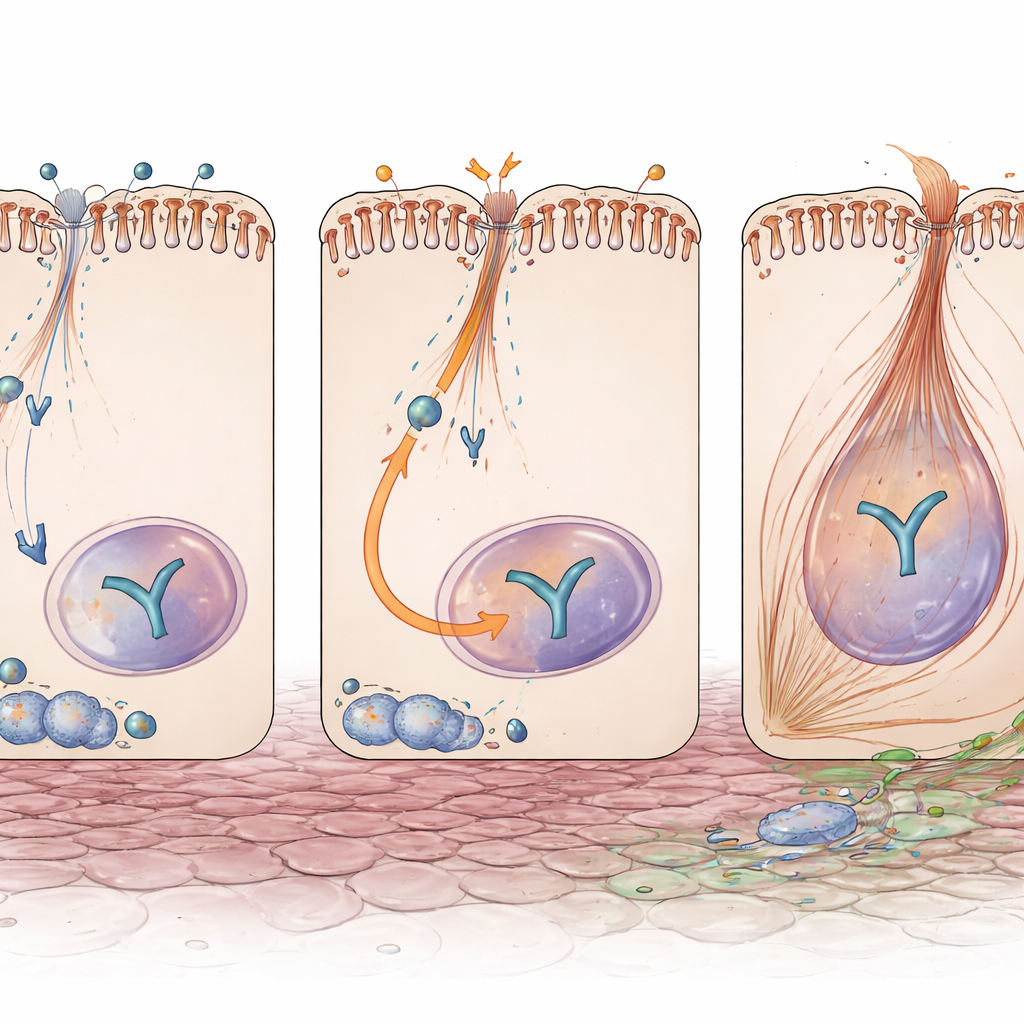
Un commutateur reliant la lésion aux signaux de cicatrisation
Un autre acteur central de la fibrose est YAP, une protéine sensible aux signaux qui migre vers le noyau pour activer des gènes liés à la croissance et à la production de matrice. Même sans lésion, les tubules privés d’Exoc5 présentaient des niveaux protéiques de YAP plus élevés. Après obstruction, YAP était davantage activé et concentré dans les noyaux cellulaires de ces reins, et ses produits en aval — des molécules connues pour piloter le remodelage fibrotique — étaient augmentés. Important : cela ne résultait pas d’une augmentation de l’activité du gène YAP, ce qui implique qu’Exoc5 limite normalement YAP au niveau protéique ou de son trafic. Dans des cellules tubulaires rénales humaines cultivées, réduire EXOC5 par interférence ARN augmentait YAP et Pax2, et rendait les cellules plus sensibles au signal pro-fibrotique TGF-β, avec des changements de type TEM plus marqués et davantage de cellules acquérant des fibres contractiles typiques des myofibroblastes.
Ce que cela implique pour les traitements futurs
Pris ensemble, les résultats dépeignent Exoc5 comme un gardien discret : sous stress, il aide les cellules tubulaires à conserver leur identité organisée et maintient en échec des signaux pro-cicatrisation comme YAP et Pax2. Quand les niveaux d’Exoc5 chutent — que ce soit par perte génétique ou suite à une lésion — les cellules tubulaires perdent plus facilement leur polarité, glissent vers un état proche du développement et alimentent le processus fibrotique. Parce que la suppression d’Exoc5 dans les tubules proximaux n’endommageait pas les reins sains mais aggravait nettement la cicatrisation après lésion, ces travaux désignent Exoc5 et ses partenaires de signalisation comme des cibles prometteuses pour des thérapies visant à ralentir ou inverser la fibrose rénale avant qu’elle n’évolue vers l’insuffisance rénale.
Citation: Lim, H.J., Han, Y.K., Noh, M.R. et al. Deficiency of exocyst complex component Exoc5 exacerbates the progression of kidney fibrosis. Exp Mol Med 58, 681–695 (2026). https://doi.org/10.1038/s12276-026-01649-8
Mots-clés: fibrose rénale, Exoc5, transition épithélio-mésenchymateuse, signalisation YAP, maladie rénale chronique