Clear Sky Science · fr
La supplémentation en L-aspartate corrige la MASLD et la MASH chez la souris en inhibant la fragmentation mitochondriale médiée par l’interaction plaquette–hépatocyte via l’axe ATP–P2X7–NEK7–DRP1
Pourquoi cette étude du foie est importante
Beaucoup de personnes accumulent des graisses dans le foie sans le savoir. Ce problème silencieux, désormais appelé stéatose hépatique associée à un dysfonctionnement métabolique (MASLD), peut évoluer vers une inflammation sévère, une fibrose et même un cancer du foie. L’article résumé ici examine si un acide aminé naturel simple, le L‑aspartate, peut protéger le foie chez la souris et révèle un coupable inattendu des lésions hépatiques : des plaquettes sanguines hyperactives qui endommagent les « centrales énergétiques » des cellules hépatiques, les mitochondries.
Un problème hépatique courant dans la vie moderne
La MASLD est étroitement liée à l’obésité et au diabète de type 2 et pourrait bientôt toucher plus d’un tiers de la population mondiale. Dans la MASLD, les hépatocytes se remplissent de graisses, s’oxydent et commencent à mourir, ce qui déclenche inflammation et formation de cicatrices. Les mitochondries saines brûlent normalement les graisses et les sucres pour produire de l’énergie, mais dans cette maladie elles sont endommagées et fragmentées, si bien que le foie brûle moins de graisses et en accumule davantage. Malgré l’ampleur du problème, un seul médicament a été approuvé jusqu’à présent et n’aide qu’une fraction des patients, si bien que les chercheurs cherchent des traitements sûrs et abordables qui restaurent la machinerie énergétique du foie.
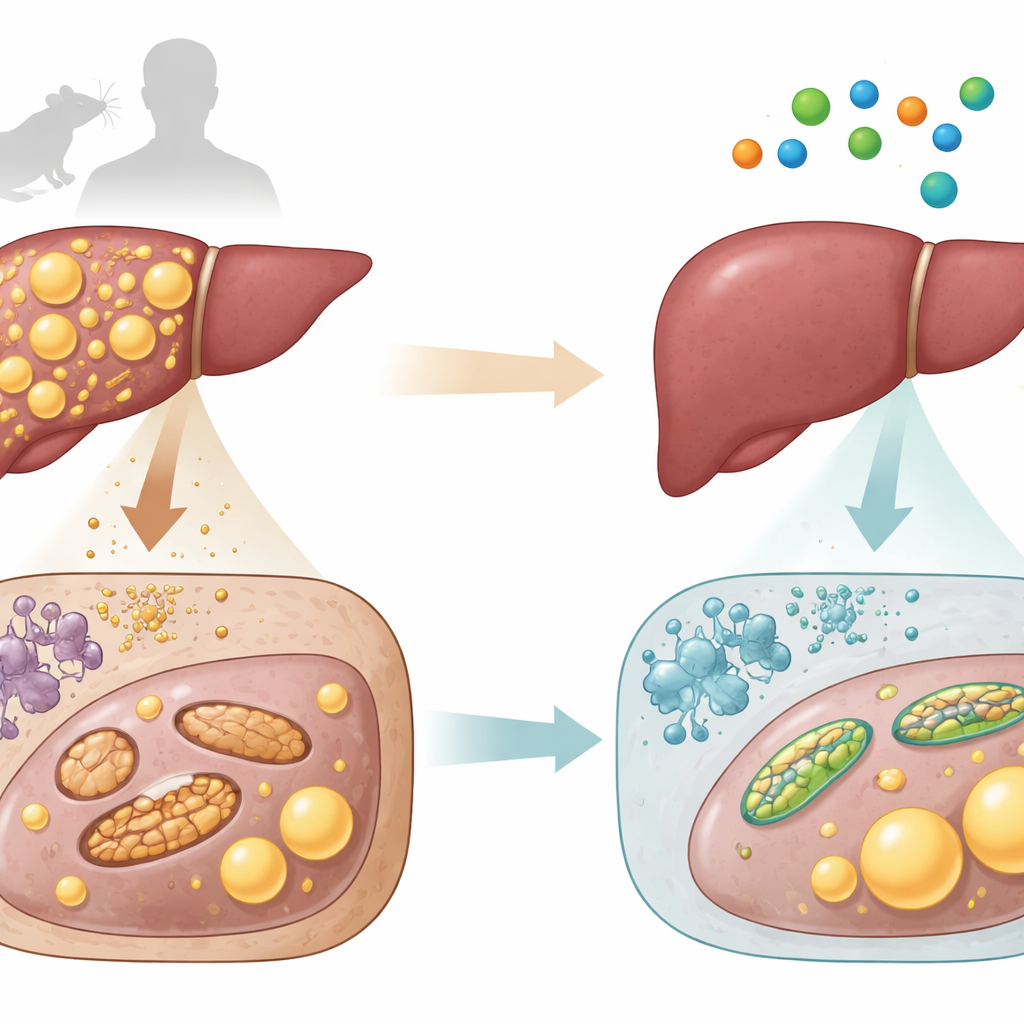
Un acide aminé simple comme aide potentielle
Le L‑aspartate est un petit élément constitutif des protéines qui participe aussi aux cycles énergétiques de l’organisme et est déjà utilisé cliniquement comme composé de soutien hépatique. Les chercheurs ont d’abord mesuré le L‑aspartate dans des échantillons de sang et de foie de souris et d’humains. Ils ont constaté que les animaux et les patients humains présentant des foies plus gras et plus endommagés avaient systématiquement des niveaux plus faibles de L‑aspartate dans leur tissu hépatique. Dans les deux espèces, moins il y avait de L‑aspartate, plus la teneur en graisse était élevée et plus les signes de lésion hépatique étaient marqués. Ce schéma suggérait qu’une baisse du L‑aspartate pouvait aller de pair avec une détérioration de la santé hépatique.
Renverser la stéatose et l’inflammation chez la souris
L’équipe a ensuite exploré si la réintroduction de L‑aspartate pouvait réellement réparer la maladie. Ils ont nourri des souris avec un régime riche en graisses et en cholestérol ou avec un régime spécial provoquant une inflammation et une fibrose hépatiques sévères, reproduisant la MASLD humaine et sa forme avancée, la MASH. Lorsque ces souris ont reçu des injections de L‑aspartate à des doses comparables à celles utilisées en clinique, leurs foies sont devenus plus clairs et moins gras, les enzymes hépatiques dans le sang ont diminué, et les examens microscopiques ont montré moins de gouttelettes lipidiques, moins d’inflammation et une réduction de la fibrose. Ces bénéfices sont apparus à la fois dans la stéatose précoce et dans la maladie inflammatoire avancée et étaient comparables à ceux des médicaments de référence établis dans les mêmes modèles.
Protéger les centrales énergétiques de la cellule
En observant l’intérieur du foie, les scientifiques ont noté que les souris malades avaient moins de mitochondries, dont beaucoup étaient agrandies et endommagées ou fragmentées en petits éléments. Le traitement par L‑aspartate a rétabli un réseau mitochondrial plus sain et allongé. Il a renforcé l’activité des complexes enzymatiques clés de production d’énergie, augmenté l’utilisation de l’oxygène par les mitochondries et la production d’ATP, et accru les marqueurs de « nettoyage » et de renouvellement mitochondriaux. Des mesures réalisées sur l’animal entier ont montré une consommation d’oxygène et une dépense énergétique plus élevées, indiquant que les souris brûlaient plus de carburant globalement plutôt que de simplement manger moins.
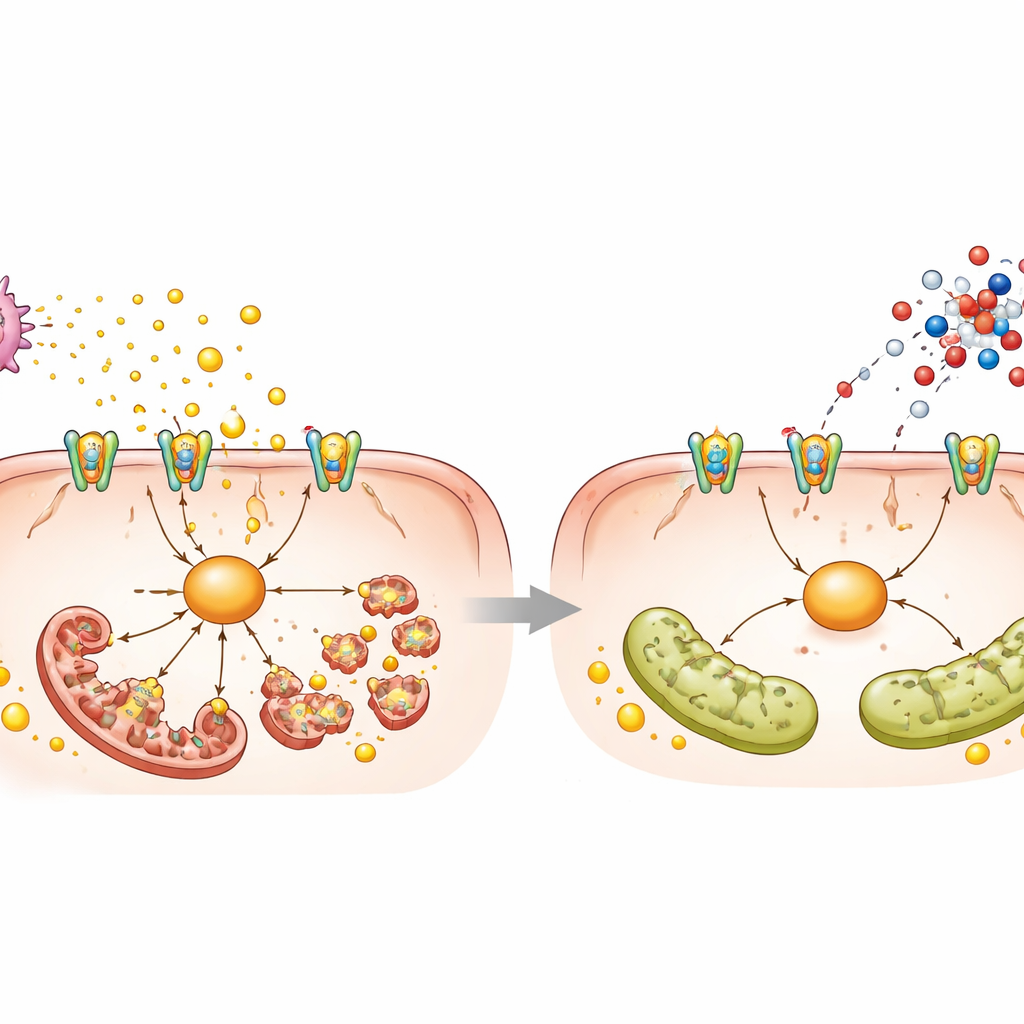
Plaquettes, signal toxique et chaîne moléculaire
Pour comprendre comment le L‑aspartate produit ces effets, les chercheurs ont combiné l’analyse de l’activité génique et du métabolisme après une seule dose. Un signal inattendu est apparu : des voies liées à l’activation plaquettaire et à une molécule messagère appelée GMPc. Dans la stéatose, les plaquettes dans le sang et le foie étaient plus nombreuses et activées, et elles libéraient un surplus d’ATP, une molécule énergétique normale qui devient nocive lorsqu’elle est déversée à l’extérieur des cellules. Cet ATP activait un récepteur appelé P2X7 sur les cellules hépatiques, qui à son tour activait une protéine nommée NEK7 et la protéine de fission DRP1, entraînant la fragmentation des mitochondries et favorisant l’accumulation lipidique et la mort cellulaire. Le L‑aspartate augmentait les niveaux de GMPc à l’intérieur des plaquettes, atténuait leur activation et leur agrégation, réduisait la libération d’ATP et calmait cette chaîne P2X7–NEK7–DRP1 au sein des cellules hépatiques. Le blocage direct des plaquettes par l’aspirine, l’inhibition de P2X7 ou l’extinction de NEK7 reproduisaient bon nombre des effets protecteurs du L‑aspartate, soutenant l’idée que la communication plaquettes–foie est centrale dans le dommage.
Ce que cela pourrait signifier pour les patients
Ensemble, ces résultats suggèrent que, dans la maladie du foie gras, des plaquettes hyperactives arrosent le foie d’ATP, ce qui déclenche une cascade moléculaire qui brise les mitochondries et aggrave l’accumulation de graisses et les lésions. Chez la souris, la supplémentation en L‑aspartate rompt cette boucle : elle maintient les plaquettes plus calmes, limite la libération d’ATP, préserve la forme et la fonction mitochondriales et inverse à la fois la stéatose simple et la maladie inflammatoire et fibrotique. Parce que le L‑aspartate est peu coûteux et déjà utilisé comme agent de soutien hépatique, ces travaux le mettent en avant comme un candidat prometteur à tester chez l’humain pour la MASLD et la MASH, tout en identifiant les dommages mitochondriaux induits par les plaquettes comme une nouvelle cible pour de futures thérapies.
Citation: Cao, WJ., Su, R., Fu, HL. et al. Supplementation of L-aspartate corrects MASLD and MASH in mice by inhibiting platelet–hepatocyte interaction-mediated mitochondrial fragmentation via the ATP–P2X7–NEK7–DRP1 axis. Exp Mol Med 58, 533–547 (2026). https://doi.org/10.1038/s12276-026-01648-9
Mots-clés: maladie du foie gras, plaquettes, mitochondries, L-aspartate, maladie hépatique métabolique