Clear Sky Science · fr
Progression de la sclérose en plaques associée aux microglies : identification de cibles et engagement thérapeutique dans des modèles humains in vitro
Pourquoi les cellules immunitaires cérébrales comptent dans la sclérose en plaques
La sclérose en plaques (SEP) est souvent décrite comme une maladie où le système immunitaire attaque le cerveau et la moelle épinière. De nombreux médicaments actuels réduisent efficacement les poussées aiguës, ou rechutes, mais n’empêchent pas la détérioration lente et silencieuse que beaucoup de patients subissent sur des années. Cette revue explique comment de petites cellules immunitaires résidant en permanence dans le cerveau, appelées microglies, peuvent conduire ce déclin à long terme — et comment de nouveaux modèles cérébraux humains cultivés en laboratoire aident les scientifiques à trouver des traitements capables enfin de ralentir ou d’arrêter la progression.
Le moteur caché des dommages continus
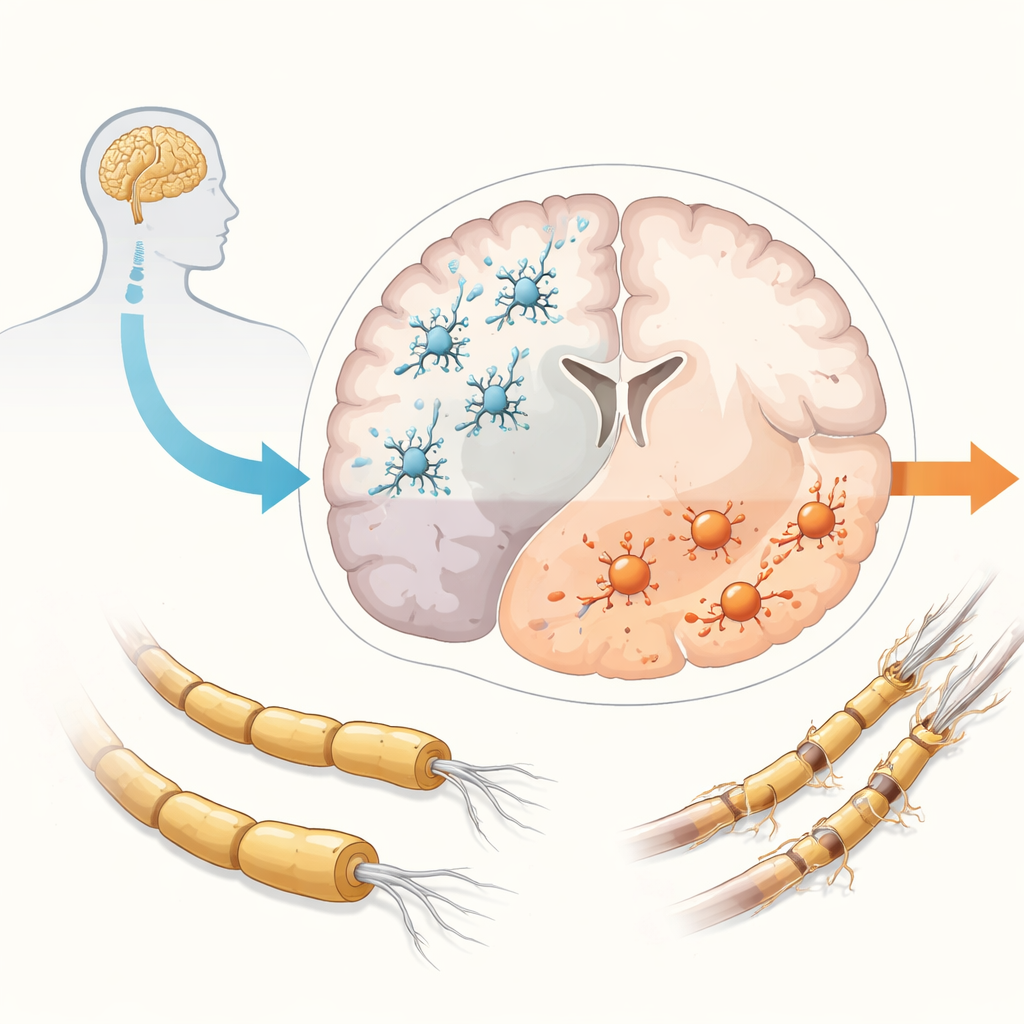
La SEP a traditionnellement été divisée en formes rémittentes et progressives, mais les données montrent aujourd’hui que la progression commence très tôt chez presque tous les malades, même lorsqu’ils semblent n’avoir que des rechutes. Alors que les rechutes sont alimentées par des cellules immunitaires venant du sang, la progression semble être portée par une inflammation piégée à l’intérieur du cerveau et de la moelle épinière. Dans cet environnement clos, les microglies participent à de nombreux processus nuisibles : inflammation continue, perte de la gaine isolante de myéline des fibres nerveuses dans la substance blanche et grise, accumulation de composés oxydants délétères et échec des mécanismes de réparation. Le résultat final est la perte progressive des neurones et de leurs connexions. Les microglies contribuent normalement à la santé cérébrale en éliminant les débris et en soutenant les neurones, mais dans la SEP elles basculent souvent vers des états plus agressifs et perdent certaines de leurs fonctions protectrices, faisant d’elles des suspectes majeures dans la progression.
Pourquoi les modèles animaux traditionnels sont insuffisants
Pendant des décennies, les études chez la souris et d’autres animaux ont été cruciales pour développer des médicaments limitant les rechutes, mais elles ont en grande partie échoué à produire des thérapies qui arrêtent la progression. Une raison est que les modèles animaux ne reproduisent qu’en partie la SEP humaine et ne recréent pas pleinement l’inflammation complexe et durable observée dans le cerveau des patients. Les microglies de rongeurs diffèrent aussi des microglies humaines sur des gènes et des réponses importants. En conséquence, des traitements prometteurs chez l’animal ne fonctionnent souvent pas chez l’homme. Le manque de modèles animaux capturant réellement la SEP progressive a poussé les chercheurs à développer de nouveaux systèmes humains en laboratoire, où ils peuvent étudier plus directement les microglies et d’autres cellules cérébrales.
Construire des modèles cérébraux humains en laboratoire
Les scientifiques utilisent aujourd’hui plusieurs niveaux de modèles in vitro pour étudier les microglies humaines. Les cellules primaires prélevées directement dans le tissu cérébral de rongeurs ou d’humains conservent de nombreuses caractéristiques naturelles mais sont difficiles à obtenir, se modifient rapidement hors de leur environnement d’origine et ne se prêtent pas facilement à une production à grande échelle. Pour surmonter ces obstacles, les chercheurs recourent aux cellules souches pluripotentes induites (iPS) — des cellules adultes reprogrammées en un état souple proche de celui des cellules souches. Ces cellules iPS peuvent être dirigées pour devenir des microglies, des neurones ou d’autres cellules cérébrales. Dans des cultures simples en monocouche, les microglies dérivées d’iPS captent de nombreux traits clés et peuvent être produites en grand nombre, permettant des expériences détaillées et des criblages médicamenteux. Elles peuvent même être générées à partir de patients individuels atteints de SEP, révélant des différences intrinsèques comme une activité génique altérée et des modifications de leur réponse au stress et d’élimination des débris.
Ajouter des environnements cérébraux réalistes
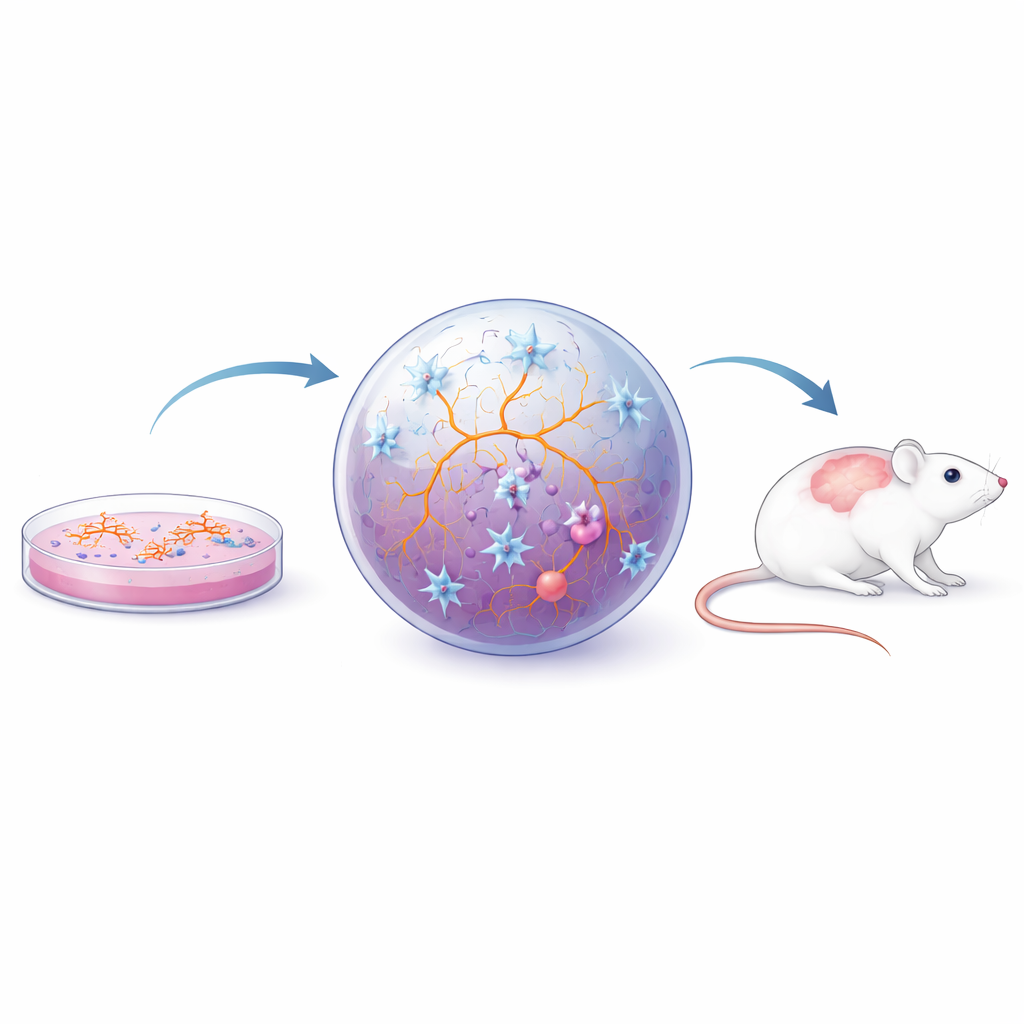
Parce que le comportement des microglies est fortement modelé par leur environnement, les chercheurs ont dépassé les couches cellulaires uniques pour des configurations plus réalistes. Dans les cocultures bidimensionnelles, les microglies croissent avec des neurones et des cellules de soutien, ce qui les aide à adopter des formes et des comportements plus naturels et permet d’étudier comment les types cellulaires s’influencent mutuellement. Les sphéroïdes et organoïdes tridimensionnels — de petits fragments auto-organisés de tissu ressemblant au cerveau — vont plus loin, offrant un milieu souple et dense qui ressemble davantage au tissu cérébral réel. Lorsqu’elles sont intégrées dans ces structures, les microglies présentent des morphologies ramifiées complexes, réagissent aux blessures, interagissent avec une couche semblable à la barrière hémato-encéphalique et répondent à des signaux inflammatoires présents dans le liquide céphalo-rachidien de personnes atteintes de SEP. De tels modèles ont servi à étudier comment une inflammation chronique déclenche un état « fatigué mais inflammé » appelé sénescence cellulaire chez les microglies et les astrocytes, et comment des altérations du métabolisme lipidique microglial peuvent gêner la réparation de la myéline. Parallèlement, la transplantation de microglies humaines dérivées d’iPS ou d’organoïdes dans le cerveau de souris permet à ces cellules de maturer davantage au sein d’un réseau vivant et d’être testées dans des modèles de maladie de type SEP établis.
Des modèles de laboratoire aux traitements futurs
Ensemble, ces modèles humains in vitro et chimériques forment une boîte à outils pour disséquer comment les microglies contribuent à la progression de la SEP et pour tester de nouveaux traitements visant à calmer l’activité microgliale nocive tout en restaurant leurs fonctions protectrices. Bien qu’aucun de ces modèles ne reproduise entièrement le cerveau humain, chacun capture différentes pièces du puzzle, et ensemble ils comblent le fossé entre des cultures cellulaires simples et des modèles animaux imparfaits. En combinant les enseignements tirés de ces systèmes, les chercheurs espèrent identifier des cibles médicamenteuses précises — comme des voies contrôlant l’inflammation, des changements apparentés au vieillissement et le métabolisme des lipides dans les microglies — qui pourraient enfin se traduire par des traitements ralentissant ou arrêtant le handicap progressif caractéristique de la SEP.
Citation: Blenkle, A., Geladaris, A. & Weber, M.S. Microglia-associated progression of multiple sclerosis: target identification and therapeutic engagement in human in vitro models. Exp Mol Med 58, 357–365 (2026). https://doi.org/10.1038/s12276-026-01647-w
Mots-clés: progression de la sclérose en plaques, microglies, cellules souches pluripotentes induites, organoïdes cérébraux, neuroinflammation