Clear Sky Science · fr
Une boucle de rétroaction positive ESRP1/circPHGDH/miR-149/RAP1B favorise les comportements malins et la glycolyse des cellules du cancer de la prostate
Pourquoi cette recherche est importante pour la santé des hommes
Le cancer de la prostate est l’un des cancers les plus fréquents chez l’homme, et de nombreuses tumeurs deviennent finalement agressives et résistantes aux traitements. Cette étude révèle un circuit de contrôle caché à l’intérieur des cellules prostatiques cancéreuses qui les aide à croître plus rapidement, à se disséminer plus facilement et à réorganiser la façon dont elles brûlent le glucose pour produire de l’énergie. En cartographiant cette boucle moléculaire, les chercheurs mettent en lumière de nouvelles vulnérabilités susceptibles d’être ciblées pour ralentir la maladie ou rendre les thérapies existantes plus efficaces.
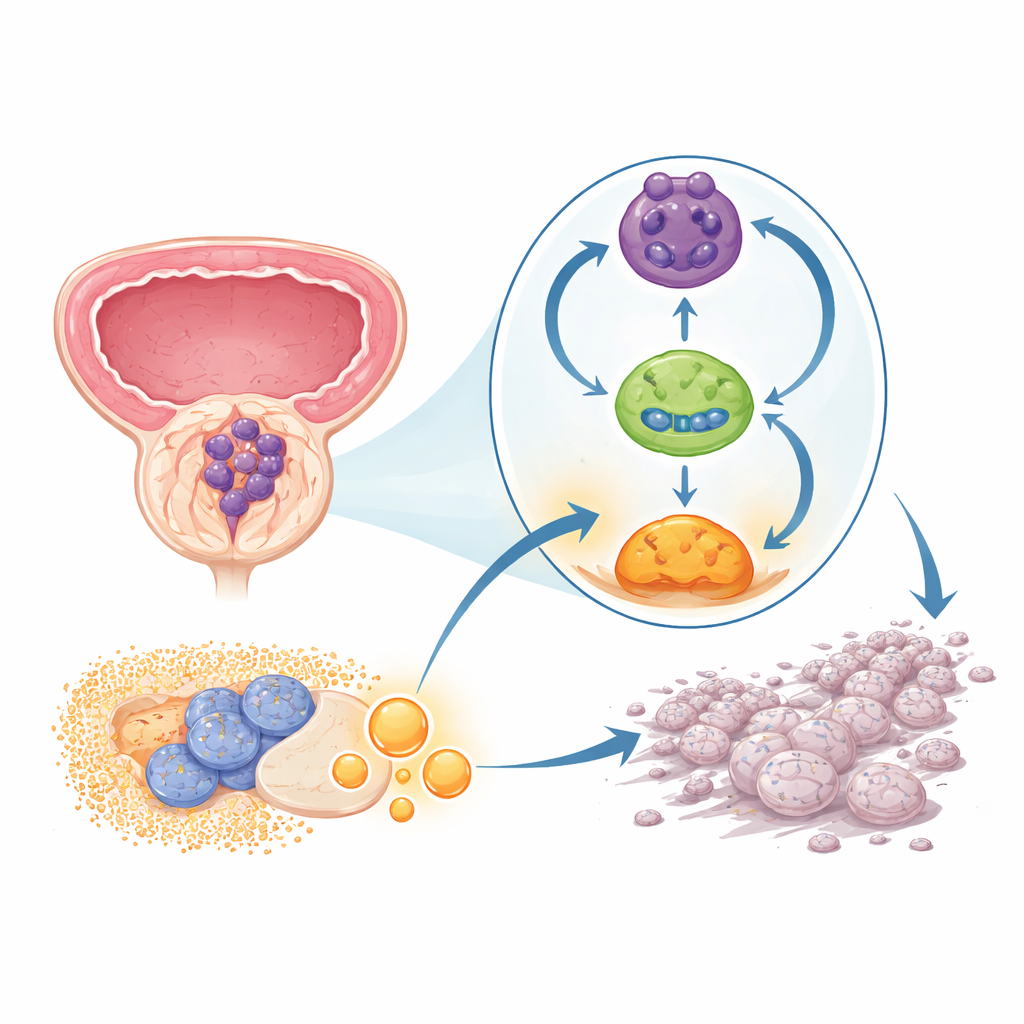
Une boucle cachée qui maintient le cancer activé
L’équipe s’est concentrée sur une classe de molécules génétiques récemment étudiée : les ARN circulaires. À la différence des brins linéaires habituels, ces molécules forment des anneaux fermés et sont remarquablement stables. Dans des échantillons de tumeurs prostatiques et des lignées cellulaires, les chercheurs ont trouvé qu’un ARN circulaire particulier, nommé circPHGDH, était systématiquement plus abondant que dans les tissus non cancéreux voisins. Les patients dont les tumeurs présentaient des niveaux plus élevés de cet ARN avaient tendance à avoir des tumeurs plus volumineuses, une extension locale plus avancée et des métastases, suggérant que circPHGDH contribue à une forme plus dangereuse de la maladie.
Comment les cellules cancéreuses modifient leur comportement
Pour déterminer ce que fait réellement circPHGDH, les scientifiques ont modifié ses niveaux dans des cellules de cancer de la prostate cultivées en laboratoire. Lorsqu’ils ont réduit circPHGDH, les cellules formaient moins de colonies, se déplaçaient et envahissaient les membranes moins efficacement, et présentaient des caractéristiques conservant un état plus « épithélial », moins enclin à la dissémination. Parallèlement, les cellules se sont éloignées d’un profil métabolique avide de glucose, typique de nombreuses tumeurs : leur dépendance à la glycolyse a diminué et elles ont davantage utilisé la production d’énergie dépendante de l’oxygène. Lorsque circPHGDH a été augmenté, tous ces traits favorisant le cancer ont évolué en sens inverse.
Petits ARN et relais du signal de croissance
L’étude a ensuite retracé la manière dont circPHGDH exerce ces effets. Dans le cytoplasme, circPHGDH agit comme une éponge pour un petit ARN régulateur appelé miR-149, le captant et l’empêchant de freiner ses cibles habituelles. Une cible clé est RAP1B, une protéine de signalisation qui alimente une voie majeure de croissance et de survie connue pour son rôle dans le cancer de la prostate. Lorsque miR-149 est neutralisé par circPHGDH, les niveaux de RAP1B augmentent et activent des signaux en aval qui favorisent la division cellulaire, la migration et un métabolisme axé sur la glycolyse. Restaurer miR-149 ou réduire directement RAP1B a inversé bon nombre de ces effets délétères, tant en cultures cellulaires que chez des souris porteuses de tumeurs prostatiques humaines.
Un déchet métabolique qui alimente le feu
Un autre niveau de l’histoire concerne la production même de circPHGDH. Sa formation dépend d’une protéine d’épissage nommée ESRP1, qui influence la manière dont les pré-ARN sont coupés et rejoins. Les chercheurs ont montré qu’ESRP1 se lie à des sites spécifiques autour de la région de circPHGDH et favorise sa forme circulaire plutôt que la version linéaire standard. Fait crucial, ils ont découvert que le lactate — produit terminal de la glycolyse — modifie chimiquement ESRP1 à un site unique, rendant la protéine plus stable. Parce que circPHGDH pousse lui-même les cellules vers une glycolyse accrue et donc une production de lactate plus importante, cela crée une boucle autorenforçante : ESRP1 augmente circPHGDH, circPHGDH stimule RAP1B et la glycolyse, la glycolyse génère du lactate, et le lactate stabilise ESRP1.
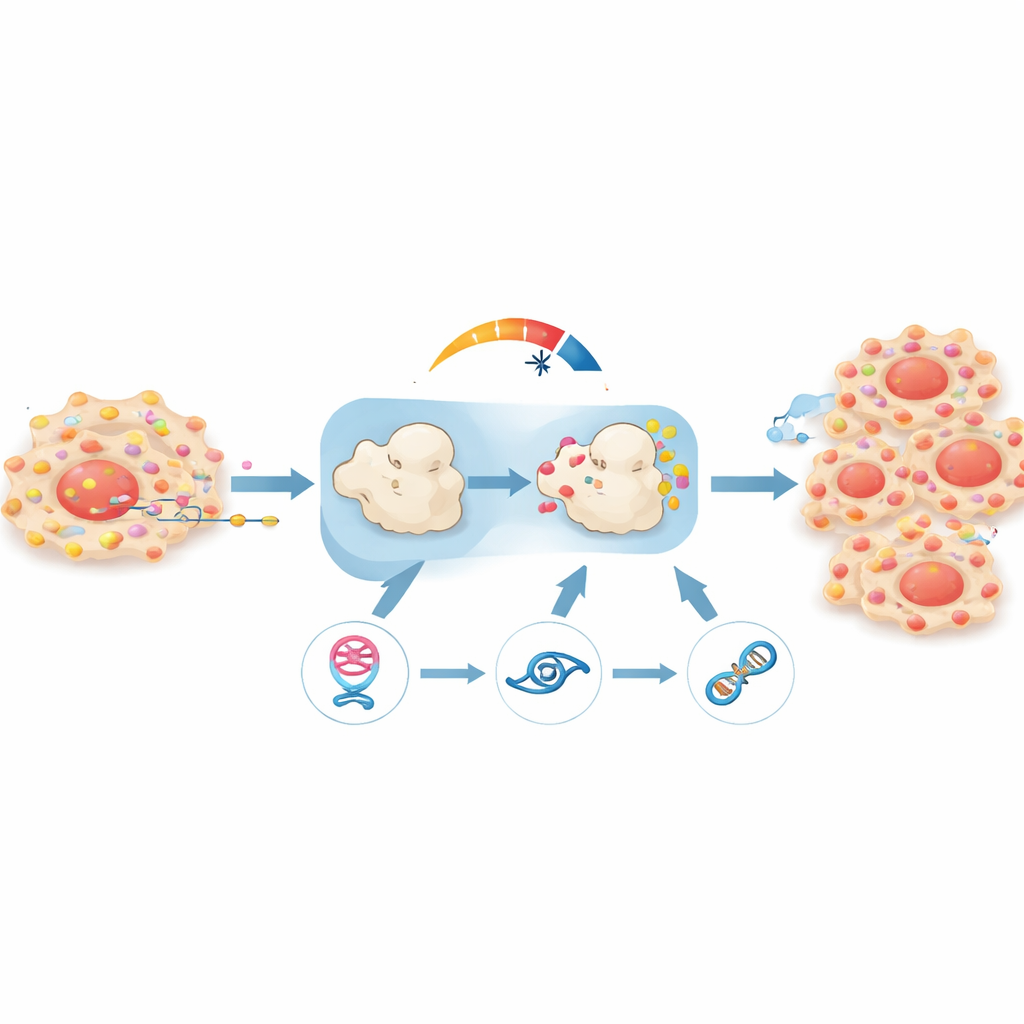
Preuves issues de modèles animaux
Pour vérifier si cette boucle est réellement pertinente in vivo, l’équipe a implanté des cellules de cancer de la prostate humain dans des souris. Les tumeurs dans lesquelles circPHGDH avait été inhibé croissaient plus lentement, pesaient moins et montraient moins de signes de dissémination, comme mesuré par imagerie corporelle et analyses tissulaires. Les marqueurs de prolifération cellulaire étaient plus faibles, et la structure tumorale apparaissait moins agressive au microscope. Lorsque les chercheurs ont soit bloqué miR-149, soit rétabli RAP1B dans ces mêmes tumeurs, une grande partie de la croissance et de la dissémination est revenue, confirmant que la chaîne circPHGDH–miR-149–RAP1B est un moteur central du comportement de la maladie.
Ce que cela implique pour les traitements futurs
Ensemble, ces résultats révèlent une boucle de rétroaction positive dans laquelle une protéine d’épissage, un ARN circulaire, un petit ARN régulateur et une protéine de signalisation coopèrent pour pousser les cellules du cancer de la prostate vers une croissance rapide, l’invasion et un métabolisme avide de sucre. Pour un public non spécialiste, le message clé est que les cellules cancéreuses peuvent câbler leurs contrôles génétiques et métaboliques en circuits auto-renforçants qui maintiennent la progression de la maladie. Rompre cette boucle — en perturbant circPHGDH, en restaurant miR-149, en bloquant RAP1B ou en interférant avec la modification dépendante du lactate d’ESRP1 — offre plusieurs pistes prometteuses pour de futurs médicaments visant à ralentir ou arrêter les formes agressives du cancer de la prostate.
Citation: Wang, X., Yu, L., Qian, X. et al. A ESRP1/circPHGDH/miR-149/RAP1B positive feedback loop promotes the malignant behaviors and glycolysis of prostate cancer cell. Exp Mol Med 58, 622–635 (2026). https://doi.org/10.1038/s12276-026-01646-x
Mots-clés: cancer de la prostate, ARN circulaire, métabolisme tumoral, microARN, voies de signalisation