Clear Sky Science · fr
PAK4 dans les maladies métaboliques : régulation par les signaux nutritifs et implications thérapeutiques
Pourquoi un interrupteur cellulaire compte pour la santé quotidienne
L’obésité, le diabète de type 2 et la stéatose hépatique sont souvent imputés aux calories, mais au cœur de nos cellules, des commutateurs moléculaires décident si nous brûlons ou stockons l’énergie. Cette revue se concentre sur l’un de ces commutateurs, une protéine appelée PAK4, et explique comment elle répond aux variations des signaux nutritifs et hormonaux, remodelant le métabolisme dans le tissu adipeux, le foie et le muscle. Comprendre ce système de contrôle caché pourrait ouvrir la voie à de nouveaux traitements visant plusieurs maladies métaboliques à la fois plutôt que d’agir sur un symptôme isolé. 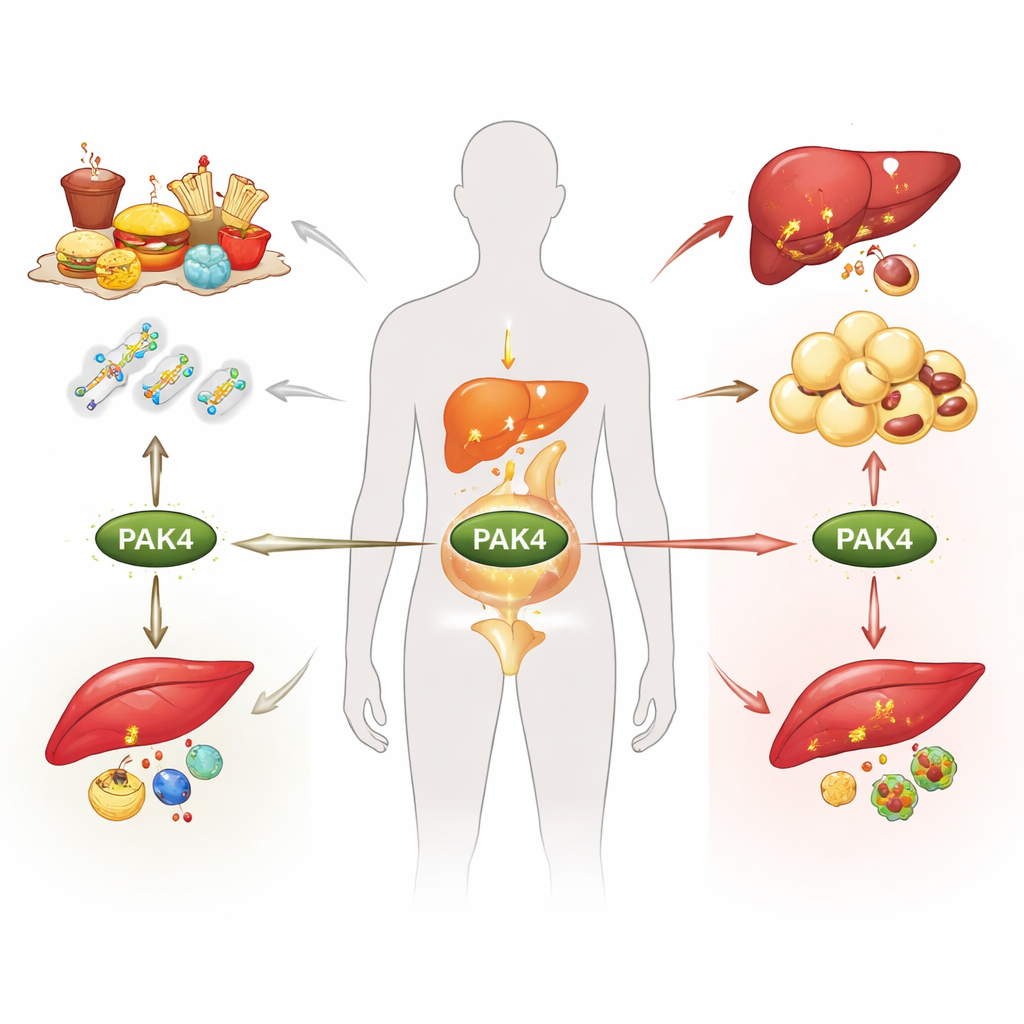
Un interrupteur maître caché dans nos cellules
PAK4 appartient à une famille d’enzymes qui relaient les signaux de petits « messagers » moléculaires à l’intérieur des cellules. En conditions saines, PAK4 est présent à de faibles niveaux dans les principaux organes métaboliques. Lorsque l’équilibre énergétique est perturbé, comme dans l’obésité ou le diabète de type 2, ses niveaux augmentent dans le tissu adipeux, le foie et le muscle squelettique. L’activité de PAK4 est contrôlée de plusieurs façons : par des messagers en amont qui modifient sa conformation, et par des marques chimiques ajoutées ou retirées après la synthèse de la protéine. Celles-ci incluent des groupements phosphate qui peuvent soit activer PAK4, soit le marquer pour destruction, ainsi que d’autres modifications qui influencent sa stabilité ou son activité. Le jeûne, l’alimentation, les hormones et le stress modulent toutes ces marques, de sorte que PAK4 « sense » l’état nutritionnel de l’organisme et transmet cette information aux principales voies métaboliques.
Comment PAK4 incline les adipocytes vers le stockage
Dans les cellules adipeuses, PAK4 joue un rôle d’essieu freinant la lipolyse. Normalement, lors du jeûne ou en cas d’élévation des hormones de stress, une autre enzyme, la PKA, déclenche la dégradation contrôlée des graisses stockées dans de petites gouttelettes. La revue décrit comment PAK4 contrecarre ce processus en ajoutant des phosphates inhibiteurs directement sur la lipase sensible aux hormones et sur une protéine liant les acides gras qui aide au transport des molécules lipidiques. Ces modifications affaiblissent la machinerie responsable de la libération des graisses. PAK4 favorise aussi la formation de nouveaux adipocytes plus tôt dans la vie en aidant des protéines du cycle cellulaire à pousser les cellules précurseurs vers un destin d’adipocytes matures. Lorsque PAK4 est supprimé ou bloqué dans des modèles animaux, les adipocytes brûlent davantage de carburant, présentent des caractéristiques de « brunification » qui augmentent la dépense énergétique, et les animaux sont protégés contre la prise de poids induite par l’alimentation. 
Rôle de PAK4 dans la stéatose hépatique et la gestion du glucose musculaire
Dans le foie, PAK4 favorise lui aussi le stockage plutôt que la combustion. Pendant le jeûne ou lors d’un régime cétogène, les niveaux de PAK4 diminuent, permettant aux hépatocytes d’accroître la lipolyse et la production de corps cétoniques, qui alimentent d’autres tissus et peuvent même freiner la croissance tumorale. Lorsque PAK4 est abondant, il ajoute des phosphates à un corépresseur nucléaire qui vient alors réprimer PPARα, le régulateur maître de l’oxydation des graisses et de la formation des cétones. Le résultat est une accumulation de lipides dans le foie et une moindre présence de cétones protectrices dans la circulation. Dans le muscle squelettique, PAK4 interfère avec l’AMPK, un senseur énergétique central qui favorise à la fois l’absorption de glucose et l’activité mitochondriale. En modifiant l’AMPK de façon à empêcher son activation, PAK4 réduit la quantité de transporteurs de glucose à la surface des myocytes et contribue à la résistance à l’insuline. La perte spécifique de PAK4 dans le muscle chez la souris inverse ces effets, améliorant le contrôle glycémique même en situation d’obésité.
Stress, protection et liens avec d’autres interrupteurs cellulaires
La revue souligne aussi l’impact de PAK4 au-delà du métabolisme courant. Lors d’épisodes de diminution du flux sanguin suivis d’une reperfusion dans des organes comme le foie, PAK4 affaiblit les défenses antioxydantes en marquant et en déstabilisant Nrf2, un protecteur clé contre le stress oxydatif. Parallèlement, un membre apparenté, PAK1, joue souvent des rôles plus protecteurs dans le muscle cardiaque, le muscle squelettique et les cellules sécrétrices d’insuline du pancréas, contribuant au maintien d’une régulation normale du glucose. Ce contraste entre une signalisation PAK4 délétère dans les maladies métaboliques et les actions généralement bénéfiques de PAK1 souligne le besoin de médicaments hautement sélectifs visant à éteindre PAK4 sans perturber des protéines apparentées essentielles pour la santé cardiaque et endocrinienne.
Transformer une découverte en traitement
Parce que PAK4 est hyperactif dans le cancer et dans les troubles métaboliques, les concepteurs de médicaments ont développé des petites molécules qui bloquent son activité, ainsi que des « dégradeurs » qui marquent directement PAK4 pour élimination. Les premiers composés inhibiteurs de PAK4 ont montré un potentiel anti‑tumoral mais ont rencontré des difficultés de spécificité et de pharmacocinétique. Des molécules plus récentes, ciblant PAK4 avec plus de précision, ont donné des résultats marquants chez des souris obèses : moindre poids corporel sans réduction de l’appétit, foies plus sains, muscles plus actifs et meilleur contrôle glycémique. Les dégradeurs vont plus loin en éliminant physiquement PAK4, et des études animales préliminaires suggèrent qu’ils pourraient protéger contre la fonte musculaire et certains cancers. Ensemble, ces observations dessinent un scénario où l’abaissement de PAK4 pourrait simultanément atténuer l’obésité, le diabète et la stéatose hépatique, transformant un interrupteur cellulaire autrefois obscur en une cible prometteuse pour de futures thérapies métaboliques.
Citation: Bang, I.H., Park, BH. & Bae, E.J. PAK4 in metabolic diseases: regulation by nutrient signals and therapeutic implications. Exp Mol Med 58, 416–424 (2026). https://doi.org/10.1038/s12276-026-01645-y
Mots-clés: PAK4, maladie métabolique, obésité, foie gras, résistance à l’insuline