Clear Sky Science · fr
La protéine sensible au redox HMGB1 : rôles intracellulaires et extracellulaires
Pourquoi une protéine caméléon compte pour la santé
À l’intérieur de presque chaque cellule de votre corps se trouve une petite protéine appelée HMGB1 qui fonctionne un peu comme un outil multifonction. En conditions calmes, elle aide discrètement à organiser l’ADN. Mais lorsque les cellules sont stressées ou endommagées, HMGB1 peut quitter le noyau, se glisser dans le tissu environnant et agir comme un signal d’alarme pour le système immunitaire. Cette revue explique comment de minuscules modifications chimiques induites par l’oxydation transforment HMGB1 en personnalités biologiques très différentes — capables de protéger les tissus, de déclencher l’inflammation ou même de contribuer à des maladies chroniques. Comprendre cet « anneau d’humeur » moléculaire pourrait ouvrir de nouvelles voies pour apaiser l’inflammation excessive sans neutraliser totalement le système immunitaire.
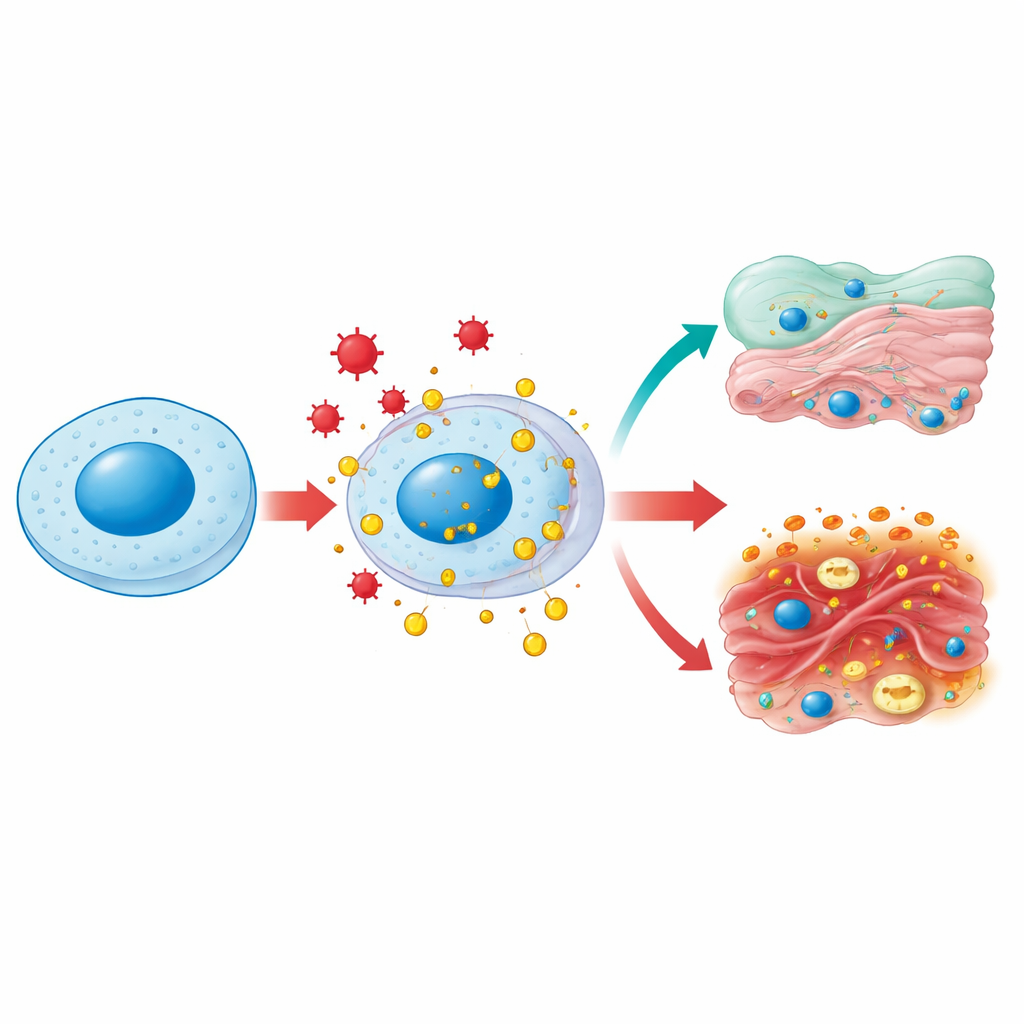
Une protéine, plusieurs quartiers d’action
HMGB1 vit normalement dans le noyau cellulaire, où elle plie et relâche l’ADN pour permettre la copie et la réparation des gènes. Sous stress — comme lors d’une infection, d’une hyperglycémie ou d’une lésion toxique — elle peut être modifiée chimiquement et escortée vers le cytoplasme puis à l’extérieur de la cellule. Dans le cytoplasme, HMGB1 contribue à la santé des mitochondries, les centrales énergétiques de la cellule, en favorisant un processus de nettoyage appelé autophagie et en empêchant une fragmentation excessive de ces organites. Une fois libérée à l’extérieur, HMGB1 devient un signal de danger classique : les cellules immunitaires la reconnaissent comme l’indication d’une lésion tissulaire et se précipitent sur les lieux. La même molécule joue donc des rôles d’entretien à l’intérieur des cellules et des rôles d’alarme à l’extérieur, selon son emplacement et son état chimique.
Comment l’oxydation réécrit son comportement
Le cœur de cette revue porte sur la manière dont l’oxydation — réactions pilotées par des espèces réactives de l’oxygène (ROS) — remodelent HMGB1. La protéine contient trois résidus sulfurés qui agissent comme de petits interrupteurs. À l’état totalement réduit, HMGB1 tend à soutenir la survie cellulaire et le recrutement des cellules réparatrices. Une oxydation modérée peut lier deux de ces sites entre eux au sein de la même protéine, créant une forme « disulfure » particulièrement apte à se fixer sur des récepteurs immunitaires tels que les récepteurs Toll-like et RAGE à la surface cellulaire. Cette version stimule fortement la production de messagers inflammatoires. Un stress oxydatif plus intense peut pousser la molécule vers une forme sur-oxydée qui ne peut plus se lier efficacement à l’ADN ni aux récepteurs ; cette forme « grillée » devient immunologiquement silencieuse et est associée à la phase de résolution de l’inflammation et à des programmes de mort cellulaire qui ne déclenchent pas d’attaque immunitaire.
Des signaux de mort cellulaire aux moteurs de maladie
HMGB1 est profondément lié aux multiples façons dont les cellules peuvent mourir. Lors de formes violentes de mort telles que la nécrose, la nécroptose, la ferroptose et la pyroptose, HMGB1 s’échappe ou est activement transportée hors des cellules, portant une signature rédox qui reflète les conditions oxydatives environnantes. Au début de la nécrose, elle tend à être sous forme réduite, tandis qu’un stress prolongé la pousse vers des états plus oxydés. Une fois à l’extérieur, HMGB1 réduite peut favoriser l’autophagie protectrice dans certaines cellules tumorales, les aidant à survivre à la chimiothérapie, tandis que les formes riches en disulfures et dimérisées amplifient les cascades inflammatoires et l’activation du complément pouvant aggraver les lésions tissulaires. HMGB1 peut aussi rétroagir pour promouvoir certaines voies de mort — par exemple en s’associant à des lipides bactériens pour déclencher la nécroptose ou en favorisant une mort cellulaire dépendante du fer dans les cellules de soutien du cerveau après un AVC. De cette façon, HMGB1 marque et module l’équilibre vie–mort dans les tissus.
Liens avec l’inflammation, l’auto-immunité et le cancer
Parce que son comportement est extrêmement sensible à l’oxydation, différentes variantes de HMGB1 apparaissent selon des motifs distincts selon les maladies. HMGB1 riche en disulfures est fortement associée à l’inflammation chronique : elle est présente dans les articulations enflammées de la polyarthrite rhumatoïde, dans le foie fibreux, dans les lésions pulmonaires, dans les dommages d’ischémie–reperfusion après chirurgie, et dans la sepsie, où son taux sanguin corrèle avec la gravité et le risque de décès. HMGB1 réduite, en revanche, accompagne souvent la migration cellulaire et le remodelage tissulaire, comme le déplacement des fibroblastes cardiaques ou des monocytes guidés par la chimiokine CXCL12. HMGB1 sur-oxydée et immunologiquement silencieuse est enrichie dans des contextes tels que l’apoptose tardive, où l’organisme souhaite éliminer les cellules mourantes sans provoquer d’attaque. Dans les tumeurs, la forme disulfure soutient un environnement immunitaire suppressif et permissif à la croissance, tandis que le blocage de HMGB1 peut réduire les tumeurs et rendre les immunothérapies ciblant les points de contrôle plus efficaces.
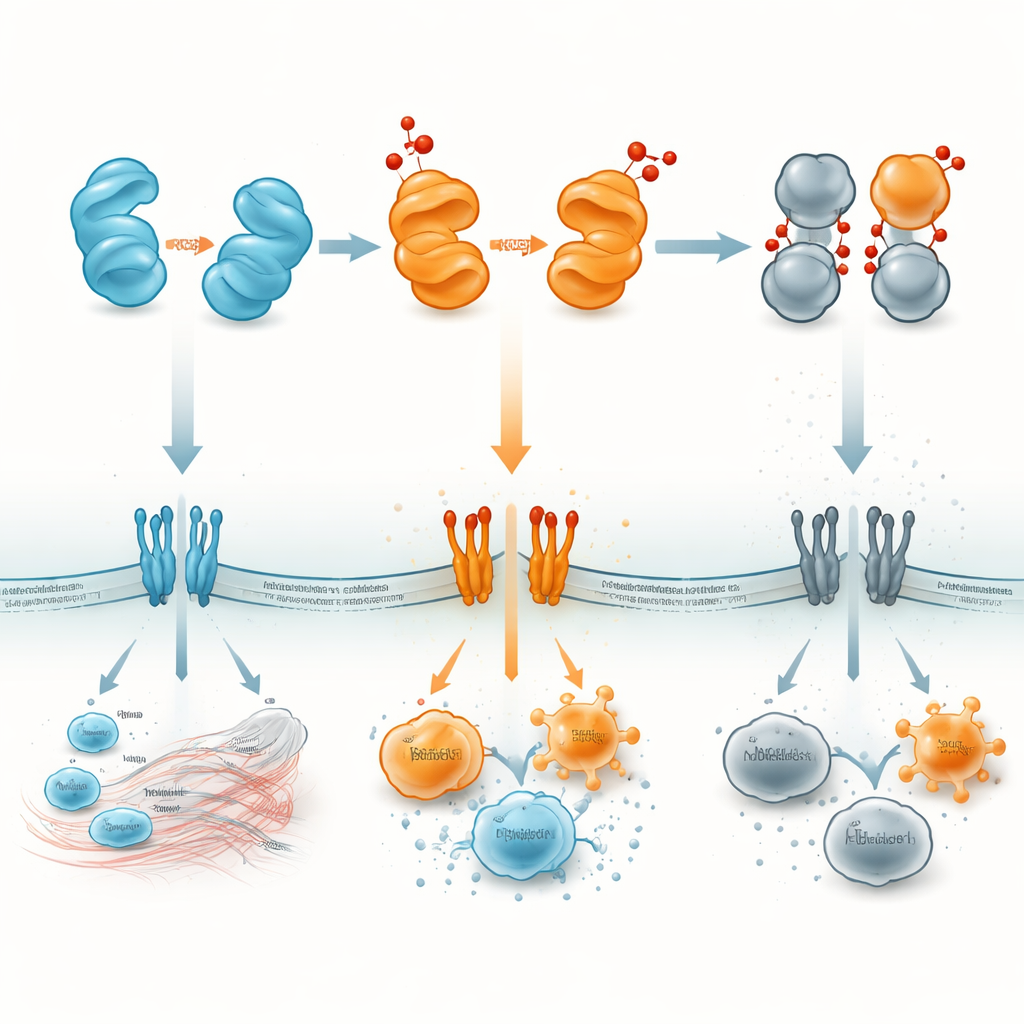
Transformer une alarme moléculaire en cible thérapeutique
Pour un observateur non spécialiste, HMGB1 peut être considérée comme une petite alarme protéique dont le volume et le message varient selon son état chimique. HMGB1 réduite a tendance à appeler des équipes de réparation ; les formes disulfure et dimérisées peuvent sonner une alarme stridente qui alimente une inflammation dommageable ; et la forme complètement oxydée se tait efficacement, contribuant à l’extinction de l’inflammation. En cartographiant où et quand chaque version apparaît — dans les noyaux, le cytoplasme, le sang ou des organes spécifiques — les chercheurs espèrent concevoir des médicaments qui bloquent les formes nocives ou stabilisent les formes bénéfiques. De telles stratégies pourraient permettre aux médecins de traiter la sepsie, les maladies auto-immunes, l’AVC, les lésions pulmonaires ou le cancer en ciblant non seulement HMGB1 elle-même, mais aussi le « variateur » oxydatif qui contrôle la manière dont cette protéine s’adresse au système immunitaire.
Citation: Kwak, M.S., Jung, S.F., Park, I.H. et al. The redox-sensitive protein HMGB1: intracellular and extracellular roles. Exp Mol Med 58, 345–356 (2026). https://doi.org/10.1038/s12276-026-01640-3
Mots-clés: HMGB1, inflammation, stress oxydatif, mort cellulaire, maladie auto-immune