Clear Sky Science · fr
Mécanotransduction via les récepteurs des cellules T : consensus, controverses et perspectives
Comment les cellules immunitaires perçoivent leur environnement
Notre système immunitaire ne se contente pas de détecter des signaux chimiques ; il ressent aussi des forces physiques. Cet article de synthèse examine comment les cellules T — globules blancs qui traquent virus et cancers — pourraient utiliser de petites poussées et tractions sur leurs récepteurs de surface pour décider d’attaquer ou non. Comprendre ce « sens du toucher » à l’échelle moléculaire pourrait modifier notre vision des vaccins, de l’immunothérapie anticancéreuse et des maladies auto-immunes.
Le rôle particulier du récepteur des cellules T
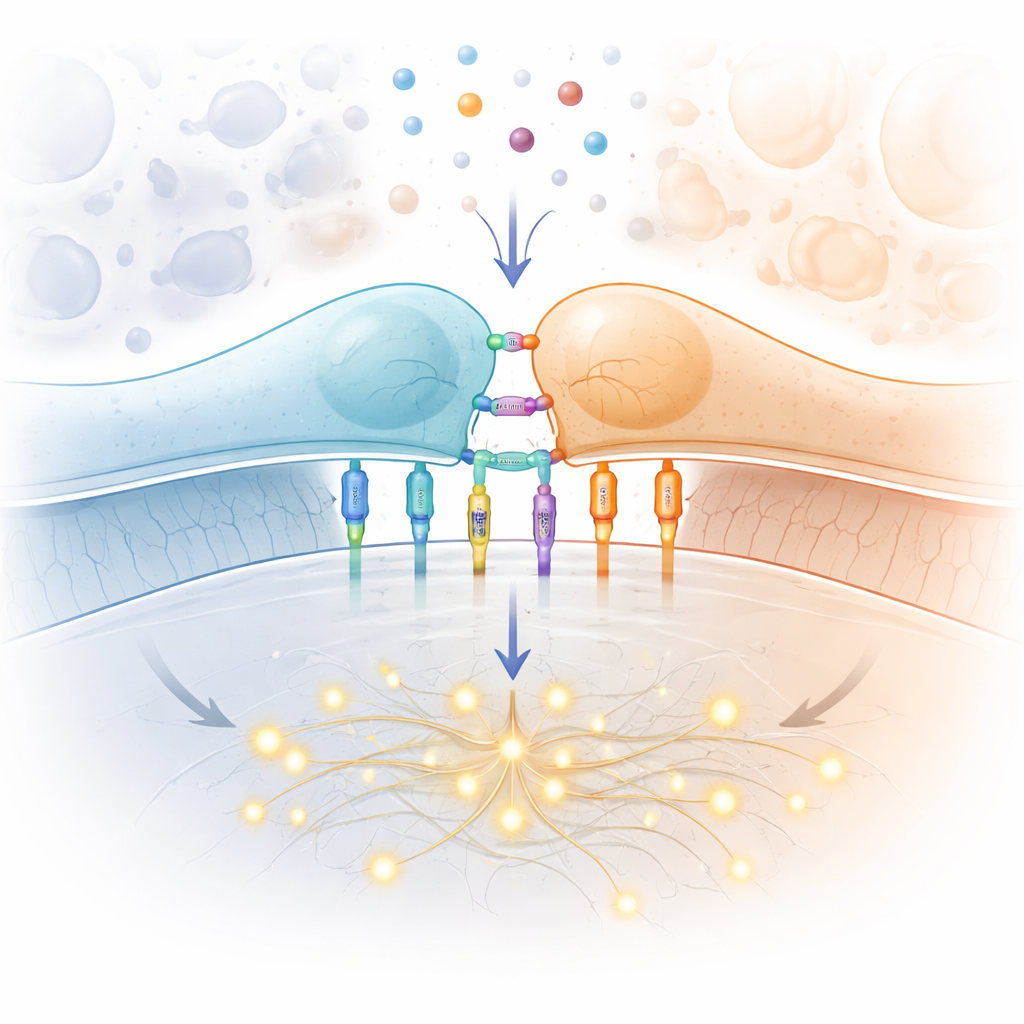
Au cœur du propos se trouve le récepteur des cellules T, une machine moléculaire à la surface des cellules T qui inspecte des fragments de protéines présentés par d’autres cellules. Lorsqu’un fragment approprié est repéré, la cellule T peut entrer en action, se multiplier et éliminer des cibles infectées ou cancéreuses. Ce récepteur doit satisfaire à des exigences ardues : il doit réagir à un nombre infime de fragments étrangers, ignorer une mer de fragments du soi inoffensifs, agir rapidement alors que les cellules T patrouillent l’organisme et ce, pour des millions de variantes de récepteurs chez chaque individu. Le câblage classique de la voie de signalisation à l’intérieur de la cellule — impliquant kinases, échafaudages protéiques et facteurs de transcription — est bien cartographié. Ce qui demeure mystérieux, c’est la toute première étape : comment le simple acte de liaison à un fragment à la surface cellulaire bascule le récepteur de l’état silencieux à l’état actif.
Idées concurrentes pour l’étincelle initiale
Les chercheurs ont proposé plusieurs modèles expliquant l’activation initiale du récepteur des cellules T. Dans une approche, la signalisation commence lorsque les récepteurs sont regroupés en petits clusters, augmentant la concentration locale et permettant aux réactions de signalisation de se dérouler plus efficacement. Une autre idée met l’accent sur des changements de conformation : la liaison pourrait tordre ou détendre des parties du complexe récepteur, libérant des segments enfouis à l’intérieur de la cellule pour que des enzymes puissent les modifier. Un troisième modèle souligne l’encombrement au niveau du contact cellule–cellule. Ici, des paires récepteur–ligand courtes se compactent en zones étroites qui excluent physiquement les enzymes volumineuses qui éteignent normalement les signaux, faisant pencher la balance vers l’activation. Chaque modèle est étayé par des expériences et explique une partie du puzzle, mais aucun n’explique à lui seul la sensibilité extrême du récepteur ni sa capacité à distinguer des fragments protéiques très semblables.
Quand le toucher et la force entrent en jeu
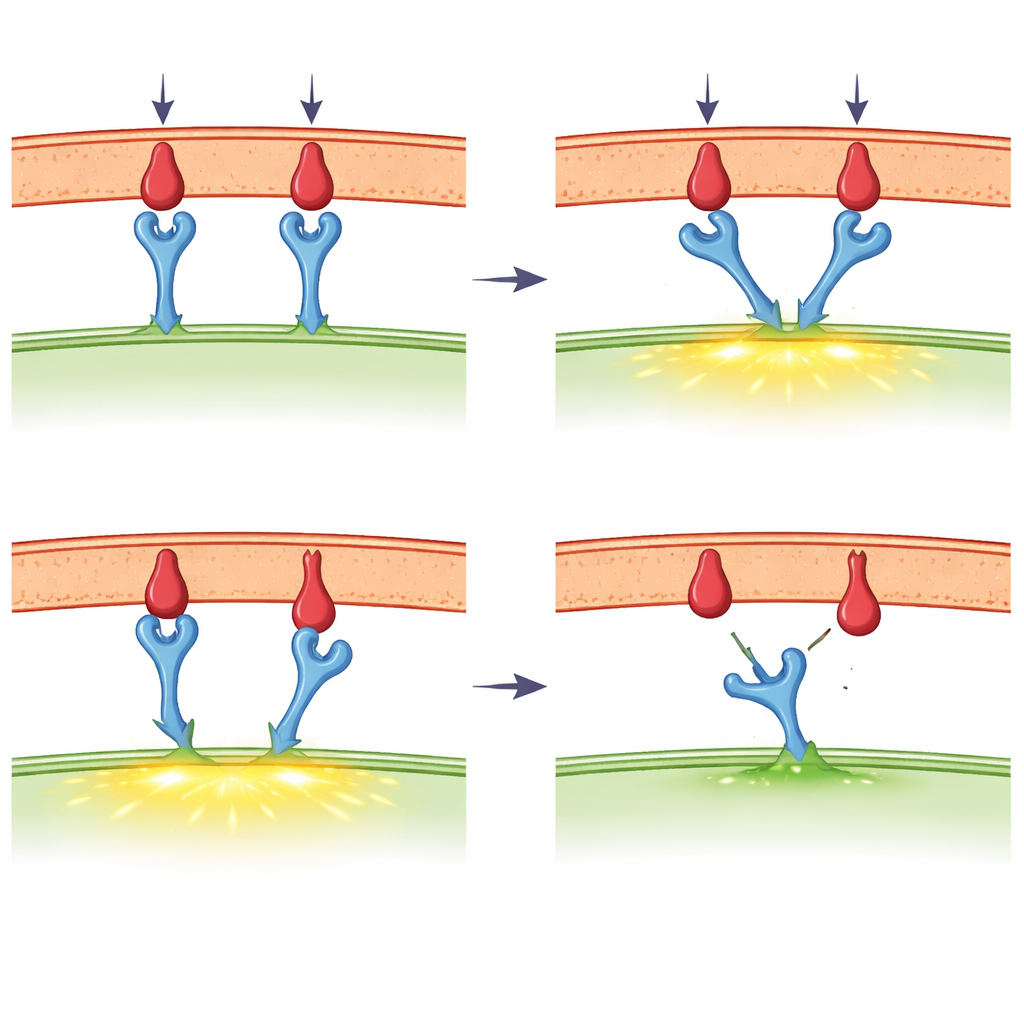
Un axe majeur de la revue est l’idée émergente selon laquelle le récepteur des cellules T agit comme un mécanorécepteur — un dispositif qui répond à la force. À l’aide d’instruments ultra-sensibles, les scientifiques ont tiré sur des liaisons récepteur–ligand individuelles avec des forces un billionième de fois plus faibles que le poids d’une pomme. Ils constatent que, pour des fragments étrangers puissants, une traction modeste peut en réalité prolonger la durée de vie de la liaison, un comportement connu sous le nom de « catch ». Les fragments plus faibles ou du soi présentent plutôt un comportement de « slip » : ils se rompent plus rapidement lorsqu’on les tire. Les cellules T elles-mêmes génèrent de telles forces via leur squelette interne d’actine et des protéines motrices, en particulier au niveau de la zone de contact étroite appelée synapse immunitaire. De nouvelles sondes de tension moléculaires montrent que des forces situées dans la plage où apparaît le comportement de type catch sont bien présentes lors des premières étapes d’activation des cellules T, bien que différentes méthodes expérimentales rapportent parfois des valeurs différentes et aient suscité des débats animés.
Décoder le soi du non-soi au fil du temps
L’article revient également sur la manière dont les cellules T pourraient transformer des événements de contact bruyants et fugitifs en décisions fiables. Une idée ancienne, la preuve cinétique, suggère que la signalisation progresse par une séquence d’étapes nécessitant du temps ; seuls les fragments qui maintiennent le récepteur engagé suffisamment longtemps permettent à la chaîne d’atteindre un point de non-retour. Les auteurs discutent comment les effets mécaniques peuvent affiner ce filtre temporel : les forces de traction prolongent la durée des liaisons productives et raccourcissent celles non productives, élargissant l’écart entre stimuli forts et faibles. Ils examinent aussi comment les cellules T peuvent intégrer de nombreux contacts courts plutôt que de compter sur un seul contact long, et comment des rétroactions dans le réseau de signalisation peuvent stocker une sorte de « mémoire » moléculaire des rencontres récentes. Ces raffinements contribuent à expliquer comment les cellules T concilient vitesse et précision dans des environnements tissulaires complexes.
Principes communs entre les récepteurs immunitaires
Bien que le récepteur des cellules T soit particulièrement exigeant dans ce qu’il doit accomplir, nombre de ses principes de conception apparaissent chez d’autres récepteurs immunitaires. Les récepteurs des cellules B et les récepteurs d’anticorps sur les cellules immunitaires innées partagent des motifs de signalisation similaires et fonctionnent souvent dans des zones de contact rapproché où l’encombrement, le regroupement et les forces cytosquelettiques comptent tous. Des réponses de type catch aux forces ont désormais été rapportées pour plusieurs paires récepteur–ligand de ce type. Cela suggère que la détection d’indices mécaniques peut être une stratégie générale utilisée par le système immunitaire pour vérifier si une cible est fermement ancrée, correctement présentée et digne d’une réponse.
Pourquoi cela importe pour la santé et la thérapie
Pour le lecteur non spécialiste, la conclusion est que les cellules T ne se contentent pas de « sentir » la présence de molécules étrangères : elles testent aussi comment ces molécules réagissent lorsqu’on les tire. En combinant chimie, physique et biologie cellulaire, cette revue soutient que les récepteurs immunitaires convertissent de subtiles différences à la fois de liaison et de force en décisions de vie ou de mort pour les cellules. Une compréhension approfondie de ces règles mécanobiologiques pourrait orienter la conception de meilleures thérapies basées sur les cellules T, de vaccins plus précis et de nouveaux traitements qui moduleraient les réponses immunitaires en changeant non seulement ce que les récepteurs lient, mais aussi la façon dont ils sont engagés mécaniquement.
Citation: Travaglino, S., Jeon, Y., Kim, Y. et al. Mechanotransduction through T cell receptors: consensus, controversies and future outlooks. Exp Mol Med 58, 319–335 (2026). https://doi.org/10.1038/s12276-026-01639-w
Mots-clés: récepteur des cellules T, mécanotransduction, liaisons à prise (catch bonds), synapse immunitaire, preuve cinétique