Clear Sky Science · fr
UBE2M comme passerelle entre la neddylation et la régulation du cycle cellulaire dans l’adénocarcinome colorectal
Pourquoi cette recherche importe pour le cancer intestinal
Le cancer colorectal est l’un des cancers les plus fréquents et mortels dans le monde, principalement parce que les cellules tumorales apprennent à se diviser sans contrôle. Cette étude met au jour un interrupteur de régulation jusque-là caché qui aide les cellules du cancer colorectal à franchir rapidement un point de contrôle critique de la division cellulaire. En révélant le fonctionnement moléculaire de cet interrupteur — et en montrant qu’un antifongique existant peut l’interférer — le travail suggère une nouvelle voie possible pour ralentir ou arrêter la croissance tumorale.
Une couche de contrôle cachée à l’intérieur des cellules tumorales
Les cellules ne se divisent pas au hasard ; elles traversent un cycle ordonné avec des points de contrôle qui vérifient s’il est sûr de copier l’ADN et de se scinder en deux. Les cellules cancéreuses manipulent souvent ces points de contrôle. Les auteurs se sont intéressés à un processus d’étiquetage chimique appelé neddylation, qui modifie subtilement les protéines après leur synthèse. Des études antérieures laissaient entendre que la neddylation est plus active dans de nombreux cancers, mais la manière dont elle se relie au cycle de division des cellules colorectales restait floue. En utilisant de grands jeux de données unicellulaires issus de tumeurs humaines, ainsi que des données d’expression génique en masse provenant de plus de 1 800 patients, l’équipe a constaté que l’activité de la neddylation est particulièrement élevée dans les cellules intestinales malignes qui se trouvent en phase G2/M — la dernière porte avant la division cellulaire.
Zoom sur une protéine « pont » moléculaire
Pour déterminer quelles molécules relient la neddylation à la division cellulaire, les chercheurs ont utilisé des analyses computationnelles de type réseau pour passer au crible des milliers de gènes. Une protéine s’est détachée : UBE2M, une enzyme qui aide à attacher la petite étiquette NEDD8 à d’autres protéines. UBE2M n’était pas seulement fortement liée aux voies de la neddylation et du cycle cellulaire dans les données ; elle était également beaucoup plus abondante dans les tumeurs colorectales que dans les tissus normaux adjacents. Les patients dont les tumeurs présentaient des niveaux élevés de UBE2M avaient tendance à avoir une survie plus mauvaise, ce qui en fait un candidat potentiel pour être un moteur plutôt qu’un simple spectateur. Lorsque l’équipe a réduit l’expression de UBE2M dans des lignées cellulaires cancéreuses et dans des modèles tumoraux murins, la croissance tumorale a ralenti, la division cellulaire a diminué et davantage de cellules ont subi une mort programmée. À l’inverse, forcer la surproduction de UBE2M a accéléré la croissance et la progression du cycle cellulaire.
Un relais qui protège une protéine clé favorisant la croissance
En creusant plus avant, les scientifiques ont cherché comment UBE2M aide les cellules à se diviser. Ils ont découvert que UBE2M n’agit pas seul mais déclenche un relais impliquant deux autres protéines, USP39 et PABPC1. Normalement, PABPC1 est ciblé pour destruction par une chaîne d’étiquettes ubiquitine qui l’envoient vers la machinerie de recyclage des protéines de la cellule. L’équipe a montré que UBE2M modifie chimiquement USP39 par l’ajout de NEDD8. Cette modification renforce la capacité de USP39 à couper les chaînes d’ubiquitine sur PABPC1, le sauvant ainsi de la destruction et le rendant plus stable. Avec plus de PABPC1 disponible, la cellule devient plus efficace pour traduire certains ARNm en protéines, notamment l’ARNm de CCNB1, une cycline qui joue le rôle d’accélérateur au point de contrôle G2/M. En substance, UBE2M aide à stabiliser PABPC1, ce qui augmente à son tour la production de CCNB1 et pousse les cellules à entrer plus facilement en division.
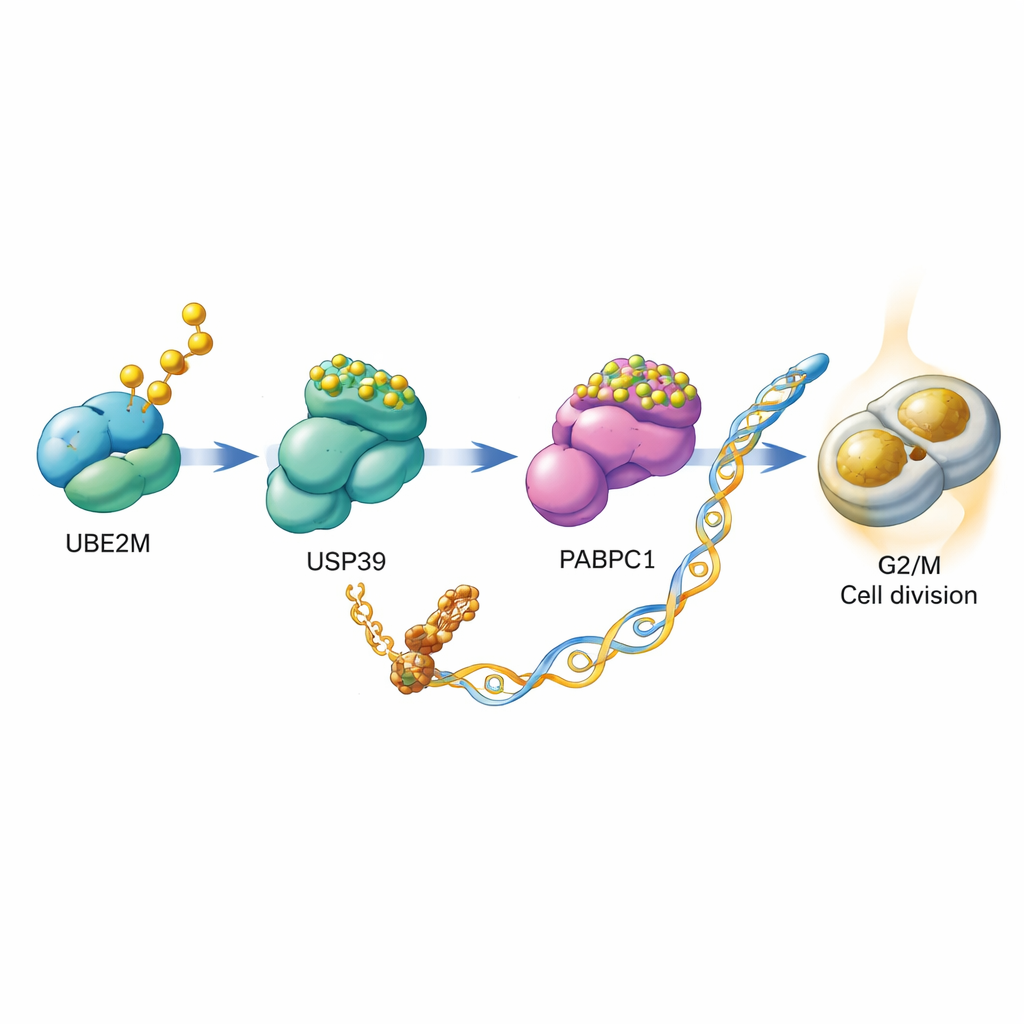
Du mécanisme moléculaire à une opportunité médicamenteuse
La découverte de cette chaîne UBE2M–USP39–PABPC1–CCNB1 a suggéré une nouvelle vulnérabilité des cellules du cancer colorectal. Les auteurs se sont tournés vers la micafungine, un médicament déjà utilisé contre les mycoses et récemment identifié comme inhibiteur de l’activité de neddylation de UBE2M. Dans des cellules de cancer intestinal cultivées en laboratoire, la micafungine a affaibli la neddylation de USP39, augmenté la dégradation de PABPC1 et réduit les niveaux de protéine CCNB1. En conséquence, la division cellulaire a ralenti, davantage de cellules se sont retrouvées bloquées au point de contrôle G2/M et l’apoptose a augmenté. Chez des souris implantées avec des cellules de cancer colorectal, un traitement quotidien par micafungine a significativement réduit la taille des tumeurs comparé aux animaux non traités, sans nécessité d’éliminer UBE2M lui‑même.
Ce que cela signifie pour les patients à long terme
Ce travail offre une image claire de la manière dont une seule enzyme, UBE2M, peut lier un système subtil d’étiquetage des protéines à la décision d’une cellule de cancer intestinal de se diviser. En stabilisant un facteur de traduction (PABPC1) via USP39, UBE2M augmente indirectement les niveaux d’un puissant moteur du cycle cellulaire, CCNB1, permettant aux tumeurs de croître plus rapidement. Bien que des recherches et des essais cliniques supplémentaires soient nécessaires, ces résultats suggèrent que bloquer ce relais — potentiellement avec des médicaments repositionnés comme la micafungine — pourrait offrir une nouvelle stratégie ciblée pour ralentir la progression du cancer colorectal et améliorer les résultats pour les patients.
Citation: Wang, Z., Wang, Y., Chen, Y. et al. UBE2M as a bridge spanning neddylation and cell cycle regulation in colorectal adenocarcinoma. Exp Mol Med 58, 501–518 (2026). https://doi.org/10.1038/s12276-026-01636-z
Mots-clés: cancer colorectal, cycle cellulaire, neddylation, UBE2M, thérapie ciblée