Clear Sky Science · fr
Toxicité gastro-intestinale induite par les médicaments et intégrité de la barrière : altération médiée par le cytosquellette dans un modèle d’épithélium intestinal humain cliniquement pertinent
Pourquoi les effets secondaires sur l’intestin comptent
De nombreux médicaments destinés à combattre le cancer, l’inflammation ou d’autres maladies peuvent involontairement endommager la muqueuse de nos intestins. Lorsque cette « peau » interne de l’intestin est abîmée, les personnes peuvent souffrir de diarrhée, de douleurs, de nausées et d’une mauvaise absorption des nutriments, parfois à un point tel que les médecins doivent interrompre ou réduire des traitements vitaux. Pourtant, les tests de laboratoire usuels ne détectent souvent pas ces problèmes avant que les médicaments n’atteignent les patients. Cette étude présente un modèle de laboratoire plus réaliste de l’intestin humain et montre comment il peut repérer plus tôt les médicaments nocifs pour l’intestin et révéler comment ils affaiblissent la barrière naturelle du corps.
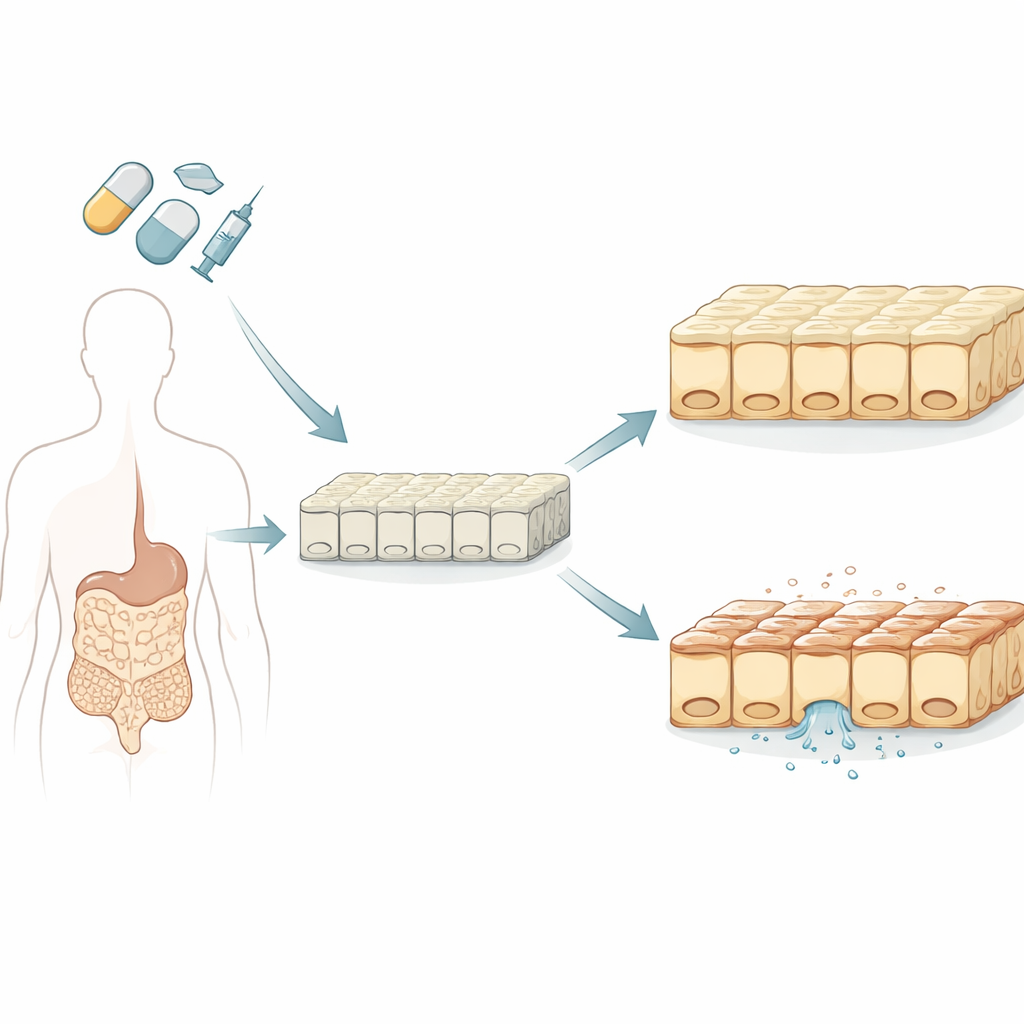
Construire un meilleur mini‑intestin
Les chercheurs ont commencé par cultiver des feuillets de cellules intestinales humaines en laboratoire à partir de cellules souches, qui peuvent se différencier en de nombreux types tissulaires. Contrairement à une lignée cellulaire d’origine tumorale traditionnellement utilisée pour les tests médicamenteux, ces cellules dérivées de cellules souches ont formé une communauté mixte qui ressemble davantage au petit intestin réel, incluant des cellules sécrétrices de mucus et productrices d’hormones. L’équipe a confirmé que ces revêtements cultivés en laboratoire présentaient une étanchéité réaliste, une polarité haut‑bas correcte et des fonctions clés de transport et de métabolisme qui influencent la façon dont les médicaments traversent et sont traités par l’intestin.
Mesurer l’étanchéité électrique de la barrière
Pour évaluer la sécurité intestinale, le groupe s’est concentré sur la résistance électrique transepitheliale, ou TEER, un indicateur non invasif de la qualité du scellement entre cellules voisines. Une TEER élevée signifie une barrière serrée et protectrice ; une TEER en baisse signifie que la paroi entre l’intestin et la circulation sanguine devient poreuse. Les scientifiques ont comparé la TEER à un test standard de survie cellulaire mesurant des molécules énergétiques telles que l’ATP. Ils ont exposé à la fois leur nouveau modèle intestinal et le modèle tumoral plus ancien à 17 médicaments connus pour différer quant à la fréquence de leurs effets gastro‑intestinaux, y compris des agents de chimiothérapie courants, des traitements oncologiques ciblés et des analgésiques comme l’ibuprofène et d’autres anti‑inflammatoires.
Détecter des dommages cachés avant la mort cellulaire
Sur ce panel de médicaments, les mesures de TEER sur le revêtement intestinal dérivé de cellules souches ont surpassé le test ATP traditionnel et le modèle de cellules tumorales plus ancien. Plusieurs médicaments de chimiothérapie ont montré peu de changement d’ATP, ce qui suggère que les cellules restaient vivantes, mais ils ont provoqué d’importantes chutes de TEER et des dommages évidents dans les images de marquage vital/mort. Cela signifie que la barrière peut céder avant que les cellules ne meurent complètement — un signal d’alerte précoce que les tests de viabilité classiques manquent. Lorsque l’équipe a comparé ses résultats de laboratoire aux dossiers cliniques sur la fréquence des symptômes intestinaux associés à chaque médicament, le nouvel essai TEER a correctement identifié presque tous les médicaments à risque élevé et a rassuré pour les médicaments à faible risque, atteignant une très grande précision.
Comment les médicaments s’attaquent à l’armature interne
Pour comprendre ce qui se passait à l’intérieur des cellules, les scientifiques ont analysé l’activité génique après traitement par deux agents de chimiothérapie ciblant les microtubules, une composante clé de l’armature interne cellulaire. Ils ont observé des réductions étendues des gènes impliqués dans le cytosquelette, l’adhésion cellule‑à‑cellule et la matrice extracellulaire — le réseau qui aide les cellules à s’ancrer à leur environnement. Des expériences supplémentaires ont montré des augmentations dépendantes de la dose des espèces réactives de l’oxygène, des molécules instables contenant de l’oxygène susceptibles d’endommager les structures cellulaires. Ensemble, ces changements suggèrent une chaîne d’événements où certains médicaments perturbent le cadre interne et les connexions des cellules intestinales, relâchant la barrière et permettant le passage de substances entre les cellules.
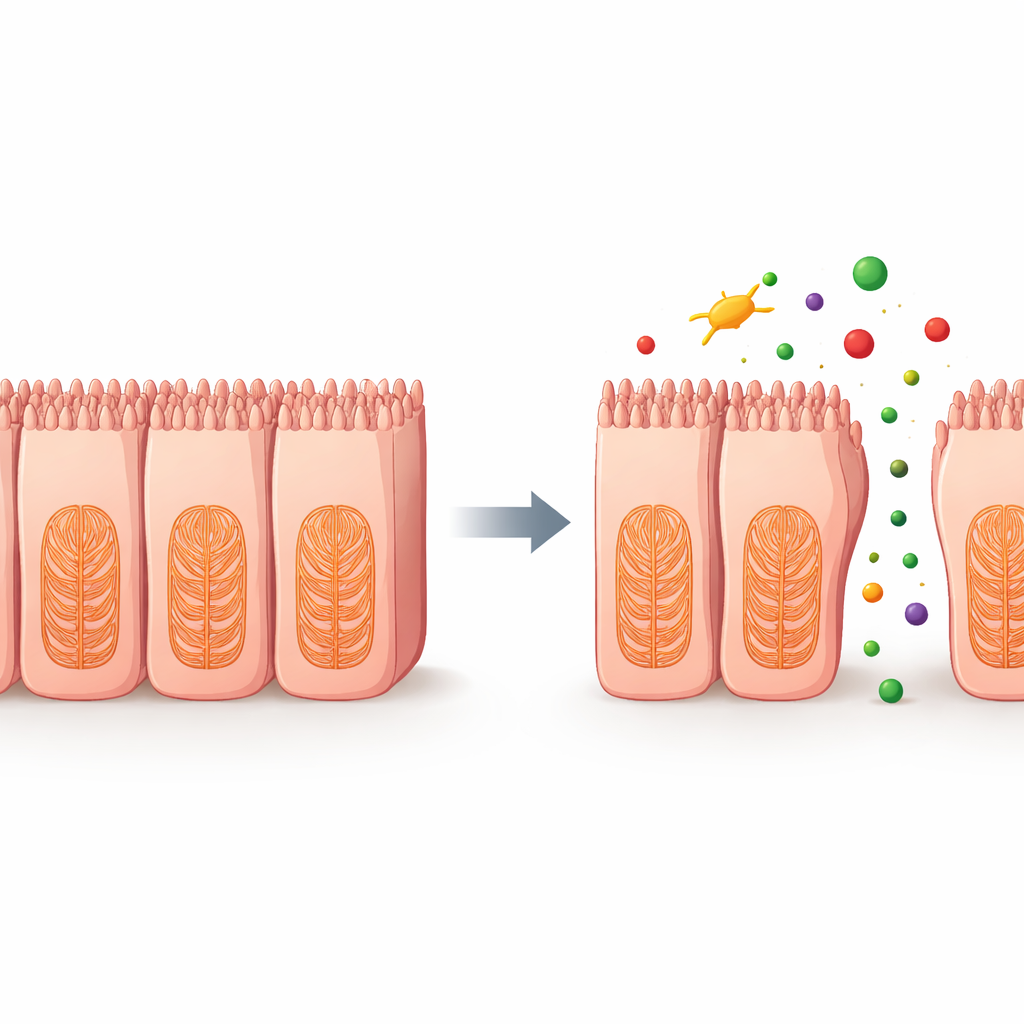
Ce que cela signifie pour les patients
Ce travail montre qu’un revêtement intestinal humain basé sur des cellules souches, associé à des mesures électriques simples de l’étanchéité de la barrière, peut prédire de façon plus fiable quels médicaments risquent de causer des lésions intestinales que les méthodes de laboratoire traditionnelles. En détectant précocement l’affaiblissement de la barrière — et en l’associant aux dommages sous‑jacents au cytosquelette cellulaire — cette plateforme pourrait aider les développeurs de médicaments à éliminer ou à repenser des composés risqués avant qu’ils n’arrivent en clinique. À long terme, de tels tests réalistes de « mini‑intestin » pourraient réduire les effets gastro‑intestinaux désagréables ou dangereux pour les patients tout en permettant aux médecins d’utiliser des thérapies puissantes de manière plus sûre.
Citation: Yu, W.D., Lee, S., Cho, HS. et al. Drug-induced gastrointestinal toxicity and barrier integrity: cytoskeleton-mediated impairment in a clinically relevant human intestinal epithelium model. Exp Mol Med 58, 487–500 (2026). https://doi.org/10.1038/s12276-025-01635-6
Mots-clés: toxicité gastro-intestinale, barrière intestinale, modèle de cellules souches, sécurité des médicaments, effets secondaires de la chimiothérapie