Clear Sky Science · fr
La CDK13 stimule le carcinome rénal à cellules claires via la modification m6A de l’ARNm d’ACLY médiée par METTL16
Pourquoi les tumeurs rénales riches en graisses comptent
Le cancer rénal à cellules claires apparaît souvent pâle et huileux au microscope parce que ses cellules sont remplies de lipides. Cette apparence particulière n’est pas qu’esthétique ; elle reflète une réorganisation profonde de la façon dont ces cellules cancéreuses gèrent leur carburant. Cette étude pose une question simple mais importante : quel interrupteur moléculaire pousse les cellules tumorales rénales à accumuler des graisses, et peut‑on désactiver cet interrupteur pour ralentir la maladie ?
Un chef d’orchestre caché de la croissance tumorale
Les chercheurs se sont concentrés sur une protéine appelée CDK13, membre d’une famille d’enzymes qui aide normalement les cellules à se diviser. En analysant de larges jeux de données patients et des échantillons tumoraux, ils ont constaté que les niveaux de CDK13 sont systématiquement plus élevés dans les carcinomes rénaux à cellules claires que dans le tissu rénal normal. Les patients dont les tumeurs présentaient plus de CDK13 avaient tendance à avoir des cancers plus volumineux, plus avancés et des pronostics plus défavorables. Quand l’équipe a réduit CDK13 dans des lignées cellulaires de cancer du rein, les cellules proliféraient moins et rencontraient des difficultés à progresser dans le cycle cellulaire, suggérant que CDK13 agit comme un chef d’orchestre caché coordonnant à la fois croissance et survie.
Du sucre au gras : réorienter l’usine énergétique de la cellule
Parce que les tumeurs rénales à cellules claires sont saturées en lipides, l’équipe a examiné si CDK13 contrôle aussi la façon dont ces cellules fabriquent des graisses. À l’aide d’un couplage de profils d’expression génique et de colorations lipidiques au microscope, ils ont montré que l’augmentation de CDK13 favorise l’accumulation de gouttelettes lipidiques à l’intérieur des cellules cancéreuses, tandis que la diminution de CDK13 a l’effet inverse. CDK13 influençait fortement une enzyme appelée ACLY, qui convertit un intermédiaire métabolique courant en acétyl‑CoA, matière première pour la synthèse des acides gras et du cholestérol. Un taux élevé de CDK13 s’accompagne d’un taux élevé d’ACLY dans les tumeurs de patients, et les deux protéines se concentrent dans les mêmes régions du tissu tumoral. Lorsque ACLY était augmenté artificiellement, cela corrigeait de nombreuses déficiences de croissance et de stockage lipidique causées par la perte de CDK13, positionnant ACLY comme un effecteur clé en aval de cette voie. 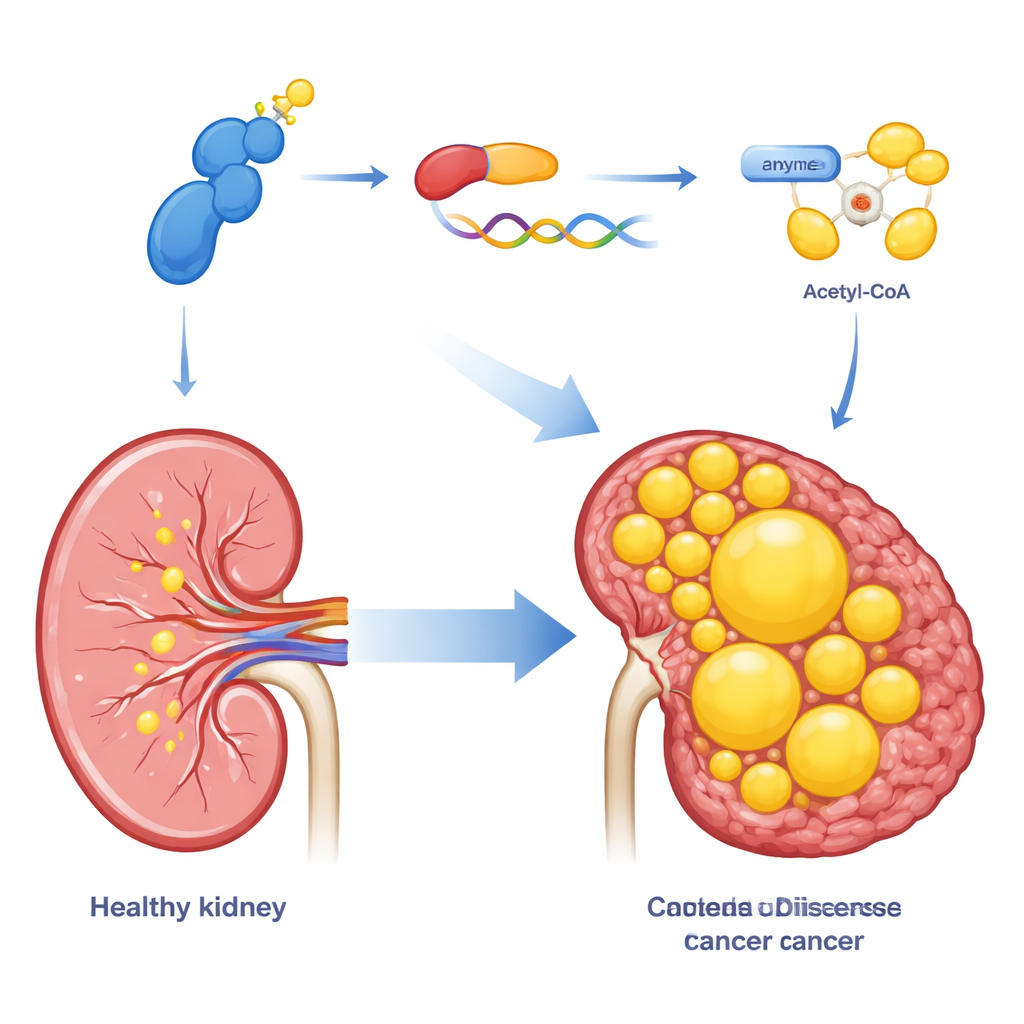
Un système de messages en couches à l’intérieur des cellules cancéreuses
Plutôt que d’agir directement sur ACLY comme un simple interrupteur marche/arrêt, CDK13 exerce son influence via un système de messages en couches fondé sur l’ARN, la molécule qui transporte les instructions génétiques de l’ADN vers les usines protéiques. Les auteurs ont découvert que CDK13 se lie physiquement à une autre enzyme, METTL16, et la modifie chimiquement : METTL16 ajoute des marques méthyle sur des messages ARN spécifiques. CDK13 ajoute un groupe phosphate à METTL16 à un site précis, rendant METTL16 plus actif. En retour, METTL16 place des marques méthyle supplémentaires sur le plan d’ARN d’ACLY. Ces marques ne changent pas le code génétique lui‑même, mais elles modifient la manière dont la cellule traite ce message. Une troisième protéine, YTHDC2, reconnaît l’ARN d’ACLY marqué et le protège de la dégradation, permettant ainsi la production d’une plus grande quantité d’ACLY au fil du temps. Cette cascade — CDK13 activant METTL16, METTL16 marquant l’ARN d’ACLY, et YTHDC2 protégeant ce message marqué — crée une boucle puissante qui stimule la synthèse des graisses. 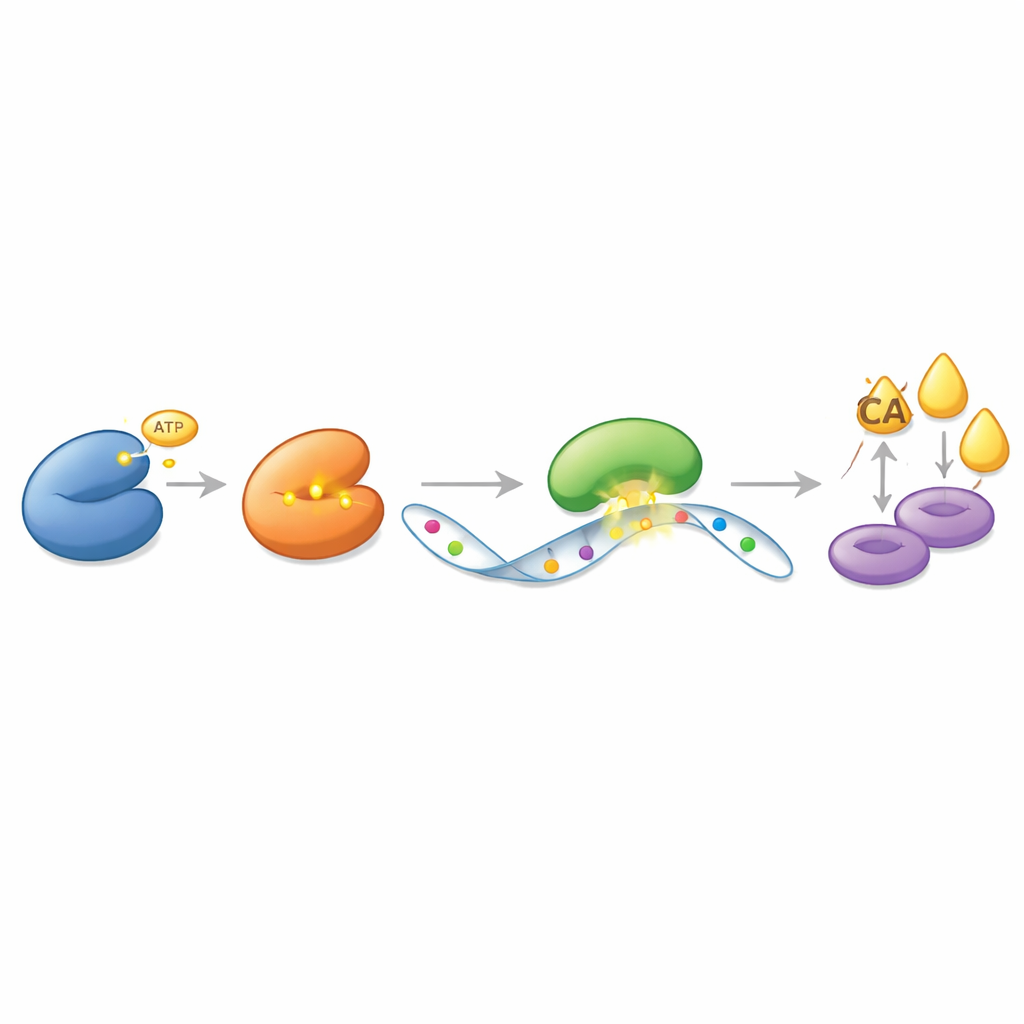
Tester la chaîne dans des cellules, des souris et des échantillons de patients
La solidité du travail réside dans la rigueur des tests de cette chaîne d’événements. Dans des cellules de cancer du rein en culture, perturber n’importe quelle partie de la voie CDK13–METTL16–ACLY réduisait les gouttelettes lipidiques et ralentissait la prolifération. Chez des souris implantées avec des cellules humaines de cancer du rein, bloquer soit CDK13 soit ACLY réduisait la taille des tumeurs et diminuait leurs réserves lipidiques, tandis que bloquer les deux simultanément produisait un effet encore plus marqué. L’équipe a également utilisé un composé de petite molécule, 1NM‑PP1, qui inhibe l’activité de CDK13. Cet agent de type médicament réduisait la marque activatrice sur METTL16, abaissait les niveaux d’ACLY et freinait la croissance tumorale, surtout en combinaison avec l’épuisement de METTL16. Dans les jeux de données patients, CDK13, METTL16 et ACLY avaient tendance à augmenter et diminuer ensemble, renforçant l’idée que cet axe est actif dans de vrais cancers, pas seulement dans des modèles de laboratoire.
Ce que cela pourrait signifier pour les traitements futurs
Pour les non‑spécialistes, le message clé est que cette étude révèle un nouveau bouton de commande de « l’usine à graisses » à l’intérieur des tumeurs rénales à cellules claires. Plutôt que de cibler uniquement les enzymes qui fabriquent les lipides, les chercheurs mettent au jour une chaîne de commandement de niveau supérieur qui stabilise les instructions pour ces enzymes. En interrompant l’axe CDK13–METTL16–ACLY, il pourrait être possible d’affamer les tumeurs des lipides dont elles ont besoin pour croître et se propager, tout en affectant moins les cellules normales. Bien que le travail soit encore préclinique et que 1NM‑PP1 ne soit pas encore un médicament contre le cancer du rein, les résultats ouvrent la voie à de nouvelles stratégies associant inhibiteurs de kinases et médicaments ciblant les enzymes modifiant l’ARN, offrant une manière plus précise de traiter cette forme de cancer du rein à métabolisme spécifique.
Citation: Chen, J., Liu, H., Zhang, Y. et al. CDK13 drives clear cell renal carcinoma through METTL16-mediated m6A modification of ACLY mRNA. Exp Mol Med 58, 472–486 (2026). https://doi.org/10.1038/s12276-025-01634-7
Mots-clés: carcinome rénal à cellules claires, métabolisme des lipides, CDK13, méthylation de l’ARN, ACLY