Clear Sky Science · fr
Le facteur régulateur des interférons 5 participe à la pathogenèse de l’emphysème via les cellules exprimant NLRP3 et Ly6C
Pourquoi cette étude pulmonaire compte
La maladie pulmonaire obstructive chronique (MPOC) et l’emphysème dépouillent des millions de personnes de leur souffle, souvent longtemps après qu’elles aient arrêté de fumer. Les médicaments actuels peuvent aider à ouvrir les voies aériennes, mais ils font peu pour calmer l’inflammation latente qui ronge en continu les poumons. Cette étude identifie un « instigateur » moléculaire de ce dommage, suggérant une nouvelle voie pour protéger les alvéoles fragiles et ralentir le déclin de la fonction pulmonaire.
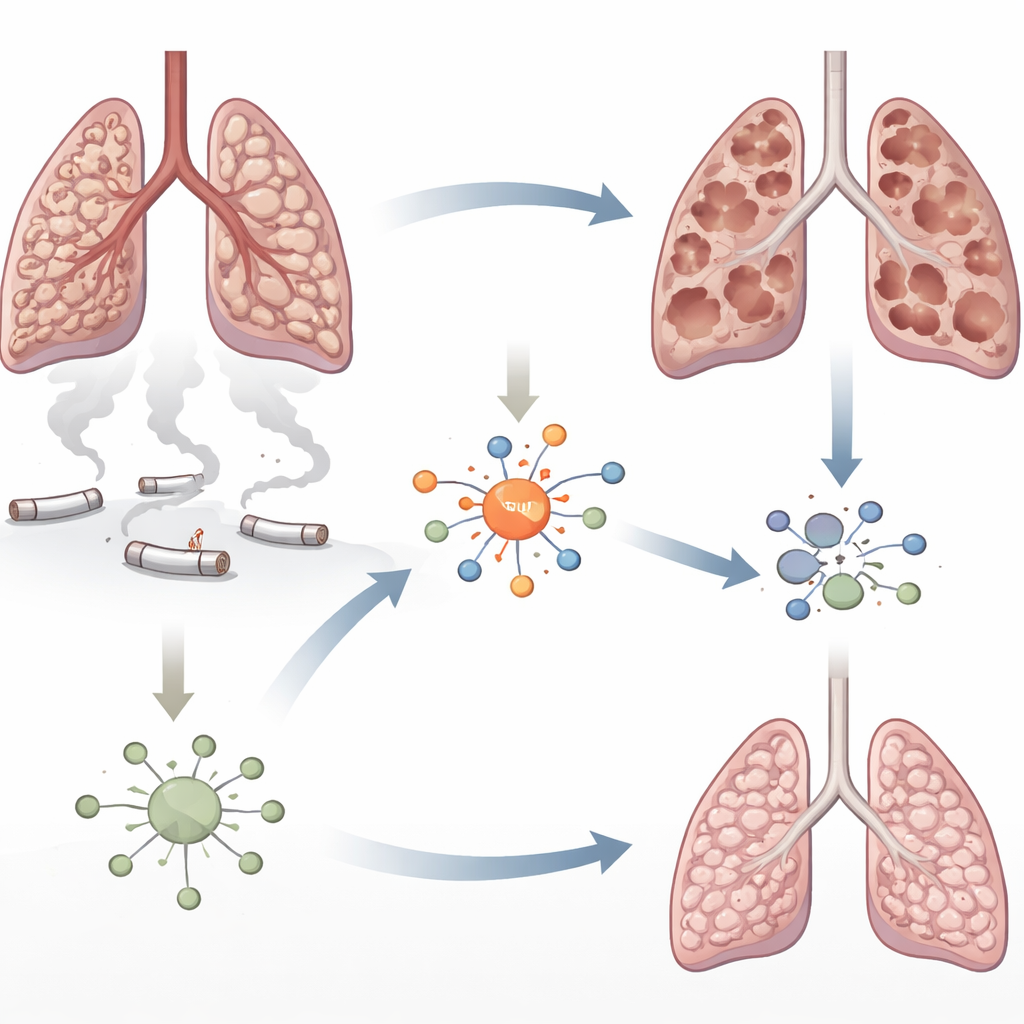
Un regard plus attentif sur les poumons endommagés par la fumée
L’emphysème se caractérise par la dégradation progressive des minuscules alvéoles qui échangent oxygène et dioxyde de carbone. La fumée de cigarette inonde les poumons de particules toxiques qui blessent les cellules et attirent des vagues de cellules immunitaires. Les auteurs se sont concentrés sur une protéine appelée facteur régulateur des interférons 5 (IRF5), connue pour stimuler l’inflammation dans les maladies auto-immunes mais peu étudiée dans la MPOC. Des travaux antérieurs laissaient entendre que les niveaux d’IRF5 augmentent dans les poumons exposés à la fumée. Ici, les chercheurs ont cherché à déterminer si IRF5 accompagne simplement l’inflammation ou s’il contribue réellement à la destruction du tissu pulmonaire.
Désactiver un commutateur clé chez la souris
Pour étudier le rôle d’IRF5, l’équipe a créé des souris dépourvues du gène codant cette protéine. Ils ont ensuite exposé des animaux normaux et des animaux déficients en IRF5 à la fumée de cigarette pendant plusieurs semaines et comparé l’état de leurs poumons. Chez les souris normales, la fumée entraînait des signes clairs d’emphysème : les cloisons entre alvéoles voisines disparaissaient, laissant de larges espaces surgonflés. En revanche, les souris sans IRF5 étaient largement protégées de ces dommages structurels, bien que la fumée ait tout de même attiré des cellules immunitaires dans les espaces aériens et augmenté de nombreuses molécules inflammatoires. Cela a mis en évidence IRF5 comme un lien crucial entre l’exposition à la fumée et la destruction effective de l’architecture pulmonaire.
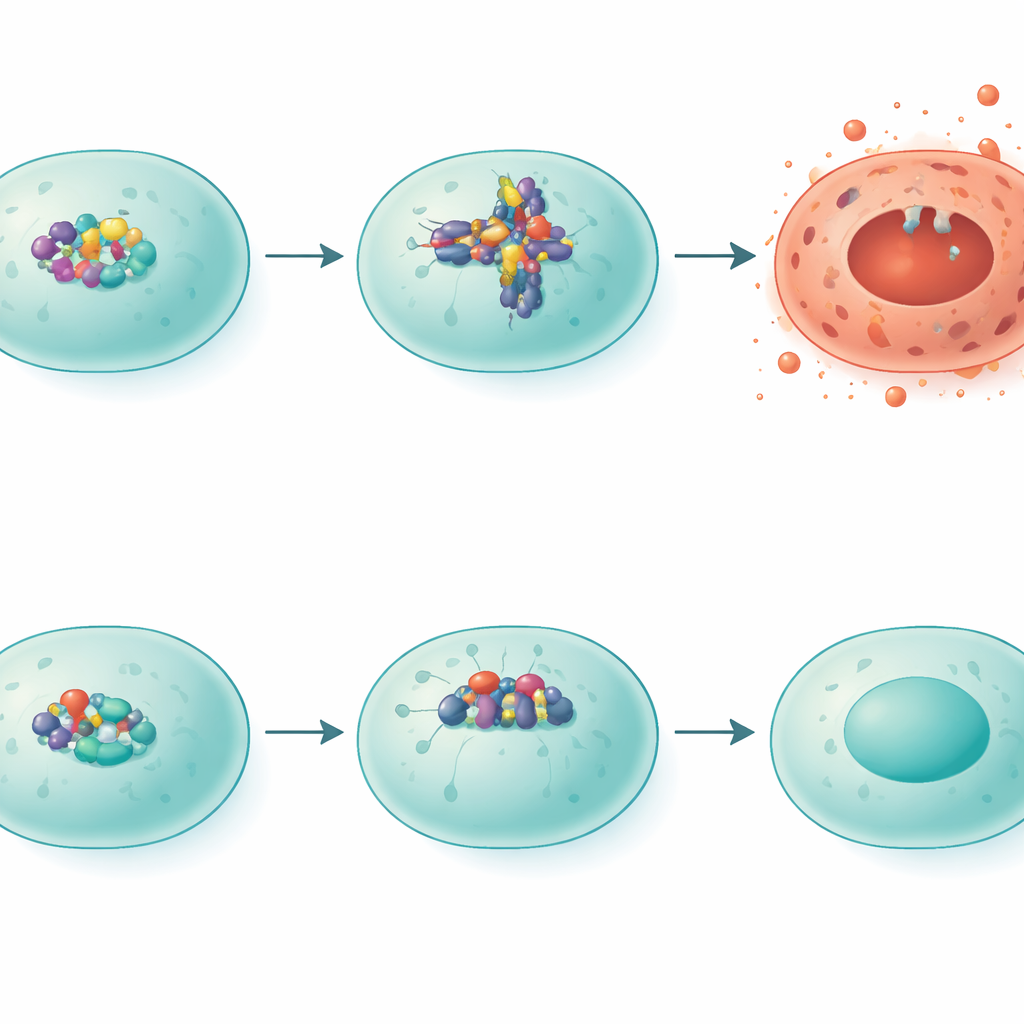
Comment IRF5 pousse les cellules vers une mort enflammée
Les chercheurs se sont ensuite penchés sur une forme particulière de mort cellulaire violente appelée pyroptose, qui perfore les membranes cellulaires et répand des contenus inflammatoires dans le tissu environnant. Un complexe protéique connu sous le nom de NLRP3 est au centre de ce processus. Chez les souris normales exposées à la fumée, les niveaux de NLRP3 augmentaient, et les profils d’une autre protéine, la gasdermine D, correspondaient à un état de type pyroptose. Chez les souris déficientes en IRF5, les niveaux de NLRP3 étaient beaucoup plus bas et la gasdermine D était clivée en formes alternatives associées à des issues moins destructrices. Lorsque l’équipe a artificiellement augmenté IRF5 dans des cellules pulmonaires en culture, les niveaux de NLRP3 ont grimpé, confirmant qu’IRF5 agit comme un commutateur transcriptionnel activant cette voie dommageable.
Des cellules immunitaires protectrices entrent en jeu
IRF5 a également modifié la composition des cellules immunitaires dans le poumon. Chez les souris sans IRF5, on a observé une augmentation marquée d’un sous-ensemble de cellules d’origine sanguine fortement marquées par une molécule de surface appelée Ly6C. Ces cellules Ly6C‑haut comprenaient à la fois des monocytes et des cellules T et apparaissaient en plus grand nombre après exposition à la fumée. Lorsque les scientifiques ont purifié des cellules Ly6C‑haut issues de souris déficientes en IRF5 et les ont transférées à des souris normales exposées à la fumée, les receveurs ont présenté moins de destruction alvéolaire et des niveaux réduits de NLRP3 dans les poumons. Des expériences supplémentaires ont montré qu’IRF5 réprime directement l’activité du gène Ly6C, ce qui suggère que, lorsque IRF5 est présent, moins de ces cellules potentiellement protectrices sont produites ou maintenues.
Les poumons humains confirment le signal
Pour vérifier si ces résultats pouvaient concerner les personnes, les auteurs ont examiné des tissus pulmonaires prélevés chez des patients opérés pour un cancer du poumon. Ils ont comparé des échantillons d’individus ayant une bonne capacité d’échange gazeux à ceux présentant un emphysème significatif. Les niveaux de protéine IRF5 étaient sensiblement plus élevés dans les poumons du groupe emphysème. Bien que cette étude ne soit pas assez vaste pour lier IRF5 précisément à la gravité des symptômes ou aux exacerbations, le schéma concorde avec les observations chez la souris : plus d’IRF5 dans les poumons malades, moins dans les poumons en meilleur état.
Ce que cela pourrait signifier pour de futurs traitements
Pris dans leur ensemble, ces travaux décrivent IRF5 comme un coordinateur central des lésions pulmonaires induites par la fumée. Il active une machine de mort cellulaire centrée sur NLRP3 et détourne les cellules immunitaires des populations Ly6C‑haut qui semblent aider à préserver la structure alvéolaire. Pour les patients, l’implication est simple : un médicament qui atténuerait l’activité d’IRF5 pourrait, en théorie, réduire les formes les plus destructrices d’inflammation sans éteindre complètement le système immunitaire. Bien que de telles thérapies n’existent pas encore pour la MPOC, cette étude fournit une cible moléculaire claire et une voie biologiquement plausible vers des traitements qui feraient plus qu’élargir les voies respiratoires rétrécies — ils pourraient réellement protéger l’armature délicate du poumon.
Citation: Heo, SH., Park, S.Y., Kim, N.H. et al. Interferon regulatory factor 5 involves the pathogenesis of emphysema through NLRP3 and Ly6C expressing cells. Exp Mol Med 58, 425–435 (2026). https://doi.org/10.1038/s12276-025-01632-9
Mots-clés: emphysème, MPOC, inflammation, immunité pulmonaire, mort cellulaire