Clear Sky Science · es
Detección ultrasensible de biomarcadores de la enfermedad de Alzheimer con biosensores fotónicos de cristal de nanopilares
Por qué importa una prueba de sangre simple para la pérdida de memoria
A medida que surgen nuevos fármacos que pueden ralentizar la enfermedad de Alzheimer, los médicos necesitan con urgencia pruebas sencillas que indiquen quién está en riesgo mucho antes de que los síntomas sean evidentes. Hoy en día, confirmar el Alzheimer suele implicar costosas exploraciones cerebrales o punciones lumbares que pocas personas reciben en la atención rutinaria. Este estudio describe un sensor minúsculo basado en la luz que puede detectar moléculas clave relacionadas con el Alzheimer en una gota de sangre a niveles clínicamente relevantes, abriendo potencialmente el camino a pruebas rápidas y de bajo coste que podrían emplearse en clínicas diarias o incluso junto a la cama del paciente.
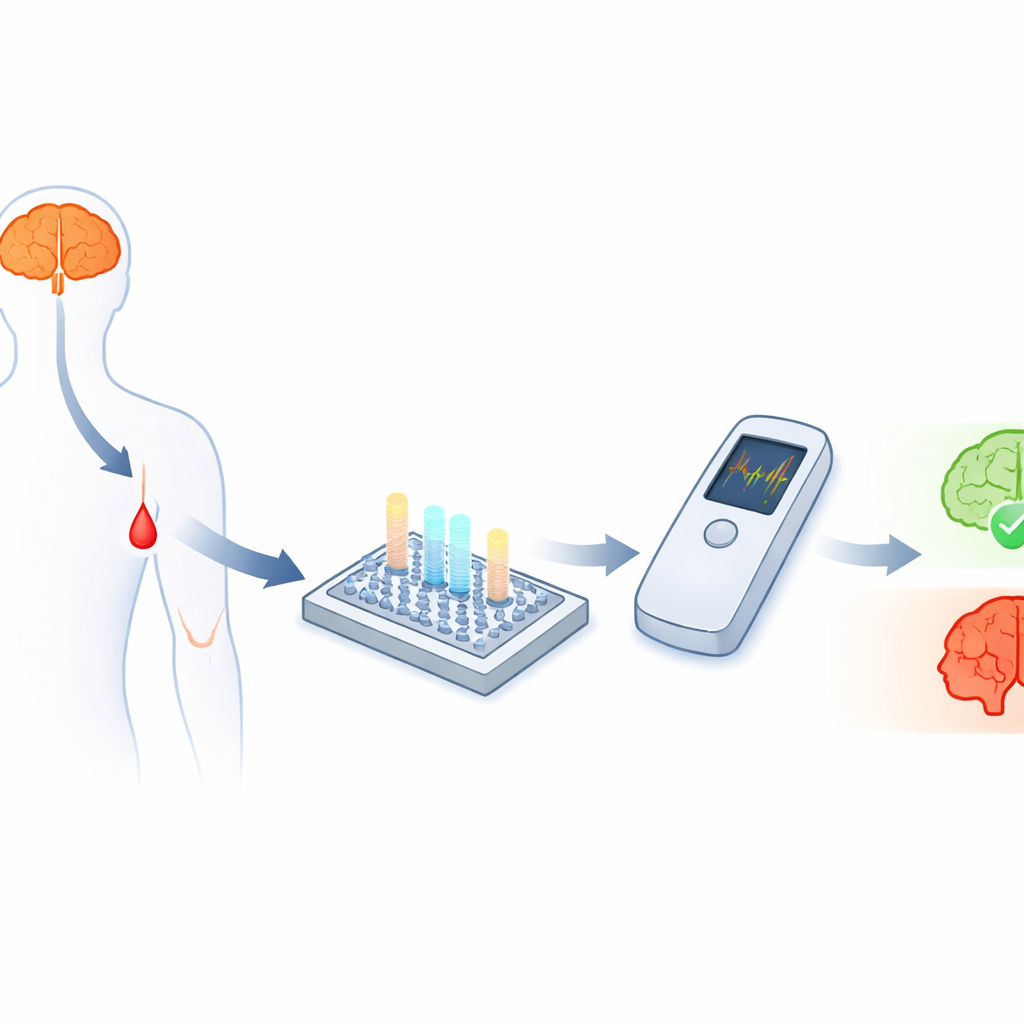
Buscando pistas en la sangre
La enfermedad de Alzheimer está estrechamente ligada a pequeños fragmentos de proteína llamados beta‑amiloide, especialmente dos formas conocidas como Aβ40 y Aβ42. Sus cantidades y, en particular, su relación ofrecen pistas importantes sobre si la enfermedad está presente y cómo progresa. El reto es que estos fragmentos son diminutos y circulan en la sangre a niveles extremadamente bajos —trillonésimas de gramo por mililitro—, lo que dificulta mucho su medición precisa fuera de laboratorios especializados. Aunque los sensores electroquímicos pueden, en principio, detectar concentraciones tan bajas, convertirlos en pruebas resistentes y asequibles para punto de atención que puedan seguir varios biomarcadores a la vez ha resultado difícil.
Guiando la luz a través de pilares diminutos
El equipo abordó este desafío empleando nanofotónica: estructuras que controlan la luz a una escala menor que la longitud de onda de dicha luz. Fabricaron un chip cubierto por una rejilla regular de pares de pilares de silicio, delgados como cabellos, sobre vidrio. Cuando la luz incide en esta superficie con patrón, queda atrapada en un modo resonante especial extremadamente sensible a cambios cerca de las puntas de los pilares, de forma parecida a cómo varía el tono de un diapasón si se añade material. Al ajustar cuidadosamente la distancia entre los pilares de cada par, los investigadores equilibraron a la vez tres propiedades cruciales: la nitidez de la resonancia óptica, la intensidad con que cambia según el entorno y la amplitud de la señal que genera. Este diseño en el “punto óptimo” hace que el chip sea especialmente adecuado para detectar cantidades diminutas de material.
Haciendo visibles moléculas invisibles
Incluso con este diseño optimizado, los marcadores del Alzheimer por sí solos apenas perturbarían la luz. Para amplificar el efecto, los investigadores emplearon una estrategia tipo sándwich con nanopartículas de oro. Primero recubrieron la superficie del sensor con capas de química adhesiva que orientan correctamente anticuerpos especializados de modo que sus sitios de unión queden apuntando hacia el líquido. Estos anticuerpos capturan Aβ40 o Aβ42 de la muestra. A continuación, nanopartículas de oro, cada una decorada con un segundo anticuerpo que reconoce el otro extremo del mismo fragmento amiloide, fluyen sobre el chip. Siempre que hay un fragmento amiloide presente, hace de puente entre la superficie y una partícula de oro, “marcando” su presencia. Dado que el oro perturba fuertemente el entorno óptico local, cada fragmento capturado produce un desplazamiento mucho mayor en la resonancia del sensor que el péptido solo, aumentando la sensibilidad en aproximadamente uno o dos órdenes de magnitud y conservando al mismo tiempo una señal óptica limpia.
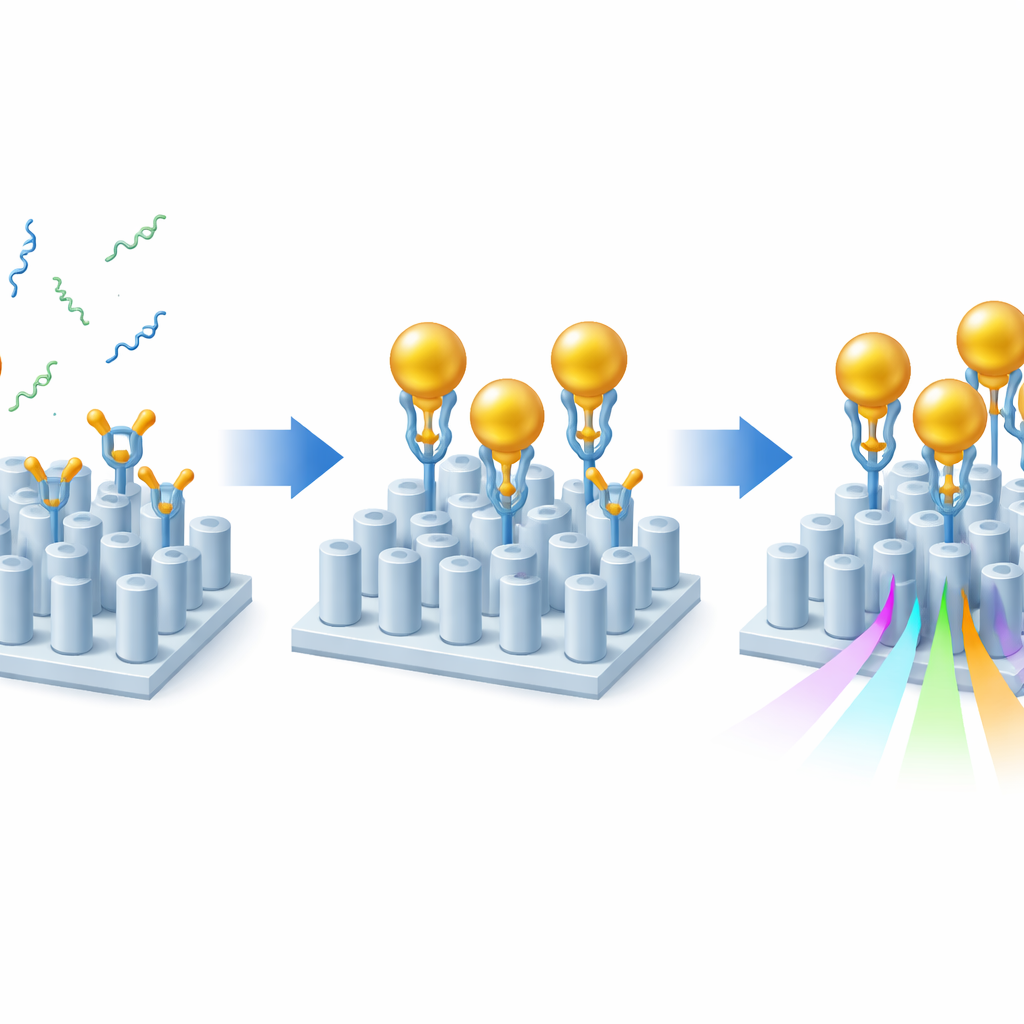
Probando muestras realistas
Para demostrar que el enfoque funciona más allá de simples tampones de laboratorio, el equipo probó su sensor con suero sanguíneo humano. Diluyeron el suero para hacerlo compatible con el manejo microfluídico, manteniendo al mismo tiempo los niveles de amiloide representativos de los hallados en pacientes. De forma importante, pudieron detectar tanto Aβ40 como Aβ42 a 0,2 picogramos por mililitro en este suero diluido —equivalente al nivel clínicamente relevante de 20 picogramos por mililitro en sangre completa. Al disponer diferentes anticuerpos de captura en regiones separadas del mismo chip, midieron simultáneamente ambas formas de amiloide dentro de un único canal diminuto, un paso clave hacia la evaluación de su relación a partir de una sola pequeña muestra. Las señales distinguieron claramente las muestras suplementadas con amiloide adicional de aquellas que contenían solo los niveles de fondo naturales que se encuentran incluso en personas sanas.
Qué podría significar esto para la atención futura
En conjunto, estos avances muestran que un sensor compacto basado en luz, potenciado por nanopartículas de oro, puede alcanzar las sensibilidades necesarias para pruebas de sangre relevantes para el Alzheimer mientras maneja más de un biomarcador a la vez. Aunque se necesita trabajo adicional para convertir esto en un dispositivo comercial robusto y para añadir otros marcadores como formas de la proteína tau, la tecnología subyacente está construida con materiales escalables y puede combinarse con ópticas simples y portátiles. Si se desarrolla por completo, podría permitir a los clínicos monitorizar la salud cerebral usando solo una pequeña muestra de sangre, facilitando en gran medida la detección temprana del Alzheimer y el seguimiento de la eficacia de los tratamientos a lo largo del tiempo.
Cita: Guilherme S. Arruda, Katie Morris, Augusto Martins, Yue Wang, Sian Sloan-Dennison, Duncan Graham, Steven D. Quinn, Emiliano R. Martins, and Thomas F. Krauss, "Ultrasensitive Alzheimer’s disease biomarker detection with nanopillar photonic crystal biosensors," Optica 12, 1587-1596 (2025). https://doi.org/10.1364/OPTICA.566672
Palabras clave: Análisis de sangre para Alzheimer, biosensor nanofotónico, beta amiloide, nanopartículas de oro, diagnóstico precoz