Clear Sky Science · es
Ablación tumoral selectiva mediante láser de femtosegundo resonante con colágeno
Convertir la luz en una herramienta dirigida contra el cáncer
El cáncer de páncreas es uno de los más letales en medicina, en parte porque resulta difícil extirparlo sin dañar el frágil órgano que lo rodea. Este estudio explora una nueva forma de usar impulsos ultrarrápidos de luz infrarroja invisible para quemar tumores pancreáticos con mayor precisión, al dirigirse a un componente estructural que los tumores presentan en exceso. El trabajo sugiere tratamientos futuros que podrían preservar más tejido sano a la vez que atacan con contundencia al cáncer.
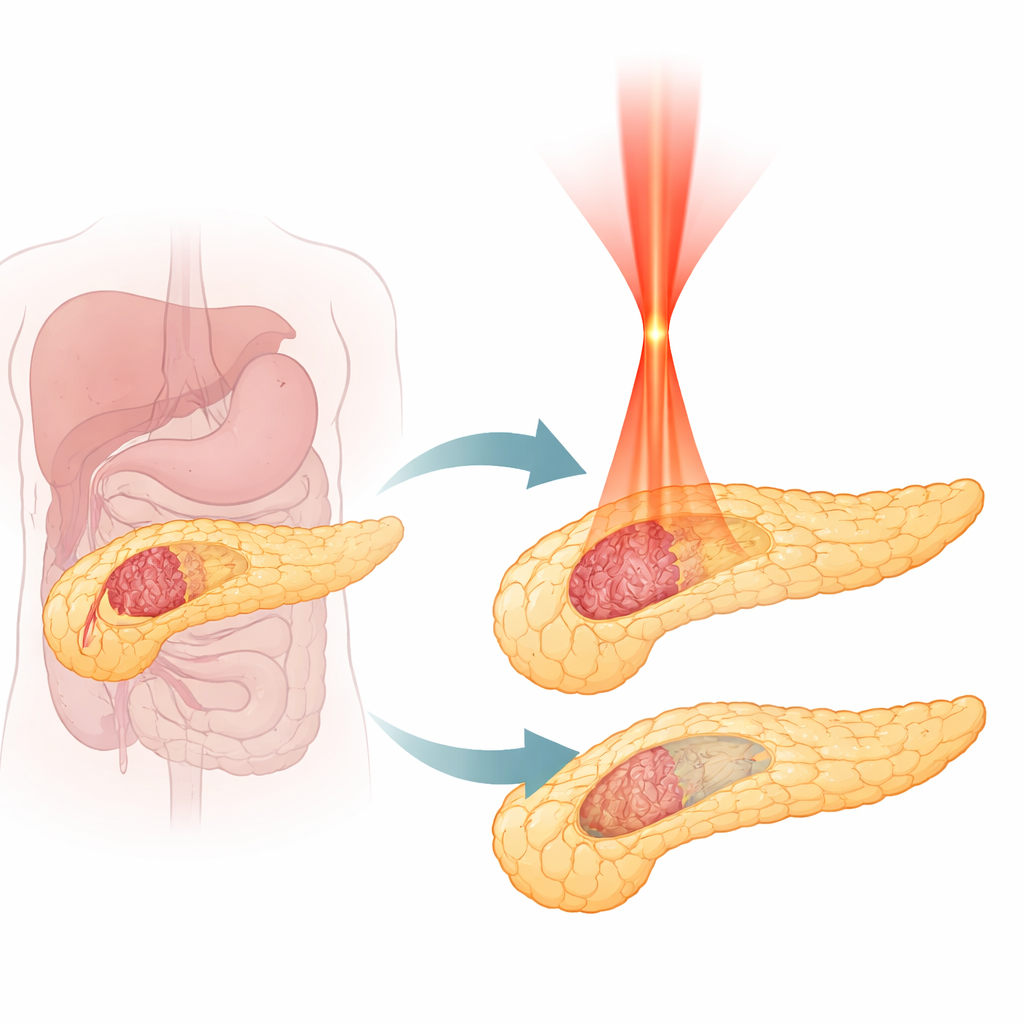
Por qué los tumores pancreáticos son tan difíciles de tratar
El adenocarcinoma ductal pancreático, la forma más común de cáncer de páncreas, crece de manera agresiva y a menudo se detecta tarde. Solo una pequeña fracción de pacientes son candidatos a cirugía, y aun la quimioterapia y la radiación modernas ofrecen beneficios limitados. Los tratamientos basados en calor que destruyen tejido, como la radiofrecuencia, el microondas o la ablación con láser convencional, pueden reducir tumores, pero tienden a quemarlo todo a su paso. Dado que el páncreas está próximo a vasos sanguíneos vitales y estructuras digestivas delicadas, ampliar la zona de tratamiento entraña riesgos graves. Por ello los médicos necesitan un método que distinga entre tumor y páncreas normal durante la destrucción, en lugar de cocinar una zona amplia.
Encontrar un punto débil oculto en el tejido tumoral
Los autores se centraron en una diferencia física clave entre los tumores pancreáticos y el páncreas sano: los tumores están repletos de material fibroso rígido rico en colágeno, mientras que el tejido normal es más blando y laxо. Empleando tinciones tisulares estándar y microscopía electrónica en muestras quirúrgicas, mostraron que el tejido canceroso contiene haces densos de fibras de colágeno, mientras que el páncreas sano adyacente tiene muchas menos. Luego usaron espectroscopía infrarroja para medir cuánto absorben estos tejidos diferentes colores de luz en el infrarrojo medio. Ambos tejidos absorben en longitudes de onda similares, pero los tumores muestran un pico mucho más fuerte cerca de 6,1 micrómetros, que corresponde a las vibraciones del colágeno. Esto sugería que un láser sintonizado precisamente a esa longitud de onda podría calentar y descomponer el tejido tumoral con mayor eficiencia que el páncreas normal.
Construir un láser que “escuche” al colágeno
Para probar esta idea, el equipo construyó un potente láser de infrarrojo medio que emite impulsos ultra-cortos —que duran solo unos pocos cientos de cuatrillones de segundo— centrados en 6,1 micrómetros. Estos impulsos de “femtosegundo” limitan la propagación indeseada del calor, de forma similar a una serie de pequeños y controlados destellos eléctricos. El sistema convierte la luz de un láser industrial de alta potencia a la longitud de onda deseada usando cristales especiales y puede entregar más de un vatio de potencia media; esto es suficiente para la ablación práctica de tejido. Los investigadores también desarrollaron una fibra hueca de vidrio que puede guiar esta luz a lo largo de un camino flexible, un paso importante hacia la capacidad de introducir el láser a través de una aguja delgada en el cuerpo para procedimientos mínimamente invasivos.
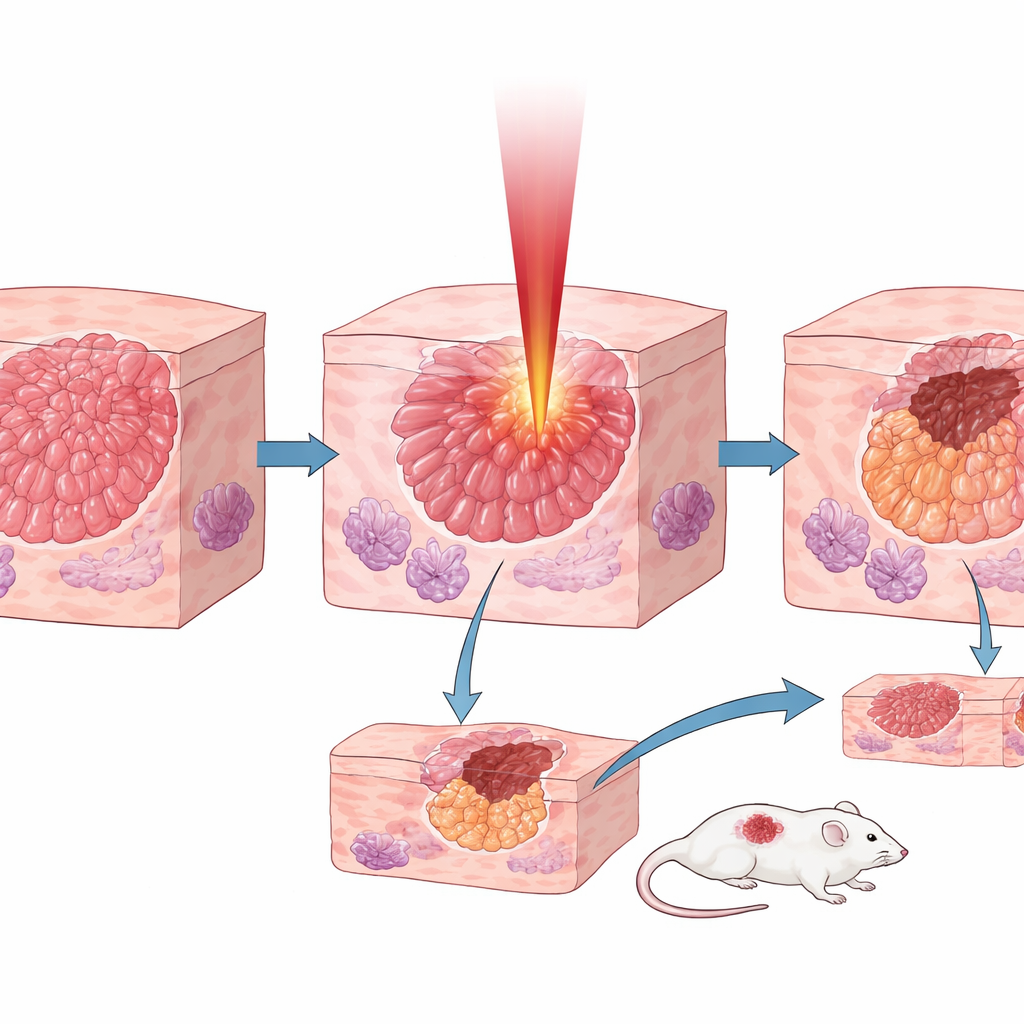
Probar la selectividad en células, ratones y tejido humano
En cultivos celulares de dos líneas de cáncer pancreático, el láser de 6,1 micrómetros fue mucho más letal que los láseres a 1 o 3 micrómetros, reduciendo drásticamente la supervivencia celular en segundos o minutos de exposición. En ratones con tumores pancreáticos subcutáneos se compararon tres longitudes de onda. Aunque el haz de 1 micrómetro llevaba mucha mayor potencia, solo eliminó capas poco profundas del tumor. El láser sintonizado al colágeno de 6,1 micrómetros alcanzó profundidades de ablación cinco a diez veces mayores y frenó el crecimiento tumoral de forma tan marcada que los tumores tratados quedaron aproximadamente en una octava parte del tamaño de los de animales no tratados. Lo más importante, cuando el equipo aplicó el láser de 6,1 micrómetros a muestras humanas de tumor y páncreas sano adyacente, los cortes en el tumor fueron dos a tres veces más profundos que en el tejido sano bajo las mismas condiciones, lo que revela una selectividad real. En contraste, al probar otro tipo de tumor hepático que no acumula colágeno extra, la ventaja desapareció en gran medida, reforzando el papel central del colágeno. Finalmente, demostraron que la fibra hueca podía entregar el mismo efecto selectivo, respaldando tratamientos futuros basados en aguja.
Qué podría significar esto para la atención oncológica futura
El estudio demuestra que ráfagas cuidadosamente sintonizadas de luz en el infrarrojo medio pueden explotar una diferencia material entre tumores y tejido sano para lograr una destrucción más selectiva. Al dirigirse a regiones ricas en colágeno, el láser de femtosegundo de 6,1 micrómetros corta más profundamente el cáncer de páncreas mientras preserva más del órgano circundante. Aunque el trabajo aún está en fase experimental y se necesitan más pruebas en modelos realistas y entornos clínicos, apunta hacia una nueva clase de procedimientos guiados por imagen y entregados por fibra que podrían tratar no solo tumores pancreáticos sino también otros cánceres ricos en colágeno con mayor precisión y menos efectos secundarios.
Cita: Dunxiang Zhang, Xing Huang, Xuemei Yang, Ning Xia, Kan Tian, Jinmiao Guo, Maoxing Xiang, Linzhen He, Zhizhuo Fu, Ang Deng, Han Wu, Yuxi Wang, Wonkeun Chang, Bole Tian, Junjie Xiong, Qi Jie Wang, Anderson S. L. Gomes, and Houkun Liang, "Selective tumor ablation via femtosecond laser resonant with collagen," Optica 12, 1578-1586 (2025). https://doi.org/10.1364/OPTICA.561337
Palabras clave: cáncer de páncreas, ablación con láser, colágeno, infrarrojo medio, cirugía mínimamente invasiva