Clear Sky Science · es
El origen en la estructura cuaternaria de la fibrilación de la hemoglobina falciforme: un estudio por dinámica molecular
Por qué importa esta historia sanguínea
La enfermedad de células falciformes comienza con un cambio minúsculo en una proteína sanguínea, pero puede alterar la forma de los glóbulos rojos, obstruir vasos y causar dolor de por vida. Este estudio examina, desde una perspectiva física detallada, cómo ese único cambio hace que la hemoglobina se apile en fibras rígidas dentro de la célula. Mediante simulaciones informáticas avanzadas, los autores conectan detalles atómicos con problemas a escala celular, ofreciendo pistas nuevas sobre cómo futuros fármacos podrían evitar que la hemoglobina atasque nuestro flujo sanguíneo.
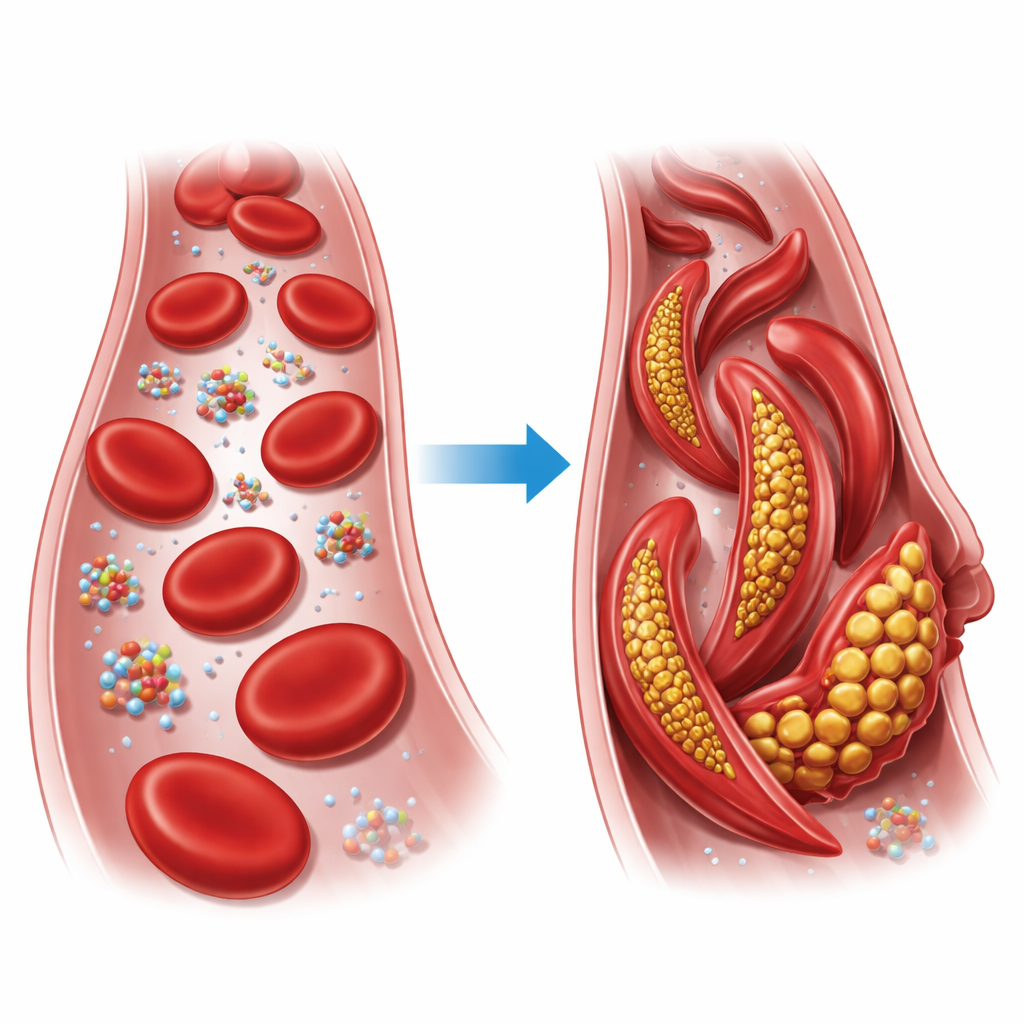
Un intercambio minúsculo con grandes consecuencias
La hemoglobina es la proteína transportadora de oxígeno que llena nuestros glóbulos rojos. Cada unidad de hemoglobina está formada por cuatro cadenas que pueden disponerse en dos conformaciones generales, conocidas como el estado relajado (R) y el estado tenso (T). En la enfermedad falciforme, se sustituye un solo componente en una de esas cadenas: un glutamato cargado es reemplazado por una valina hidrofóbica en la posición seis de la cadena beta. En condiciones de bajo oxígeno, esta versión alterada, llamada hemoglobina falciforme, se enlaza formando largas fibras que deforman los glóbulos rojos —normalmente redondos— en formas rígidas tipo hoz, que pueden obstruir vasos pequeños y privar a los tejidos de oxígeno.
Siguiendo la forma cambiante de la hemoglobina
Los autores se centran en cómo las unidades completas de hemoglobina rotan y se empaquetan entre sí en una fibra. Siguen este cambio de forma a gran escala mediante un único ángulo que mide cómo se tuercen dos mitades de la proteína entre sí. Usando simulaciones de dinámica molecular —experimentos virtuales que calculan cómo se mueven los átomos a lo largo del tiempo en agua y sal— empujan suavemente ese ángulo a lo largo de un amplio rango y calculan cuánto cuesta energéticamente cada conformación. Encuentran que tanto la hemoglobina normal como la falciforme pueden explorar muchas de estas conformaciones a temperatura corporal. La hemoglobina falciforme muestra un ligero ángulo preferido, pero esas preferencias por sí solas no bastan para explicar por qué solo la forma falciforme forma fibras estables.
Por qué las fibras falciformes se pegan y las normales se deshacen
Para profundizar en la formación de fibras, el estudio mide cuánto se atraen entre sí las unidades vecinas de hemoglobina a lo largo y a través de la fibra. El equipo calcula la energía cohesiva —la atracción neta que mantiene unidas las unidades— para muchas conformaciones globales. En la hemoglobina falciforme, esta energía cohesiva permanece negativa (es decir, atractiva) en todo el rango de conformaciones que probaron, por lo que las fibras son estables y no se deshacen con facilidad. En contraste, en la hemoglobina normal, algunas conformaciones presentan energía cohesiva positiva, lo que hace que las fibras en esos ángulos sean inestables y propensas a romperse de forma espontánea. Una diferencia clave es cómo los grupos laterales de la valina mutada se encajan en las proteínas vecinas: en la hemoglobina falciforme, estos parches hidrofóbicos forman contactos robustos tanto lateralmente como a lo largo del eje de la fibra, promoviendo directamente el crecimiento de la fibra.
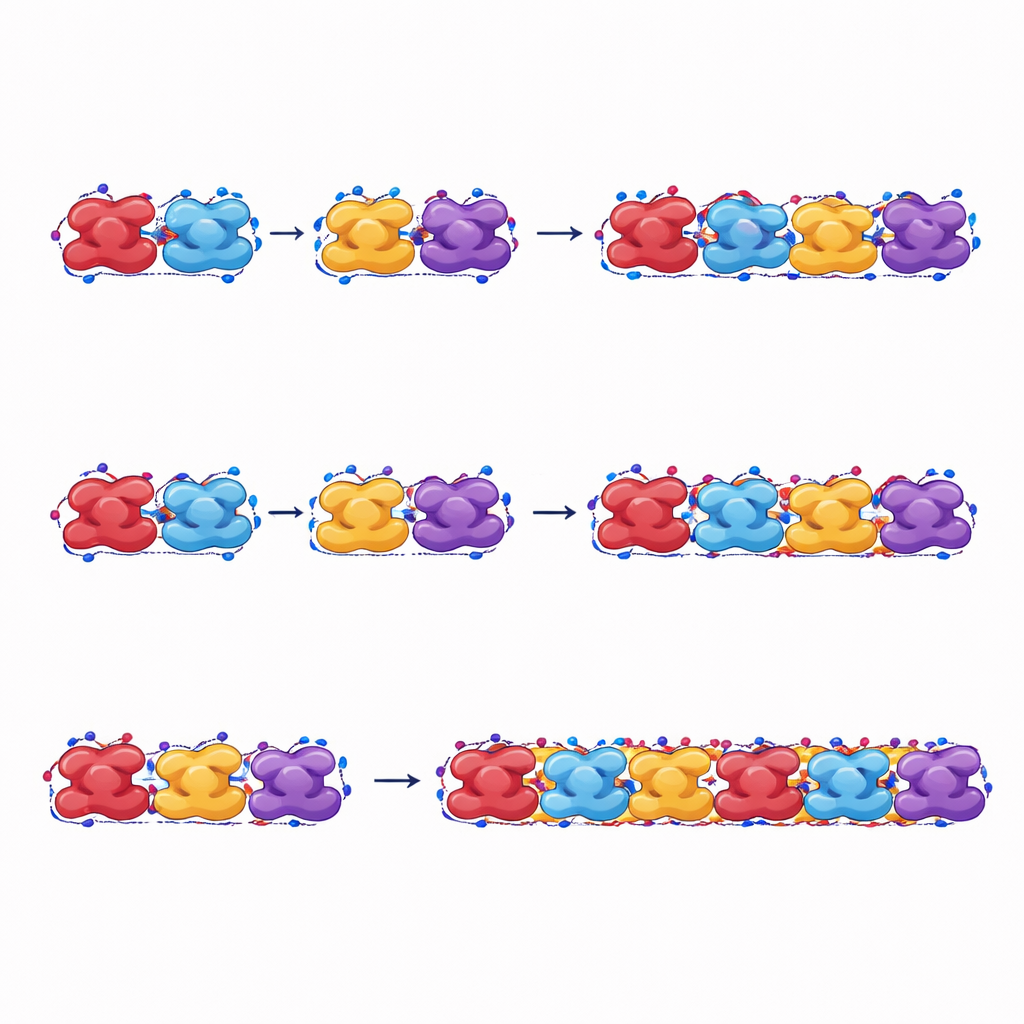
Cómo soportan carga y se rompen estas fibras
Los autores también estiran sus fibras simuladas para imitar el estrés mecánico. Cuando se tiran a lo largo de su longitud, las fibras hechas de hemoglobina falciforme soportan mayores fuerzas y deformaciones y disipan más energía antes de romperse que las hechas de hemoglobina normal. Incluso la forma relajada de las fibras falciformes, que no es la que aparece inicialmente, puede mantener la cadena mediante cambios plásticos en la forma, ayudando a que la fibra permanezca intacta una vez formada. Por el contrario, las fibras de hemoglobina normal se separan con mayor facilidad entre unidades vecinas y absorben menos energía antes de fallar, lo que confirma que son menos estables bajo esfuerzo.
Pistas para futuros tratamientos y nuevos materiales
En conjunto, las simulaciones muestran que un único cambio de aminoácido remodela la forma en que las unidades de hemoglobina se encuentran, torciendo el ensamblaje global hacia ángulos que favorecen una atracción fuerte, especialmente en el estado tenso. Esta combinación de geometría y adherencia permite que la hemoglobina falciforme forme fibras largas y rígidas que resisten tanto el movimiento térmico como el tirón mecánico, lo que en última instancia deforma los glóbulos rojos y bloquea el flujo sanguíneo. Al señalar características específicas del arreglo global de la proteína que controlan la estabilidad de las fibras, el trabajo sugiere que fármacos antisickle eficaces podrían actuar empujando la hemoglobina hacia conformaciones en las que las fibras resulten energéticamente desfavorables y mecánicamente frágiles —convirtiendo un atasco molecular mortal de nuevo en un flujo sanguíneo libre.
Cita: Jiang, M., Qin, Z. The quaternary structure origin of the fibrillation of sickle hemoglobin: a molecular dynamics study. npj Soft Matter 2, 7 (2026). https://doi.org/10.1038/s44431-026-00019-8
Palabras clave: enfermedad de células falciformes, fibras de hemoglobina, aglomeración de proteínas, dinámica molecular, trastornos sanguíneos