Clear Sky Science · es
Dinamina optimiza las interacciones proteína-membrana para la fisión
Cómo las células pellizcan ordenadamente sus propias membranas
Cada segundo, tus células están ocupadas desprendiendo pequeñas burbujas de membrana para transportar carga, remodelar compartimentos internos y combatir virus. Este acto aparentemente simple de cortar un tubo membranoso estrecho en dos piezas resulta ser sorprendentemente difícil desde el punto de vista físico. Este artículo plantea una pregunta engañosamente básica: ¿cómo hace una proteína llamada dinamina para que el corte de membrana sea posible y fiable, y qué rasgos de la proteína son realmente esenciales para la tarea?
Los pellizcadores celulares en acción
La dinamina es una máquina molecular que forma un collar alrededor de tubos membranosos delgados y se aprieta como una soga para ayudar a que se rompan. Tales eventos de fisión sustentan procesos como la endocitosis, en los que las células incorporan material, así como la división de estructuras internas como las mitocondrias. Si no interviene nada, un tubo de membrana se resiste con fuerza a romperse, porque primero debe comprimirse hasta casi el espesor de la propia membrana y atravesar un estado intermedio inestable. Esta barrera energética es mucho mayor que la energía de agitación aleatoria disponible dentro de una célula, por lo que proteínas especializadas de fisión como la dinamina son esenciales.
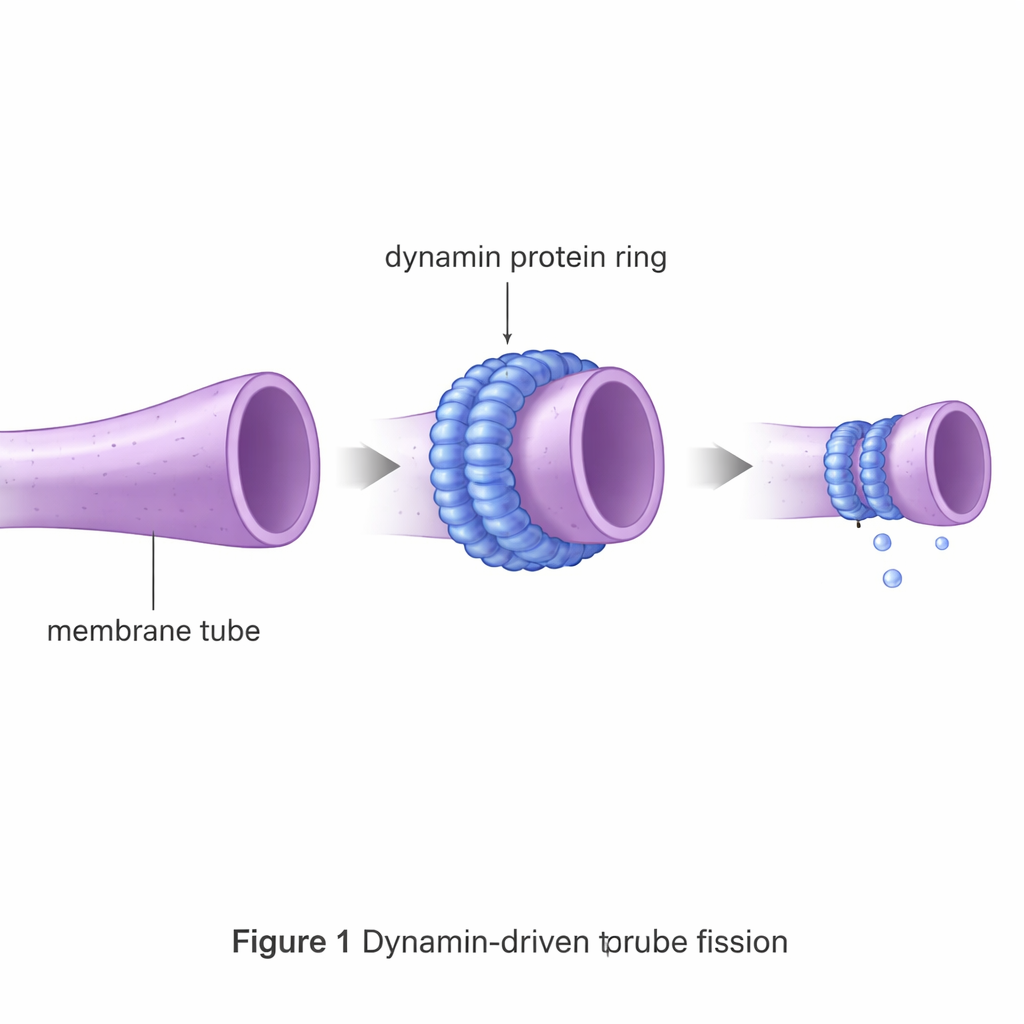
Usando membranas virtuales para probar diseños de proteínas
Observar directamente el instante crítico en que un tubo se parte es extremadamente difícil en experimentos: la imaginería rápida carece de detalle molecular y los métodos de alta resolución congelan el sistema en el tiempo. Para salvar esta brecha, los autores usan una potente herramienta teórica llamada teoría del campo autoconsistente. En lugar de seguir cada átomo, describen los lípidos y el disolvente como cadenas flexibles que sienten campos que varían suavemente. Las proteínas se introducen no como estructuras atómicas completas sino como potenciales externos con forma de toro que o bien simplemente excluyen espacio, se adhieren a la superficie de la membrana, o se insertan en la monocapa externa. Con este marco, pueden calcular tanto las formas resultantes de la membrana como el costo energético completo de pasar de un tubo intacto al intermedio de fisión.
Qué tipo de agarre ayuda a que un tubo se rompa
El equipo varía sistemáticamente cómo una proteína tipo dinamina interactúa con la membrana. Algunas proteínas modelo sólo ocupan la superficie, actuando como un puño rígido; otras son ligeramente o fuertemente adhesivas a los grupos cabeza externos; otras imitan el dominio PH real de la dinamina al insertar partes hidrofóbicas en la monocapa externa y «abrir» los grupos cabeza a un lado. Para cada caso examinan tres magnitudes relacionadas: qué tan fuertemente la proteína se adhiere a un tubo no constreñido, cuánto induce de curvatura y constricción mientras está unida, y cuán alta sigue siendo la barrera energética para que el tubo pase a un estado de hemifisión donde se han fusionado las capas internas. Encuentran que el simple apretón reduce la barrera pero no lo suficiente para explicar una fisión eficiente, y que una adhesión superficial fuerte puede en realidad dificultar la ruptura porque la membrana debe primero despegarse de la proteína para completar el colapso.
Por qué una inserción superficial vence al simple apriete
El diseño más eficaz es aquel en el que la proteína se inserta parcialmente entre los grupos cabeza lipídicos y tira de sus colas hacia arriba, creando una flexión local con forma de cheurón en la membrana. Este «splay» desplaza el punto más estrecho del tubo ligeramente al lado del anillo proteico en vez de directamente bajo él. Como resultado, la membrana puede completar el colapso crítico hacia el intermedio de hemifisión sin desprenderse de la proteína, y la barrera energética global cae en más de un orden de magnitud respecto a un tubo desnudo. Cuando los autores permiten que los parámetros de la proteína se ajusten automáticamente para minimizar esta barrera, la solución óptima coincide estrechamente con el tamaño y la acción del dominio PH de la dinamina: un parche hidrofóbico de anchura moderada que se inserta de forma superficial, no una superficie amplia y excesivamente adhesiva que arrancaría lípidos de la solución.
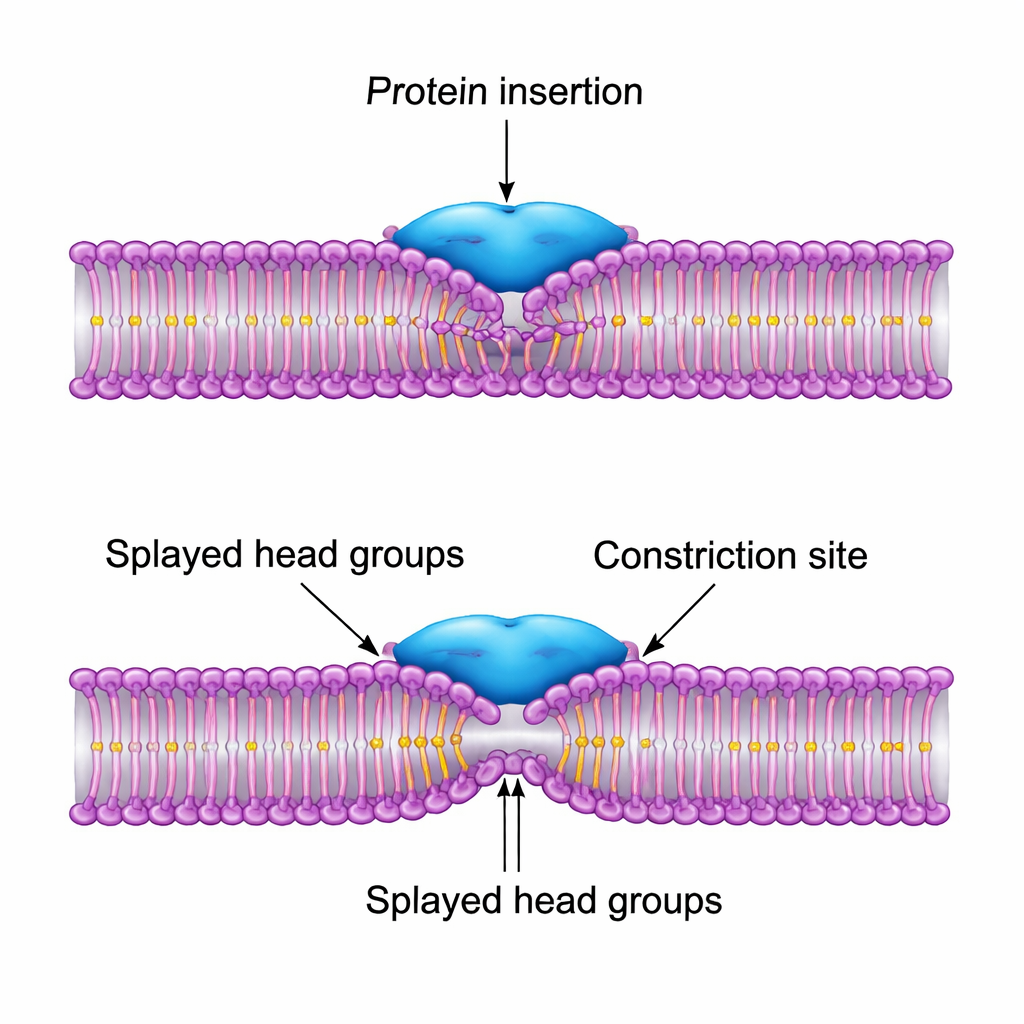
Reglas de diseño para la naturaleza y la nanotecnología
Para un público no especializado, el mensaje clave es que la dinamina no funciona sólo apretando un cinturón alrededor de la membrana, sino afinando cuidadosamente cómo y dónde sujeta la monocapa externa. Una cuña poco profunda que separa los lípidos externos y concentra la curvatura justo al lado de la proteína resulta mucho más efectiva que la constricción por fuerza bruta o la adhesión fuerte. Estos resultados ayudan a explicar por qué la evolución ha favorecido la arquitectura particular de la dinamina y sugieren principios de diseño para proteínas sintéticas o fármacos que necesiten cortar o remodelar membranas de forma controlada en medicina y nanotecnología.
Cita: Spencer, R.K.W., Müller, M. Dynamin optimizes protein-membrane interactions for fission. npj Soft Matter 2, 6 (2026). https://doi.org/10.1038/s44431-026-00018-9
Palabras clave: fisión de membrana, dinamina, interacciones proteína–membrana, curvatura de membrana, teoría del campo autoconsistente