Clear Sky Science · es
Acortando la brecha computacional-experimental: aprovechando un modelo grande de lenguaje para priorizar terapias contra el Alzheimer mediante la comparación de modelos de aprendizaje
Por qué esto importa para familias y pacientes
La enfermedad de Alzheimer roba la memoria, la independencia y la calidad de vida, y sin embargo siguen siendo escasos los tratamientos realmente efectivos. Este estudio explora una forma más rápida de encontrar nuevos tratamientos usando medicamentos ya existentes, combinando modelos computacionales potentes con un modelo grande de lenguaje—el mismo tipo de IA que hoy aparece en chatbots cotidianos—para cribar enormes cantidades de datos médicos y artículos científicos. El objetivo es reducir una larga lista de fármacos posibles hasta un conjunto pequeño y realista que los científicos y médicos puedan probar en pacientes.
Reutilizar medicamentos antiguos con un propósito nuevo
Desarrollar un fármaco completamente nuevo desde cero puede llevar más de una década y costar miles de millones de dólares, sin garantía de éxito. Una alternativa es la “reorientación de fármacos”, que busca nuevos usos para medicamentos ya aprobados para otras afecciones, como la enfermedad de Parkinson o la depresión. Dado que estos fármacos tienen perfiles de seguridad conocidos, a menudo pueden avanzar más rápido hacia ensayos clínicos en Alzheimer. Pero los métodos computacionales modernos que examinan bases de datos biológicas y la literatura médica ahora generan listas enormes de candidatos—mucho más de los que los investigadores pueden evaluar manualmente—creando un nuevo cuello de botella en el proceso.
Reunir varios modelos inteligentes
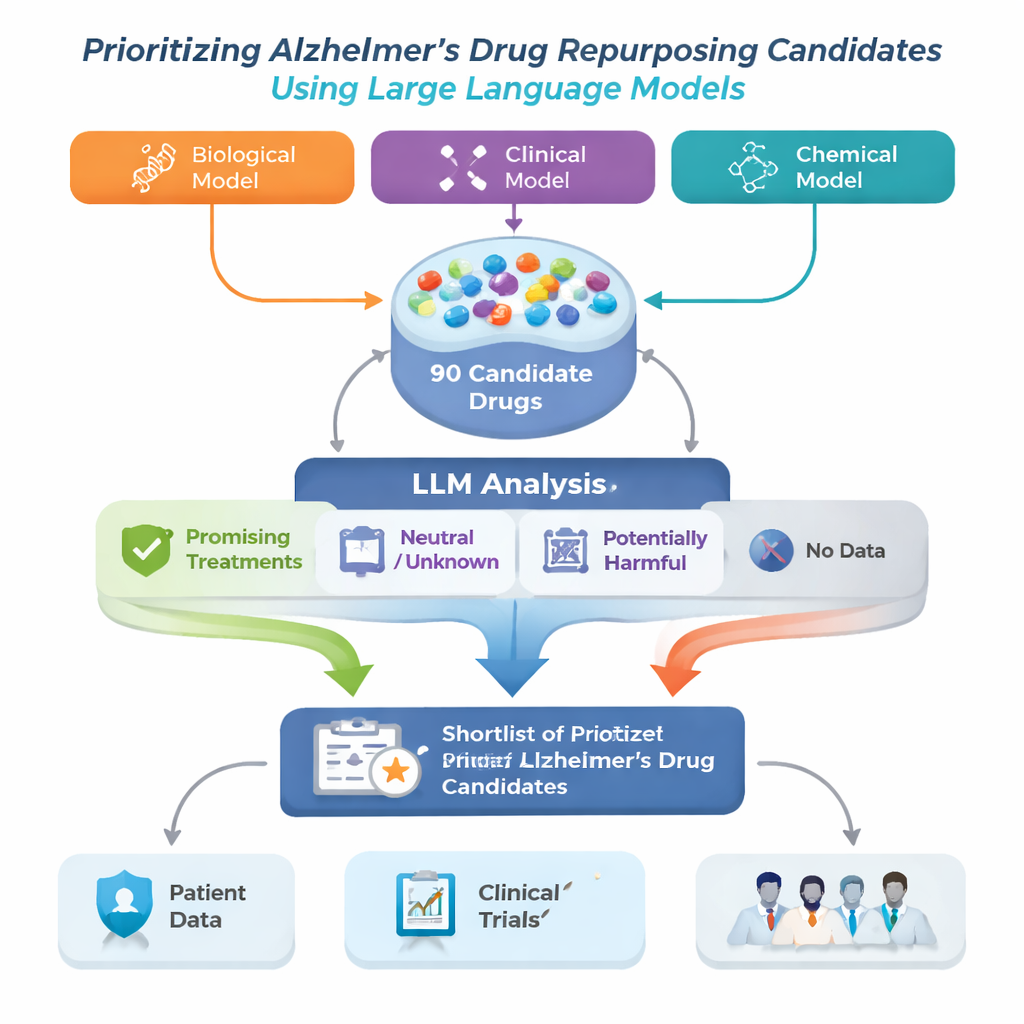
El equipo de investigación abordó este problema construyendo un marco de reorientación de fármacos para Alzheimer que parte de tres modelos computacionales avanzados diferentes. Cada modelo examina un gran “mapa” biomédico llamado grafo de conocimiento, que enlaza enfermedades, fármacos, genes y otros conceptos médicos, y sugiere fármacos que podrían ayudar en el Alzheimer. Como cada modelo detecta patrones de manera distinta, sus listas no se solapan completamente. Los autores combinaron las 30 principales sugerencias de cada modelo en una única cartera de 90 fármacos candidatos, y luego emplearon un modelo grande de lenguaje (LLM) para desempeñar el papel de revisor automatizado pero cauteloso, leyendo estudios publicados sobre cada fármaco y valorando si la evidencia parecía útil, neutral o perjudicial para el Alzheimer.
Cómo la IA lee la literatura médica
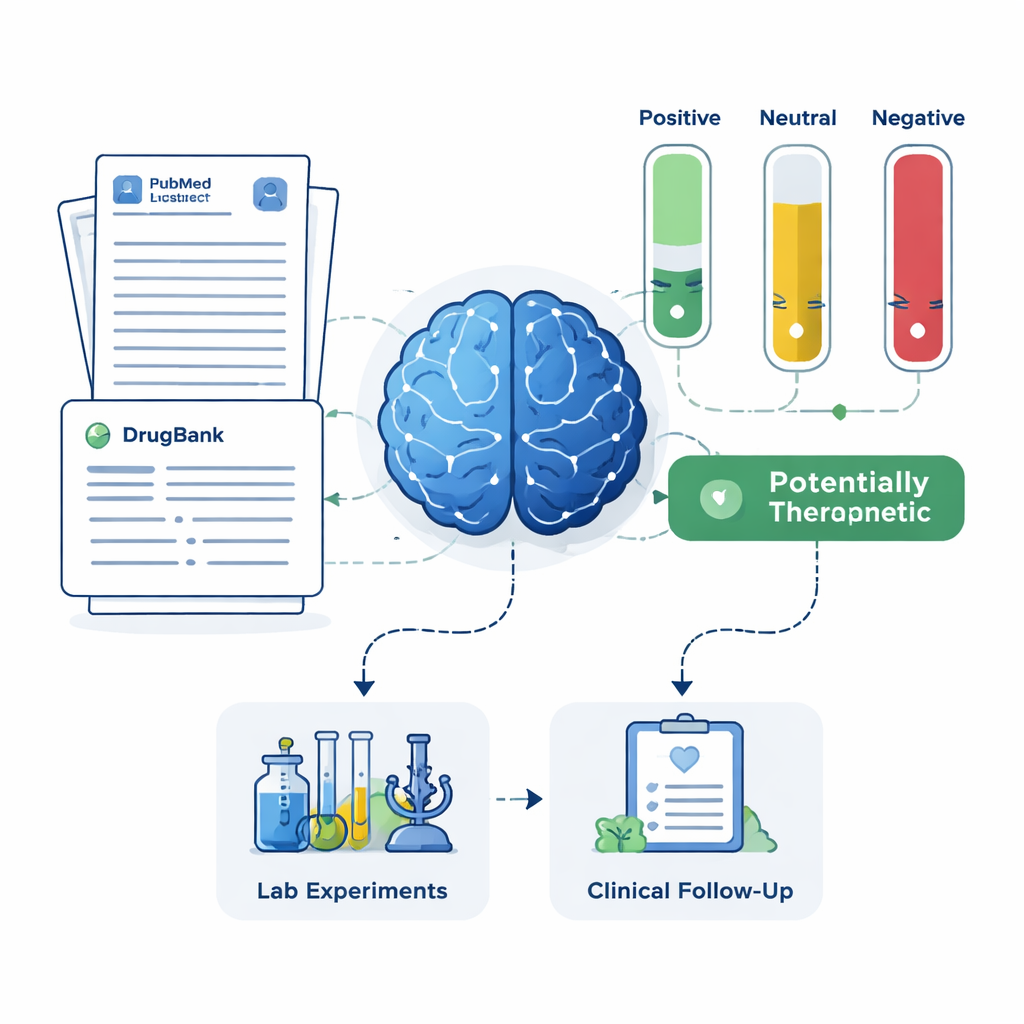
Para cada fármaco candidato, el sistema recuperó hasta 200 resúmenes científicos de PubMed además de descripciones detalladas de fármacos procedentes de una base de datos farmacéutica. Se instruyó al LLM para que basara su juicio únicamente en el texto que se le mostraba y para etiquetar cada resumen como positivo, neutral o negativo respecto al tratamiento del Alzheimer. Estas etiquetas se convirtieron luego en puntuaciones simples: la proporción de resúmenes que eran positivos, neutrales o negativos. Usando dos conjuntos de reglas—una más estricta que requería evidencia positiva clara y otra más indulgente que marcaba cualquier indicio de beneficio—el marco clasificó los fármacos en cuatro grupos: tratamientos prometedores, potencialmente perjudiciales, poco claros o neutrales, y fármacos sin artículos relacionados con Alzheimer en absoluto. Este último grupo, aunque poco estudiado, puede contener oportunidades especialmente novedosas.
Comprobación con pacientes reales y ensayos clínicos
Para ver si la lista corta generada por la IA tenía sentido en el mundo real, el equipo comparó sus resultados con dos fuentes independientes: un gran registro de pacientes con Alzheimer y los registros de ensayos clínicos registrados. El marco recuperó con éxito la memantina, un fármaco existente para Alzheimer con señales protectoras sólidas en datos de pacientes y un extenso historial de ensayos, como un candidato de alta prioridad. También destacó fármacos como magnesio, minociclina, pimavanserina, testosterona y doxiciclina, que tienen distintos niveles de investigación de apoyo pero habían sido considerados prometedores por clínicos expertos. Al mismo tiempo, el sistema identificó fármacos cuya literatura sugería posible daño o falta de beneficio, recomendando que estos se priorizaran menos o se investigaran por sus efectos adversos en lugar de como tratamientos.
De las predicciones computacionales a los siguientes pasos prácticos
En términos cotidianos, este marco actúa como un asistente de investigación ultrarrápido y cuidadoso que lee miles de artículos, coteja patrones en grandes bases de datos médicas y entrega a los expertos humanos una lista mucho más corta y mejor organizada de candidatos a fármacos para Alzheimer en los que concentrarse. El estudio muestra que, combinando distintos tipos de IA—modelos basados en grafos para generar ideas y un modelo de lenguaje para juzgar la evidencia—los investigadores pueden encontrar más rápido tanto fármacos bien respaldados como opciones nuevas e intrigantes para su ensayo. Si bien este enfoque no cura el Alzheimer por sí solo, ofrece una forma poderosa de conectar las ideas generadas por ordenador con el trabajo duro de los experimentos de laboratorio y los ensayos clínicos, acelerando potencialmente el camino hacia tratamientos más efectivos.
Cita: Li, M., Niu, S., Xu, Y. et al. Bridging the computational-experimental gap: leveraging large language model to prioritize Alzheimer’s therapeutics based on comparison of learning models. npj Health Syst. 3, 20 (2026). https://doi.org/10.1038/s44401-026-00074-3
Palabras clave: Enfermedad de Alzheimer, reorientación de fármacos, inteligencia artificial, modelos grandes de lenguaje, grafos de conocimiento