Clear Sky Science · es
La mutación APP E590D aumenta la generación de péptidos Aβ y Aη y agrava la tauopatía
Por qué importa esta mutación rara
La enfermedad de Alzheimer suele concebirse como la acumulación lenta de dos proteínas perjudiciales, la amiloide y la tau, en el cerebro. La mayoría de las personas desarrollan Alzheimer sin una causa única y clara, pero algunas familias portan cambios genéticos raros que pueden inclinar el equilibrio de forma drástica. Este artículo examina uno de esos cambios poco comunes en el gen de la proteína precursora de amiloide (APP) y muestra cómo puede potenciar la producción de fragmentos proteicos tóxicos y empeorar el proceso de enmarañamiento conocido como tauopatía. Comprender este caso raro ofrece pistas que pueden aplicarse de forma mucho más amplia a cómo comienza y luego acelera el Alzheimer.
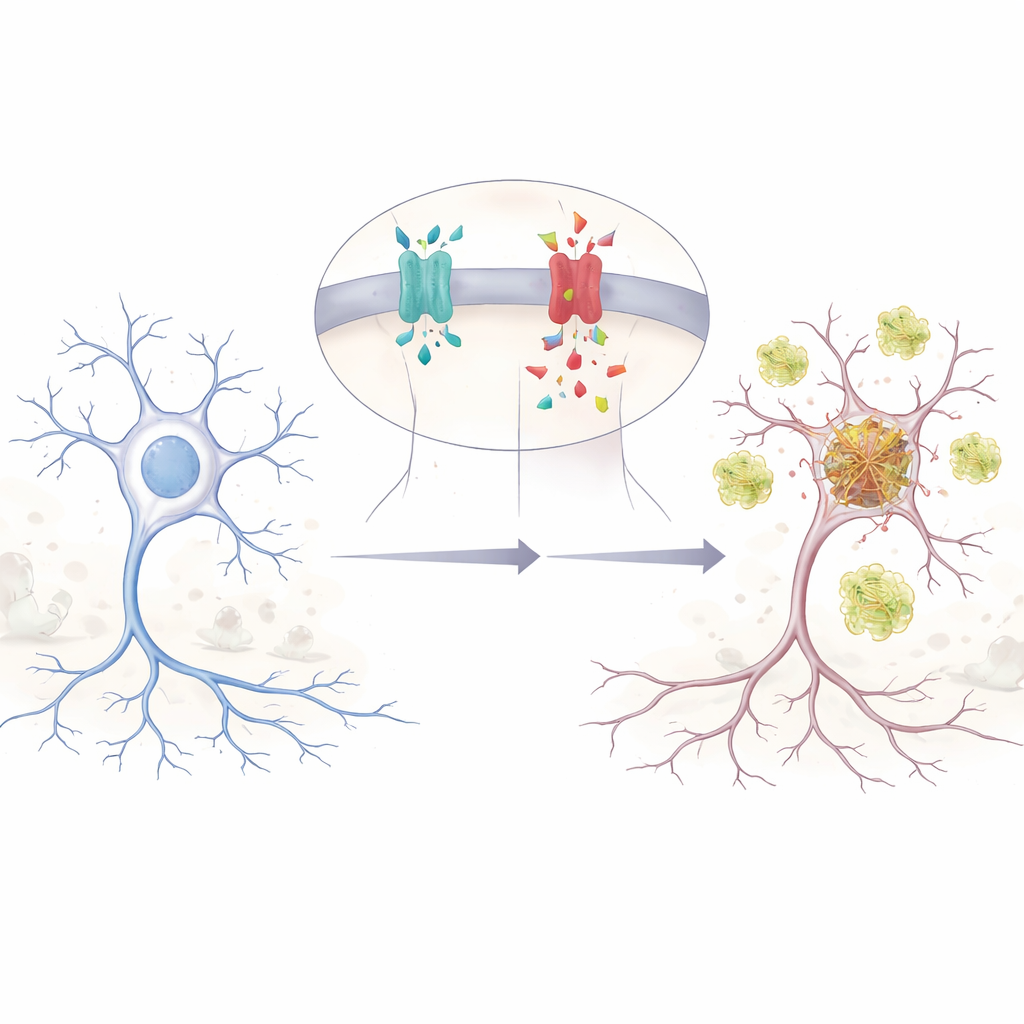
Un pequeño cambio genético con grandes efectos
Los autores se centran en un cambio de una sola letra en el gen APP, denominado E590D en la forma cerebral principal de APP. Esta mutación se ha comunicado en solo dos personas, ambas con Alzheimer confirmado a edades relativamente jóvenes y con problemas poco habituales de memoria y conducta muy tempranos. Debido a su extrema rareza, los científicos no estaban seguros de si realmente causa la enfermedad o si era un mero observador inocuo. Para averiguarlo, el equipo recreó la mutación en células humanas y en neuronas de ratón, y luego siguió cómo APP se fragmentaba en sus múltiples trozos. Descubrieron que la APP mutante produce mucho más beta-amiloide (Aβ), el péptido pegajoso vinculado desde hace tiempo al Alzheimer, que la APP normal cuando se comparan los niveles de forma justa.
Dos péptidos tóxicos en lugar de uno
APP puede cortarse de varias maneras, como un tronco que se rebana en distintos puntos. La vía clásica del Alzheimer genera Aβ, pero otro corte produce un fragmento menos conocido llamado Aη. Trabajos previos mostraron que Aη puede dañar las conexiones entre las células nerviosas y debilitar la capacidad del cerebro para reforzar los recuerdos. En sus experimentos, los investigadores encontraron que la mutación E590D no solo aumenta Aβ; también incrementa de forma marcada Aη y un fragmento upstream que alimenta ambas vías. Esto significa que la mutación desplaza el procesamiento de APP hacia un doble impacto de péptidos perjudiciales, potencialmente alterando los circuitos cerebrales incluso antes de que se esperen las placas amiloides clásicas.
Cómo la mutación acelera el tráfico celular
Para entender por qué se generan más fragmentos tóxicos, el equipo estudió dónde se localiza y cómo se mueve APP en la superficie celular. Muchos de los cortes que crean Aβ ocurren solo después de que APP ha sido internalizada mediante un proceso llamado endocitosis. Usando imágenes y trucos bioquímicos que etiquetan las proteínas en la superficie y luego siguen su internalización, los científicos mostraron que la APP mutante es menos abundante en el exterior de las células y se internaliza más rápidamente en compartimentos internos que la APP normal. Una vez dentro de estos endosomas tempranos, APP encuentra las enzimas que generan Aβ, y el tráfico alterado parece dar a esas enzimas más oportunidad de actuar. Al mismo tiempo, también aumenta el corte en el sitio η en la superficie, lo que explica el aumento de Aη.
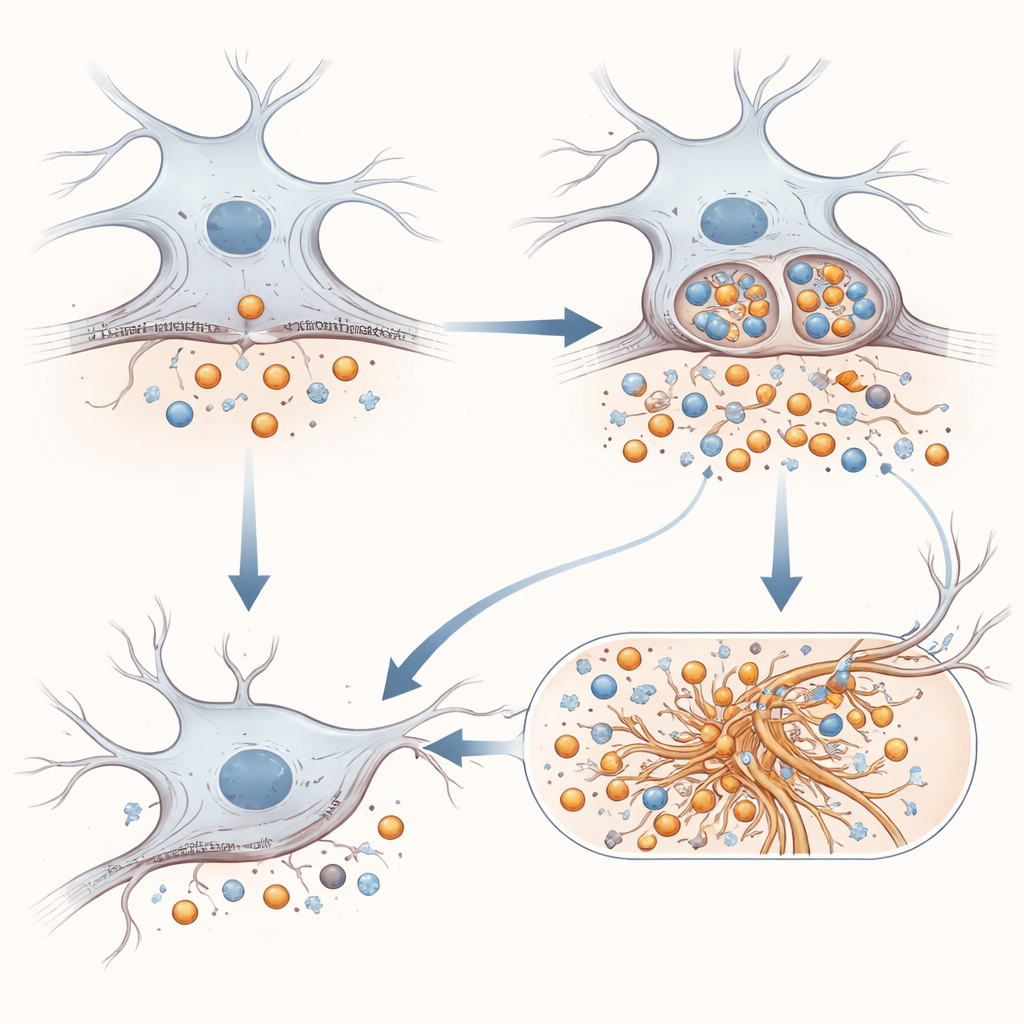
De fragmentos proteicos a tau enmarañada y neuroinflamación
La historia no termina con los fragmentos relacionados con la amiloide. Los investigadores probaron si la APP mutante influiría en la tau, la proteína estructural que forma fibras retorcidas en muchas demencias. En modelos celulares que se activan cuando semillas de tau inducen la formación de nuevos agregados, la presencia de APP E590D condujo a una agregación más fuerte que la APP normal o la ausencia de APP. En un modelo de ratón ya predispuesto a problemas de tau, la inyección en el hipocampo de un virus que expresa la APP mutante empeoró los ovillos de tau y desencadenó una mayor activación de astrocitos y microglía, las células de soporte e inmunitarias del cerebro. Curiosamente, las piezas amiloides solubles estándar fueron difíciles de detectar en estos cerebros de ratón, pero apareció un fragmento derivado de APP distinto solo cuando estaba presente la mutación, lo que sugiere un procesamiento alterado en tejido vivo.
Qué significa esto para entender el Alzheimer
En conjunto, los hallazgos muestran que esta rara mutación de APP no es benigna. Empuja a APP a generar más de un péptido tóxico, acelera los pasos de internalización que favorecen los cortes perjudiciales y amplifica el enmarañamiento de la tau y la inflamación en el cerebro. Para el público general, el mensaje clave es que la biología del Alzheimer no está impulsada por un único agente nocivo, sino por una red de fragmentos proteicos y respuestas celulares interactivas. Estudiar variantes genéticas tan potentes pero inusuales ofrece una vista ampliada de esa red. En este caso, sugiere que las terapias podrían necesitar considerar tanto la amiloide como péptidos alternativos derivados de APP como Aη, así como su impacto combinado sobre la tau, en lugar de dirigirse a una sola vía de forma aislada.
Cita: Liu, T., Wetzel, L., Roy, D. et al. APP E590D mutation increases generation of Aβ and Aη peptides and exacerbates tauopathy. npj Dement. 2, 21 (2026). https://doi.org/10.1038/s44400-026-00069-9
Palabras clave: Enfermedad de Alzheimer, proteína precursora de amiloide, ovillos de tau, neuroinflamación, mutación genética