Clear Sky Science · es
Una plataforma cuantitativa de alto rendimiento que utiliza organoides cerebrales humanos disociados en 2D para modelar la neuroinflamación en la enfermedad de Alzheimer
Por qué las infecciones podrían importar para la pérdida de memoria
La enfermedad de Alzheimer suele describirse como una acumulación lenta de proteínas pegajosas en el cerebro, pero crecientes evidencias sugieren que las infecciones podrían ayudar a poner en marcha este proceso. Este estudio explora esa idea usando pequeños modelos cerebrales cultivados en el laboratorio para plantear una pregunta simple: ¿puede un virus común causante de herpes labial desencadenar cambios similares a los del Alzheimer en células cerebrales humanas, y puede un fármaco antiviral revertir esos cambios?
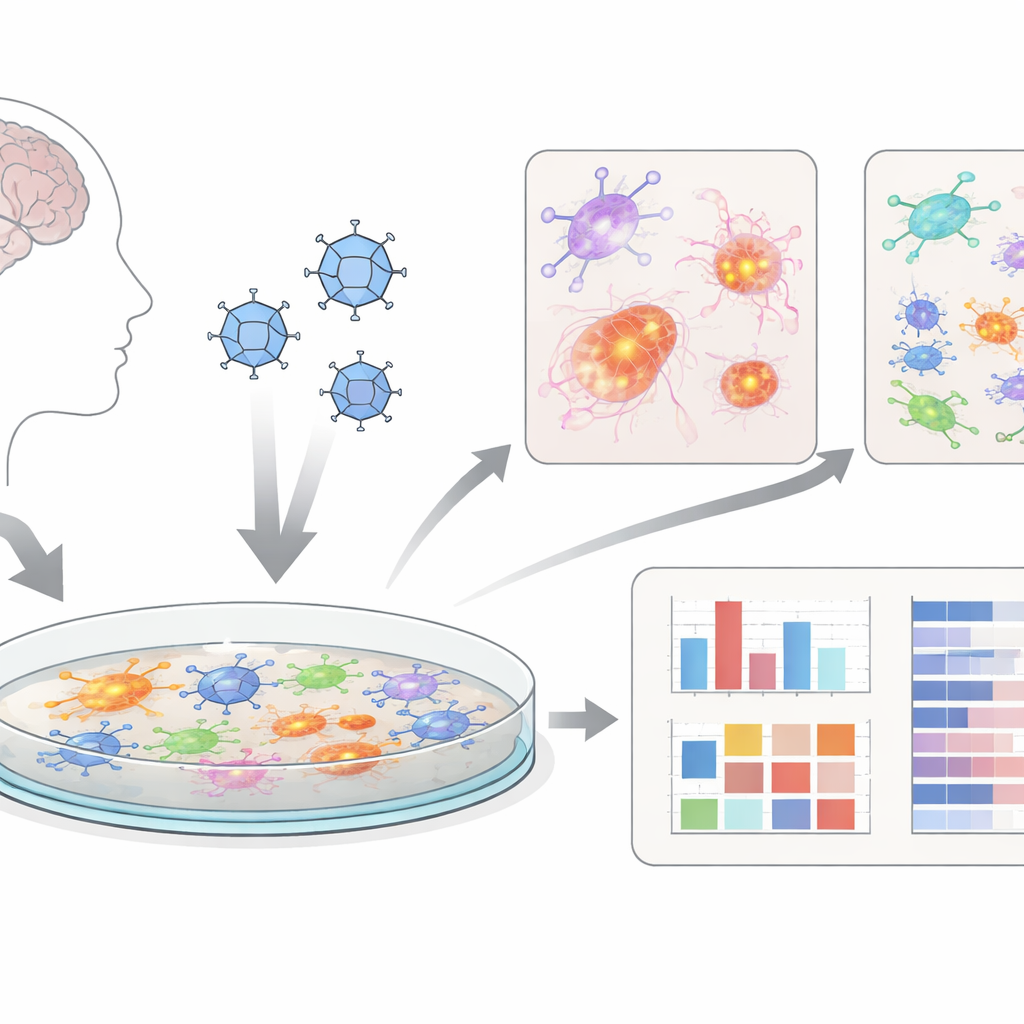
Mini‑cerebros en una placa
En lugar de trabajar únicamente con animales, los investigadores utilizaron “organoides cerebrales”: agregados de células con aspecto cerebral obtenidos a partir de células madre humanas. Después disociaron suavemente estos organoides 3D en capas planas de células cerebrales mixtas, que incluyen neuronas, células de soporte llamadas astrocitos y microglía con funciones inmunes. Estas cultivos bidimensionales, que denominan dcOrgs, son más fáciles de infectar de forma homogénea y de probar en alto rendimiento, lo que permite examinar muchas placas y condiciones de fármaco en paralelo. Esto hace que el sistema resulte atractivo como herramienta de cribado para nuevos tratamientos.
Un virus del herpes labial como chispa
El equipo infectó los dcOrgs con el virus del herpes simple 1 (VHS‑1), el virus responsable de la mayoría de los herpes labiales y sospechoso desde hace tiempo de contribuir a la demencia en algunas personas. Compararon los cultivos infectados con controles tratados simuladamente, con cultivos tratados con un antiviral (aciclovir), con cultivos expuestos a otro virus (influenza A) y con virus inactivado por luz ultravioleta. Mediante análisis automatizados de células y secuenciación de una sola célula, confirmaron que el VHS‑1 infectó robustamente muchos tipos celulares en la placa, mientras que el virus inactivado y la influenza produjeron patrones de cambio muy diferentes y más leves.
Cambios similares al Alzheimer dentro y entre las células
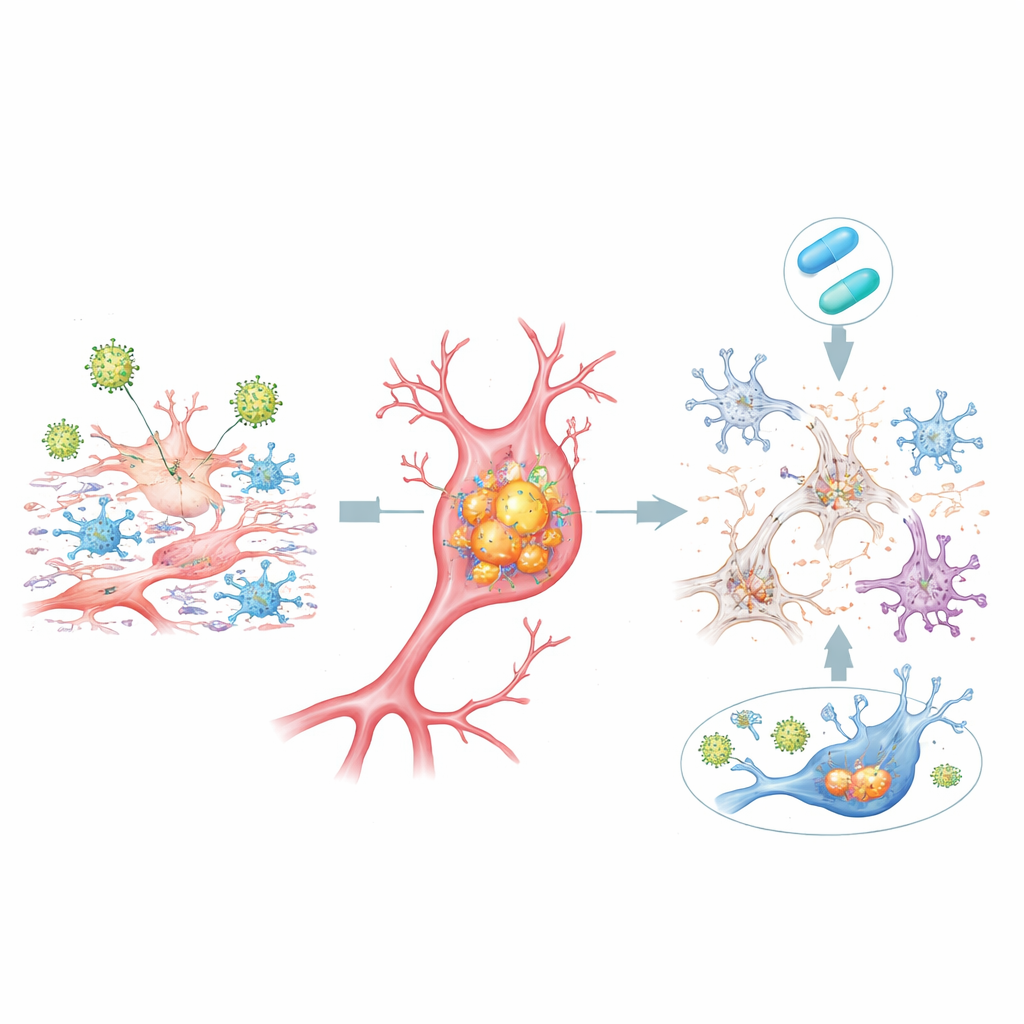
En los dcOrgs infectados por VHS‑1, muchas células acumularon altos niveles de las mismas formas proteicas observadas en cerebros con Alzheimer: amiloide beta agrupado dentro de las células y múltiples versiones «fosforiladas» de tau, otra proteína clave de la enfermedad. Estas acumulaciones se asociaron con mayor fuerza a células que contenían proteínas virales y fueron especialmente intensas en células moribundas. Al mismo tiempo, se liberó menos del fragmento de amiloide beta más largo (Aβ42) al fluido circundante en comparación con formas más cortas, un cambio que refleja patrones medidos en el líquido cefalorraquídeo de pacientes con Alzheimer. También cambiaron las poblaciones celulares: disminuyó el número de neuronas, mientras que astrocitos y microglía se expandieron, evocando la pérdida neuronal y la inflamación reactiva observadas en tejido cerebral de pacientes.
La actividad génica vincula el modelo con el Alzheimer humano
Al examinar la actividad génica en todo el genoma, los investigadores hallaron que la infección por VHS‑1 en los dcOrgs activó y desactivó muchos genes previamente relacionados con el riesgo de Alzheimer en grandes estudios genéticos humanos. Estos cambios no se observaron en cultivos más simples de células madre ni en dcOrgs infectados por influenza, lo que sugiere una interacción específica entre el VHS‑1 y el entorno cerebral mixto. La secuenciación de una sola célula reveló que algunos de los cambios génicos vinculados al Alzheimer procedían de células expuestas al virus pero que contenían poco o ningún material genético viral, insinuando que señales procedentes de vecinos infectados pueden propagar programas inflamatorios nocivos.
Lo que el tratamiento antiviral puede y no puede arreglar
Agregar el antiviral aciclovir poco después de la exposición al VHS‑1 redujo la expresión de genes virales, atenuó muchas respuestas inflamatorias, disminuyó la acumulación de amiloide beta y tau tóxicos dentro de las células y restauró parcialmente el equilibrio entre los distintos tipos celulares. Para una fracción sustancial de genes asociados al Alzheimer, sus niveles de actividad volvieron hacia la normalidad. Sin embargo, no todos los cambios fueron reversibles: un grupo considerable de genes humanos quedó sin cambios o incluso se vio más perturbado por el tratamiento, especialmente cuando el fármaco fue menos eficaz bloqueando genes virales tardíos. Esto subraya que, aunque detener la replicación viral puede ayudar, puede no deshacer por completo la cascada biológica una vez que se ha puesto en marcha.
Qué significa esto para comprender el Alzheimer
Para un público no especializado, la conclusión es que un virus humano causante de herpes labial, actuando dentro de una mezcla realista de células cerebrales humanas, puede producir rápidamente muchas señas de identidad de la enfermedad de Alzheimer: desde agregados proteicos y neuronas moribundas hasta patrones genéticos ya observados en pacientes. El sistema plano basado en organoides desarrollado aquí es rápido, cuantitativo y escalable, lo que lo convierte en un terreno de pruebas potente para antivirales y otras terapias dirigidas a calmar la inflamación cerebral. Aunque esto no prueba que las infecciones por herpes causen el Alzheimer en todos los pacientes, refuerza la hipótesis de que, para un subconjunto de personas, las infecciones virales crónicas o reactivadas pueden ser una pieza importante del rompecabezas y un posible objetivo para la prevención.
Cita: Olson, M.N., Barton, N.J., Feng, L. et al. A high-throughput, quantitative platform using 2D dissociated human cerebral organoids to model neuroinflammation in Alzheimer’s disease. npj Dement. 2, 20 (2026). https://doi.org/10.1038/s44400-026-00066-y
Palabras clave: enfermedad de Alzheimer, virus del herpes simple, organoides cerebrales, neuroinflamación, terapia antiviral