Clear Sky Science · es
Codificación de aristas funcionales en grafos para modelar relaciones espacialmente variables en el microambiente tumoral
Por qué importa cartografiar el vecindario del cáncer
El cáncer no crece aislado. Las células tumorales conviven en un vecindario bullicioso de células inmunitarias, células de soporte, vasos sanguíneos y señales químicas, todos apiñados en el espacio. La disposición de estos vecinos y la intensidad con que se influyen entre sí pueden determinar si un cáncer se disemina, responde al tratamiento o se mantiene controlado. Este artículo presenta SPIFEE, un nuevo marco de inteligencia artificial que convierte imágenes microscópicas y mapas moleculares de tumores en redes, ayudando a los investigadores a identificar qué interacciones entre células y vías están más vinculadas al tipo de enfermedad y al resultado del paciente.
Convertir tejido en un mapa de red
Los estudios modernos del cáncer miden mucho más que el aspecto de un tumor al microscopio. Algunos métodos resaltan docenas de proteínas en células individuales, otros ofrecen detalladas láminas de la estructura tisular, y herramientas más recientes registran qué genes están activos en miles de puntos a lo largo de un corte tumoral. SPIFEE trata todas estas fuentes como distintas vistas del mismo vecindario. Representa cada muestra como un grafo: los nodos representan entidades clave en el microambiente tumoral—como tipos celulares, patrones visuales del tejido o vías moleculares—mientras que las aristas capturan cómo estas entidades interactúan en el espacio. De forma crucial, SPIFEE no reduce una interacción a un solo número como la “distancia.” En su lugar, cada arista almacena una pequeña curva que describe cuán fuertemente dos entidades se mezclan o se repelen a lo largo de un rango de distancias, preservando un detalle espacial mucho más rico.
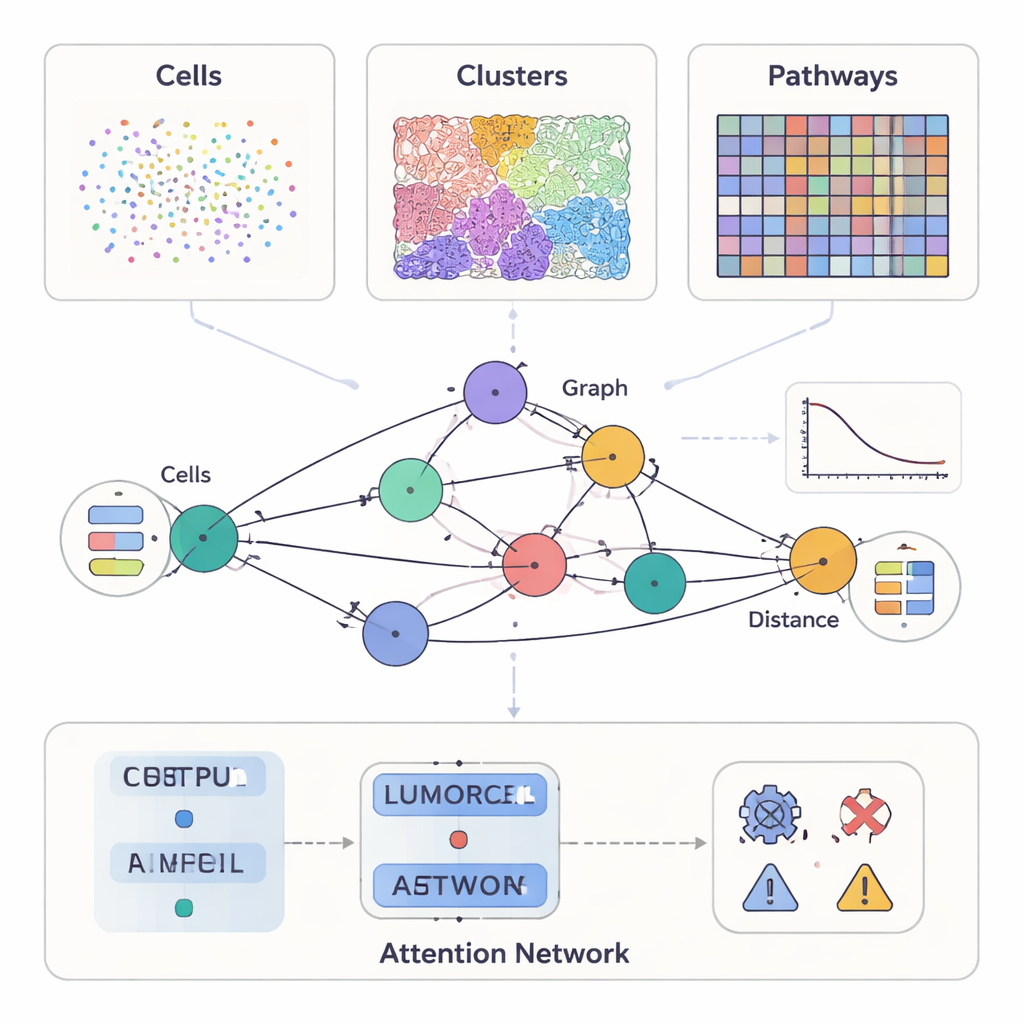
Una lente flexible para muchos tipos de datos oncológicos
Los autores probaron SPIFEE en varios conjuntos de datos oncológicos grandes e independientes que abarcan diferentes tecnologías y escalas. En muestras de enfermedad pancreática marcadas con inmunofluorescencia multiplexada, cada nodo del grafo representaba un tipo celular, y las características de los nodos provenían de secuenciación de ARN unicelular que resumía cómo tienden a comunicarse esas células. En láminas de cáncer de pulmón teñidas con el método rutinario de hematoxilina y eosina, los nodos representaban patrones visuales recurrentes del tejido, descubiertos automáticamente por un sistema de aprendizaje auto-supervisado. En un tercer escenario, láminas estándar de cáncer de pulmón se convirtieron mediante una herramienta de aprendizaje profundo en transcriptómica espacial virtual, y los nodos de SPIFEE representaron vías moleculares como hipoxia, vías relacionadas con estrógenos o JAK–STAT, con características derivadas de la actividad génica. En todos estos contextos, el mismo marco pudo ingerir distintos tipos de nodos y aun así construir grafos espaciales comparables.
Encontrar las interacciones que separan los resultados clínicos
Una vez que SPIFEE construye un grafo, lo pasa por una red de atención sobre grafos (graph attention network), un tipo de red neuronal que aprende no solo a predecir un resultado—como subtipo de cáncer, riesgo de supervivencia o enfermedad frente a inflamación no cancerosa—sino también a resaltar qué aristas fueron más relevantes para esa predicción. En tejido pancreático, SPIFEE distinguió pancreatitis crónica de adenocarcinoma ductal pancreático con mayor precisión que métodos previos basados en grafos. El modelo se centró de forma consistente en interacciones que involucraban células epiteliales (similares a tumorales) y células T reguladoras, células presentadoras de antígeno y células T ayudantes, apuntando a un vecindario inmunosupresor más prominente en el cáncer que en la inflamación. En láminas de adenocarcinoma pulmonar, SPIFEE identificó patrones estroma-tumorales particulares cuyas interacciones se correlacionaban con mejor o peor supervivencia, sugiriendo que las “zonas fronterizas” entre tumor y tejido de soporte codifican pistas pronósticas importantes que los análisis estándar pueden pasar por alto.
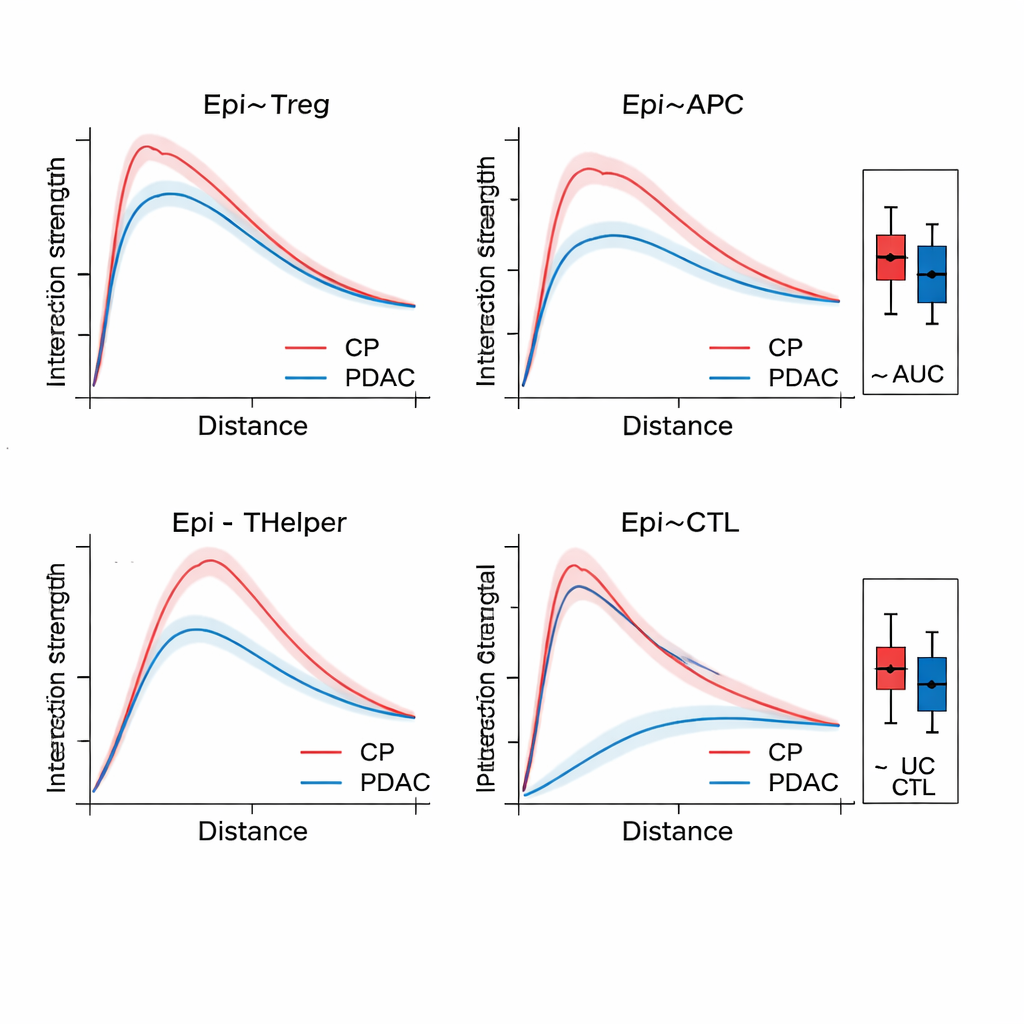
Leer el diálogo molecular a partir de láminas rutinarias
Quizá lo más llamativo es que SPIFEE pudo inferir interacciones significativas entre vías a partir de imágenes patológicas ordinarias una vez que éstas se tradujeron en mapas predichos de actividad génica. Al tratar las vías como nodos y su coocurrencia espacial como aristas funcionales, el método destacó pares como hipoxia con EGFR o JAK–STAT con PI3K—combinaciones ya conocidas por impulsar la evasión inmune y la resistencia a fármacos en cáncer de pulmón. También elevó vías relacionadas con estrógenos en adenocarcinoma pulmonar y ciertas vías inmunitarias y de estrés en tumores escamosos, hallazgos que coincidieron con patrones vistos en secuenciación de ARN a granel y en un conjunto de datos independiente de transcriptómica espacial real. Esto sugiere que, incluso cuando las mediciones moleculares son aproximadas, los patrones espaciales en láminas rutinarias aún contienen señales recuperables sobre cómo interactúan vías clave en tumores vivos.
Qué significa esto para la atención oncológica futura
Para un no especialista, el mensaje clave es que SPIFEE ofrece una nueva manera de leer la “vida social” de las células cancerosas directamente desde imágenes y mapas moleculares. Al codificar cómo cambian las relaciones con la distancia en lugar de aplanarlas a puntuaciones únicas, y al usar redes neuronales basadas en atención para clasificar qué interacciones importan más, el marco puede descubrir combinaciones de células, patrones tisulares y vías que distinguen tipos de cáncer y predicen la supervivencia. Aunque estos hallazgos aún requieren validación biológica y clínica, enfoques como SPIFEE apuntan hacia un futuro en el que las muestras tumorales rutinarias puedan producir no solo instantáneas estáticas, sino mapas dinámicos de puntos calientes de interacción que ayuden a guiar el diagnóstico, la estratificación de riesgo y, eventualmente, las decisiones de terapia personalizada.
Cita: Tsang, A.P., Krishnan, S.N., Kulkarni, R. et al. Encoding functional edges in graphs to model spatially varying relationships in the tumor microenvironment. npj Artif. Intell. 2, 27 (2026). https://doi.org/10.1038/s44387-026-00075-5
Palabras clave: microambiente tumoral, transcriptómica espacial, redes neuronales en grafos, patología del cáncer, interacciones célula-célula