Clear Sky Science · es
Una red neuronal informada por el metabolismo identifica vías que influyen en la potencia y toxicidad de combinaciones antimicrobianas
Por qué esto importa para la salud cotidiana
A medida que más infecciones dejan de responder a nuestros antibióticos habituales, los médicos recurren cada vez más a combinaciones de fármacos. Pero mezclar medicamentos puede ser una espada de doble filo: la pareja adecuada puede eliminar bacterias persistentes, mientras que la combinación equivocada puede dañar órganos como los riñones y el hígado. Este estudio presenta un nuevo enfoque computacional, llamado CALMA, diseñado para ayudar a científicos y clínicos a encontrar combinaciones de fármacos que sean a la vez potentes contra los microbios y más benignas para los pacientes.
Combatir gérmenes sin prueba y error
Tradicionalmente, descubrir buenas combinaciones de antibióticos ha significado probar en el laboratorio y en pacientes enormes cantidades de pares o tríos de fármacos. El número de mezclas posibles crece de forma explosiva con cada fármaco añadido, lo que hace que una prueba experimental completa sea poco realista. Además, la mayoría de las herramientas actuales se centran únicamente en la intensidad con la que las combinaciones matan bacterias, ignorando cómo podrían dañar los tejidos humanos. Los autores sostienen que, para diseñar mejores tratamientos, debemos considerar ambos lados de la ecuación: la potencia contra los patógenos y la seguridad para las personas.
Un modelo inteligente que entiende la química celular
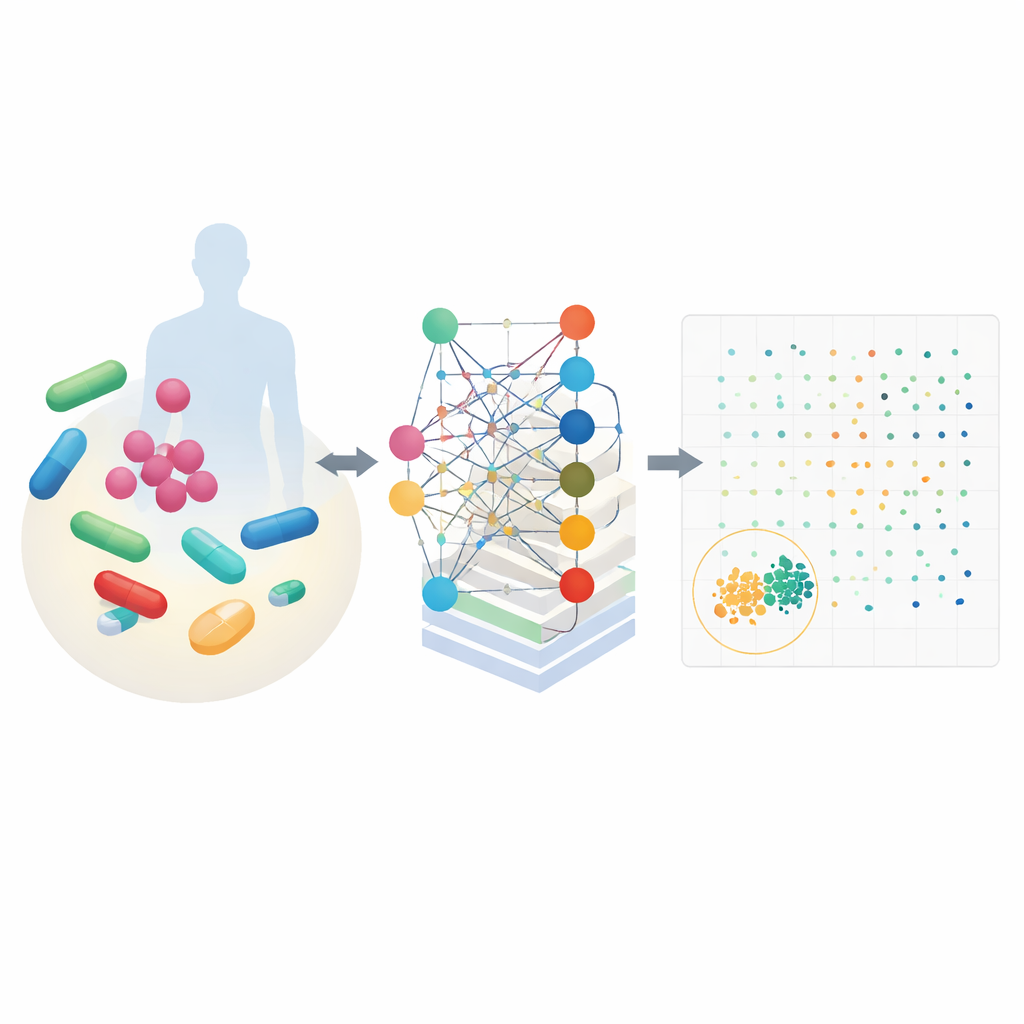
CALMA combina dos ideas potentes. Primero, utiliza mapas detallados del metabolismo celular que describen cómo los organismos convierten nutrientes en energía y bloques de construcción. Estos mapas, elaborados para bacterias como Escherichia coli y el germen de la tuberculosis, simulan cómo cambian miles de reacciones químicas cuando está presente un fármaco. Segundo, CALMA alimenta estas simulaciones a una red neuronal artificial cuya estructura refleja las rutas metabólicas. Agrupando la información según rutas biológicas conocidas —como la producción de energía o el reciclaje de nucleótidos—, el modelo aprende patrones que vinculan vías específicas con la eliminación efectiva de bacterias o con efectos secundarios dañinos en células humanas.
Explorando el paisaje de las mezclas de fármacos
Usando datos de experimentos previos y grandes bases de datos de seguridad, los investigadores entrenaron a CALMA para asignar a cada combinación de fármacos dos puntuaciones: una sobre cuánto ataca a las bacterias y otra sobre la probabilidad de ser tóxica en humanos. Al representar gráficamente estas puntuaciones se crea un paisaje donde los mejores candidatos se sitúan en la esquina inferior izquierda: potentes contra microbios y suaves con las células humanas. Cuando aplicaron CALMA a 35 fármacos de relevancia clínica, la herramienta redujo casi 600 pares posibles a un pequeño conjunto de opciones prometedoras, disminuyendo el espacio de búsqueda experimental en aproximadamente un 97 por ciento. Entre las principales sugerencias hubo combinaciones que incluían antibióticos comunes como azitromicina, vancomicina, isoniazida y trimetoprim.
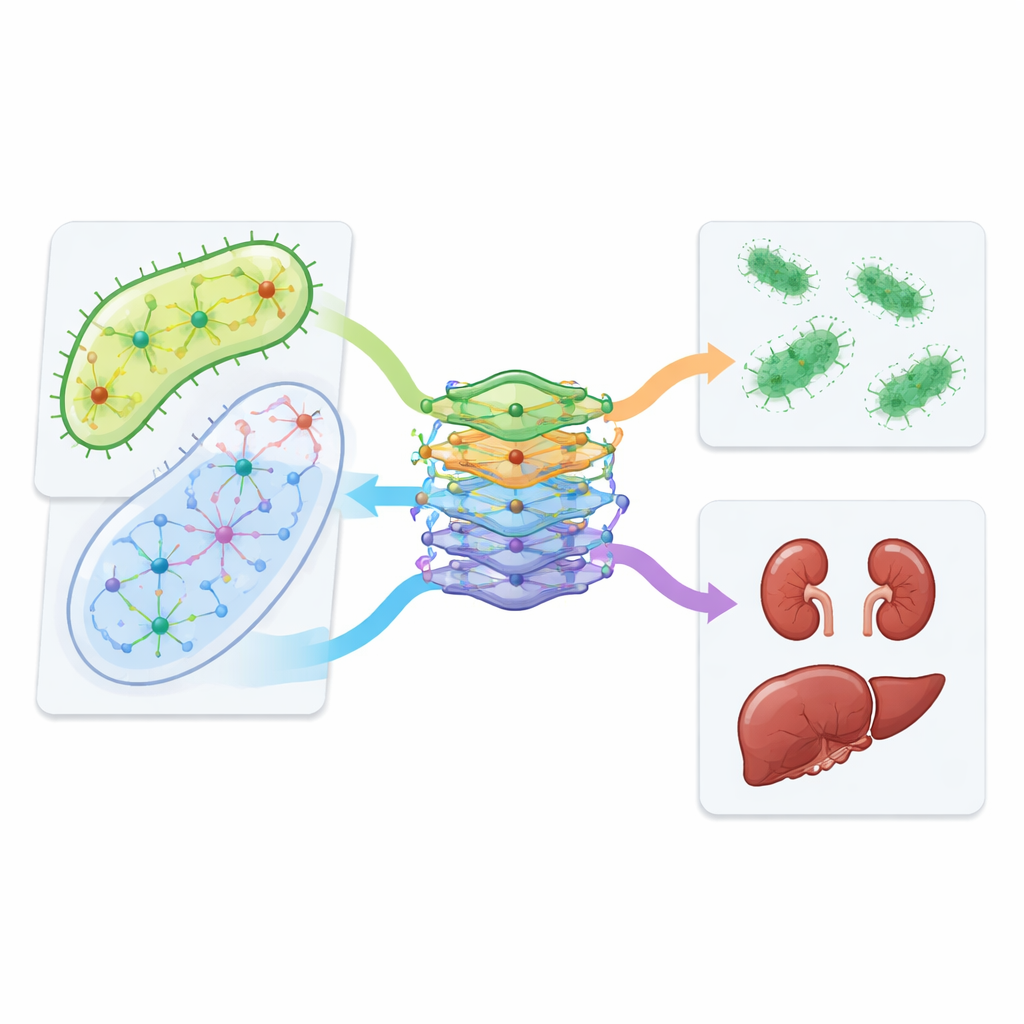
De las predicciones por ordenador a las pruebas de laboratorio y a pacientes reales
El equipo pasó más allá de las simulaciones para probar varias combinaciones predichas en líneas celulares de riñón e hígado. Encontraron que ciertos pares, incluidos azitromicina con vancomicina e isoniazida con trimetoprim, eran menos tóxicos para las células humanas que los fármacos por separado, manteniendo al mismo tiempo actividad contra E. coli. El diseño de CALMA también permitió a los investigadores sondear qué rutas metabólicas impulsan la toxicidad. Una vía que recicla los bloques de construcción del ADN, conocida como salvamento de nucleótidos, emergió como un actor clave: modificarla en experimentos celulares cambió la toxicidad de algunas combinaciones. Finalmente, los autores examinaron historias clínicas de cientos de miles de pacientes y observaron que las personas que recibieron azitromicina junto con vancomicina presentaban menos problemas renales documentados que pacientes similares tratados solo con vancomicina, lo que corrobora los hallazgos de laboratorio.
Qué implica esto para tratamientos futuros
Para un no especialista, CALMA puede considerarse un filtro inteligente que comprende lo suficiente de biología como para sugerir qué mezclas de fármacos merecen probarse primero. En lugar de mezclar antibióticos a ciegas y esperar lo mejor, los investigadores pueden centrarse en combinaciones que los modelos predicen que atacarán puntos débiles bacterianos mientras protegen vías humanas sensibles. Aunque el método depende de los datos disponibles y no es perfecto, ofrece una ruta más racional para diseñar terapias combinadas. Con el tiempo, herramientas como CALMA podrían ayudar a los médicos a tratar infecciones resistentes con mayor seguridad, reducir el ensayo y error en el desarrollo de fármacos e incluso adaptarse a otras enfermedades donde las combinaciones de tratamientos y los efectos secundarios son preocupaciones importantes.
Cita: Arora, H.S., Lev, K., Robida, A. et al. A Metabolism-Informed Neural Network Identifies Pathways Influencing the Potency and Toxicity of Antimicrobial Combinations. npj Drug Discov. 3, 11 (2026). https://doi.org/10.1038/s44386-026-00042-9
Palabras clave: combinaciones de antibióticos, toxicidad de fármacos, redes neuronales artificiales, metabolismo, resistencia antimicrobiana