Clear Sky Science · es
Desarrollo de un protocolo para contrarrestar la activación espontánea in vitro de fibroblastos intestinales usando diseño de experimentos
Por qué importa mantener tranquilas a las células que reparan el intestino
En enfermedades crónicas del intestino como la de Crohn, el tejido cicatricial puede estrechar lentamente el intestino hasta que los alimentos apenas pasan, lo que a menudo conduce a una intervención quirúrgica. Esta cicatrización, llamada fibrosis, está impulsada por células de soporte conocidas como fibroblastos que se vuelven hiperactivas y depositan demasiado tejido conectivo. Para entender y, algún día, prevenir este proceso, los científicos dependen de fibroblastos cultivados en el laboratorio. Pero hay un problema: los platos de plástico simples usados en la mayoría de los laboratorios empujan a estas células a un estado activado de forma artificial, lo que dificulta estudiar los primeros pasos que conducen de un intestino sano a uno fibrótico.
Cuando la placa de laboratorio envía la señal equivocada
Los autores mostraron primero lo rápido que los fibroblastos intestinales se activan en el plástico de cultivo estándar. En apenas 24 horas, tanto una línea celular establecida como células primarias de donantes masculinos y femeninos pasaron de un estado tranquilo a una forma activada, semejante a la muscular. Produjeron altos niveles de proteínas asociadas a la contracción y la cicatrización, como la actina de músculo liso α y la proteína de activación de fibroblastos, incluso sin desencadenantes inflamatorios añadidos. Esto significa que muchos modelos de laboratorio existentes pueden partir de un estado que ya se parece a una enfermedad avanzada en lugar de a cambios tempranos y reversibles.
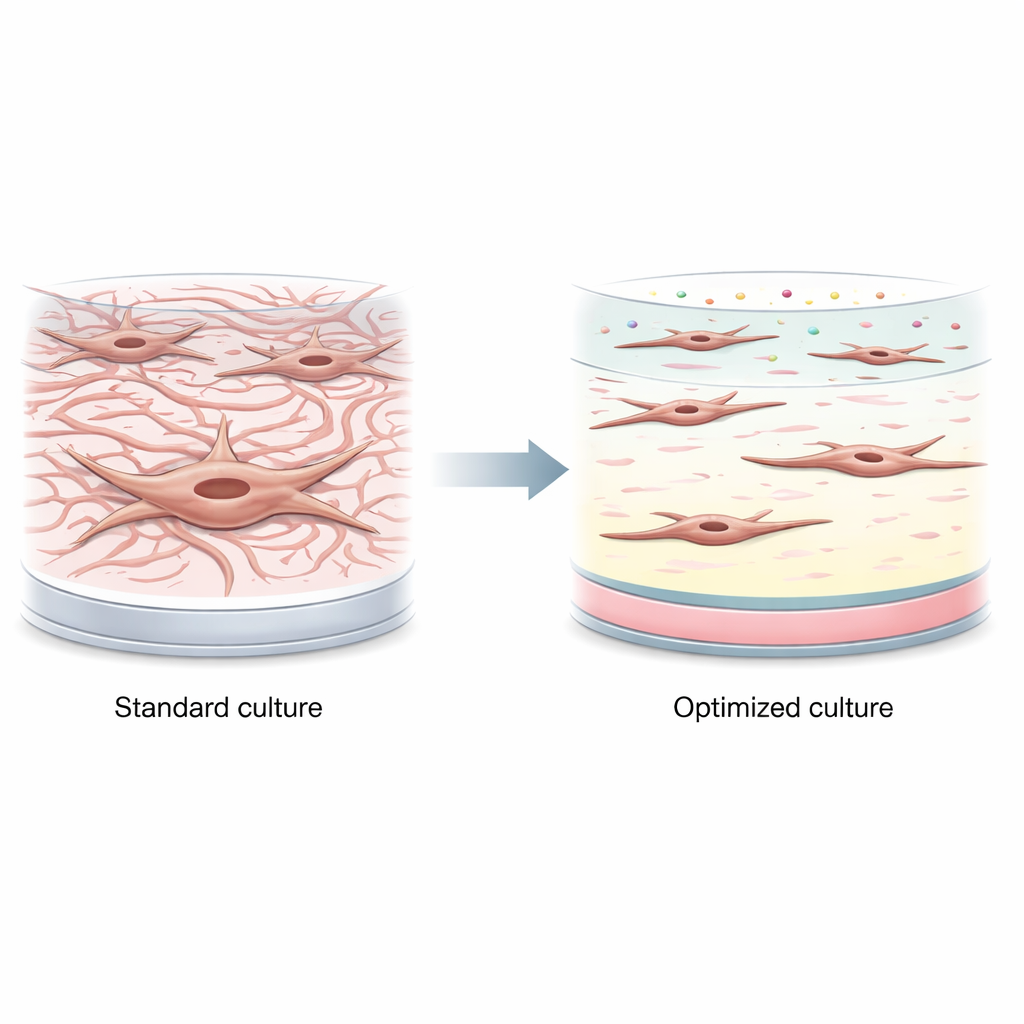
Probar ingredientes por separado no es suficiente
Para calmar de nuevo a las células, el equipo exploró componentes del entorno natural de los fibroblastos en el intestino, incluyendo proteínas clave de la matriz (colágenos tipo I y III, y laminina) y factores solubles (vitamina D y factor de crecimiento básico de fibroblastos, o FGF). Los probaron de uno en uno, ya sea como recubrimientos de superficie o como aditivos al medio de cultivo. Algunas condiciones redujeron marcadores de activación: por ejemplo, dosis moderadas de vitamina D disminuyeron un marcador importante de cicatrización varias veces, y ciertas densidades de recubrimiento tuvieron efectos leves. Pero estos beneficios se vieron compensados por problemas como la reducción de la supervivencia celular a niveles altos de vitamina D, y en general las modificaciones individuales no mantenían de forma fiable a los fibroblastos en un estado de baja actividad.
Dejar que la estadística explore el espacio de posibilidades
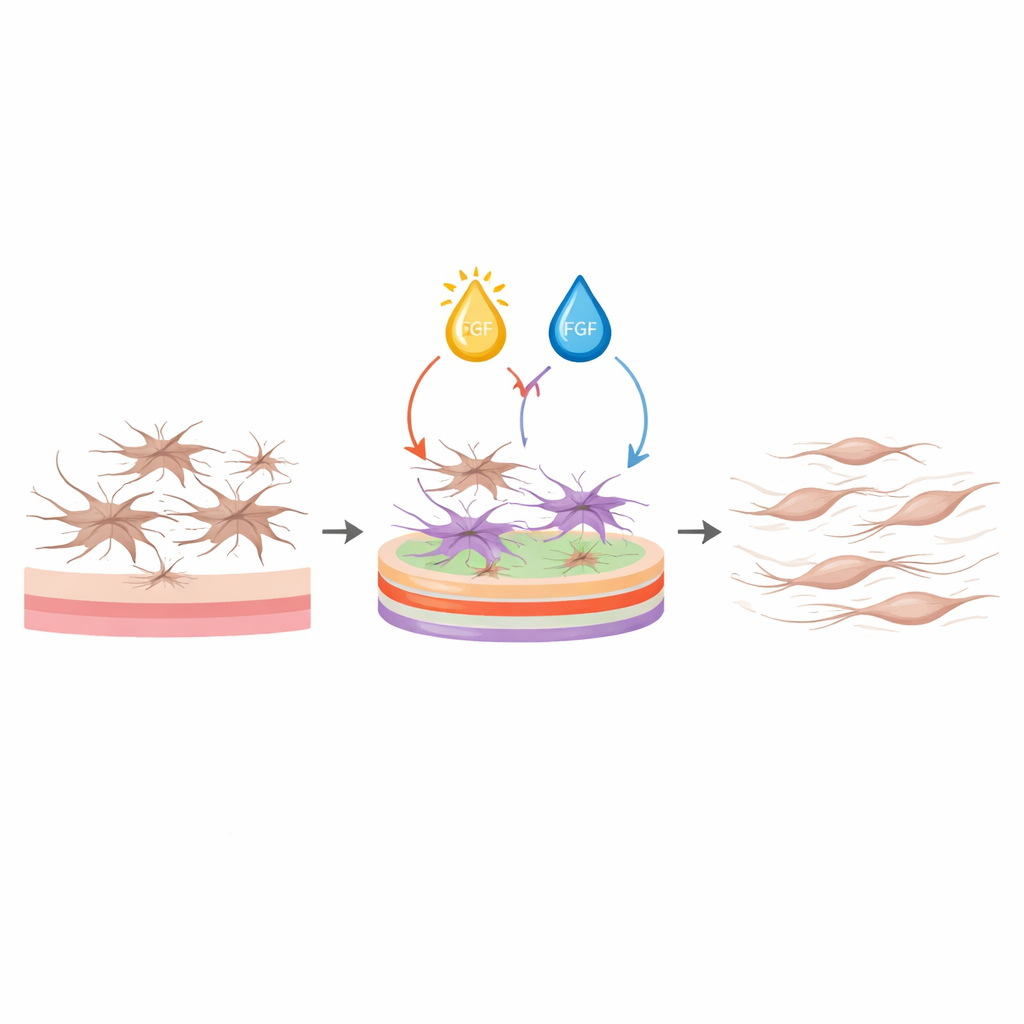
En lugar de ajustar un parámetro a la vez, los investigadores usaron un enfoque formal de "diseño de experimentos" para explorar muchas combinaciones de forma eficiente. Variaron cinco entradas—las tres proteínas de la matriz más la vitamina D y el FGF—en un amplio rango de dosis, generando 42 condiciones de cultivo escogidas cuidadosamente. Para cada una midieron cuatro resultados relacionados con la cicatrización: un marcador clave de activación, la secreción de una proteína matriz principal (fibronectina), el crecimiento celular y la supervivencia celular. Modelos estadísticos revelaron luego qué factores, y qué emparejamientos entre ellos, tenían mayor influencia. La vitamina D emergió como un actor potente pero sensible a la dosis, afectando todas las lecturas, mientras que el FGF tendió a reducir la activación y a favorecer el crecimiento y la supervivencia celular. El colágeno I, el colágeno III y la laminina configuraron cómo se interpretaban estas señales solubles, con ciertas combinaciones que amortiguaban la activación mucho más que cualquier factor individual.
Construir una receta para fibroblastos tranquilos pero sanos
Usando estos modelos, el equipo pidió al software que identificara condiciones que simultáneamente redujeran los marcadores de activación y la producción de matriz mientras mantenían las células vivas, sin exigir que la proliferación fuera baja. La mejor receta combinó una alta densidad de colágeno I, bajo colágeno III y alta laminina en la superficie de cultivo, junto con vitamina D de rango medio y FGF alto en el medio. Bajo este protocolo, los fibroblastos permanecieron delgados y fusiformes en lugar de extendidos y estrellados, expresaron niveles mucho más bajos de genes y proteínas vinculados a la contracción y la fibrosis, y secretaron mucho menos colágeno y fibronectina. Al mismo tiempo, su viabilidad se mantuvo igual o mejor que la de las células en plástico simple. Es importante que estos efectos se observaron no solo en la línea celular modelo sino también en fibroblastos primarios de donantes humanos masculinos y femeninos, lo que demuestra que el protocolo es robusto.
Qué significa esto para la investigación futura sobre la fibrosis intestinal
Al ajustar cuidadosamente el "vecindario" alrededor de los fibroblastos intestinales—tanto la superficie a la que se adhieren como los factores que los bañan—este estudio ofrece un protocolo directo que mantiene a estas células en un estado no activado, pero saludable, usando materiales de laboratorio estándar. Para los investigadores, esto proporciona un punto de partida limpio para añadir desencadenantes inflamatorios o mecánicos específicos y observar cómo comienza la fibrosis, en lugar de trabajar con células que ya son similares a tejido cicatricial. Más ampliamente, el trabajo demuestra cómo el diseño estadístico puede descubrir combinaciones sutiles y no intuitivas de ingredientes que doman comportamientos celulares complejos, allanando el camino para mejores modelos de cicatrización y, eventualmente, estrategias más dirigidas para prevenir o revertir la fibrosis intestinal.
Cita: Mohammadalizadeh, Z., Sudi, S., Basto Moreno, D.A. et al. Developing a protocol to counteract spontaneous in vitro activation of intestinal fibroblasts using design of experiments. npj Biomed. Innov. 3, 25 (2026). https://doi.org/10.1038/s44385-026-00079-5
Palabras clave: fibrosis intestinal, activación de fibroblastos, protocolo de cultivo celular, vitamina D y FGF, diseño de experimentos