Clear Sky Science · es
Inferir anomalías en vías de señalización a partir de imágenes histopatológicas mediante un grafo de conocimiento heterogéneo gen-vía con restricciones lógicas
Ver señales celulares ocultas en preparaciones de cáncer
Cuando los médicos examinan el cáncer al microscopio, mayormente ven formas y colores, no las complejas conversaciones moleculares que ocurren dentro de las células. Sin embargo, esas invisibles “conversaciones” de señalización entre genes y vías a menudo determinan cómo crece un tumor y cómo podría responder a un tratamiento. Este estudio presenta un nuevo sistema de inteligencia artificial que analiza imágenes rutinarias de patología e infiere qué rutas de comunicación celular, o vías, están fallando, ofreciendo una forma de vislumbrar el comportamiento molecular sin pruebas de laboratorio adicionales.
De las pistas de genes individuales a la imagen más amplia
Los enfoques tradicionales tratan de predecir el estado de genes individuales a partir de imágenes de tejido: ¿está mutado un gen concreto o no? Eso es útil, pero el cáncer rara vez depende de un único gen defectuoso. En cambio, grupos de genes actúan conjuntamente para perturbar vías de señalización enteras que controlan el crecimiento, la supervivencia y la respuesta inmune. Los autores sostienen que centrarse en genes individuales pasa por alto este comportamiento cooperativo y puede no explicar por qué los tumores se ven y se comportan de determinada manera al microscopio.
Construyendo un mapa entre imágenes, genes y vías
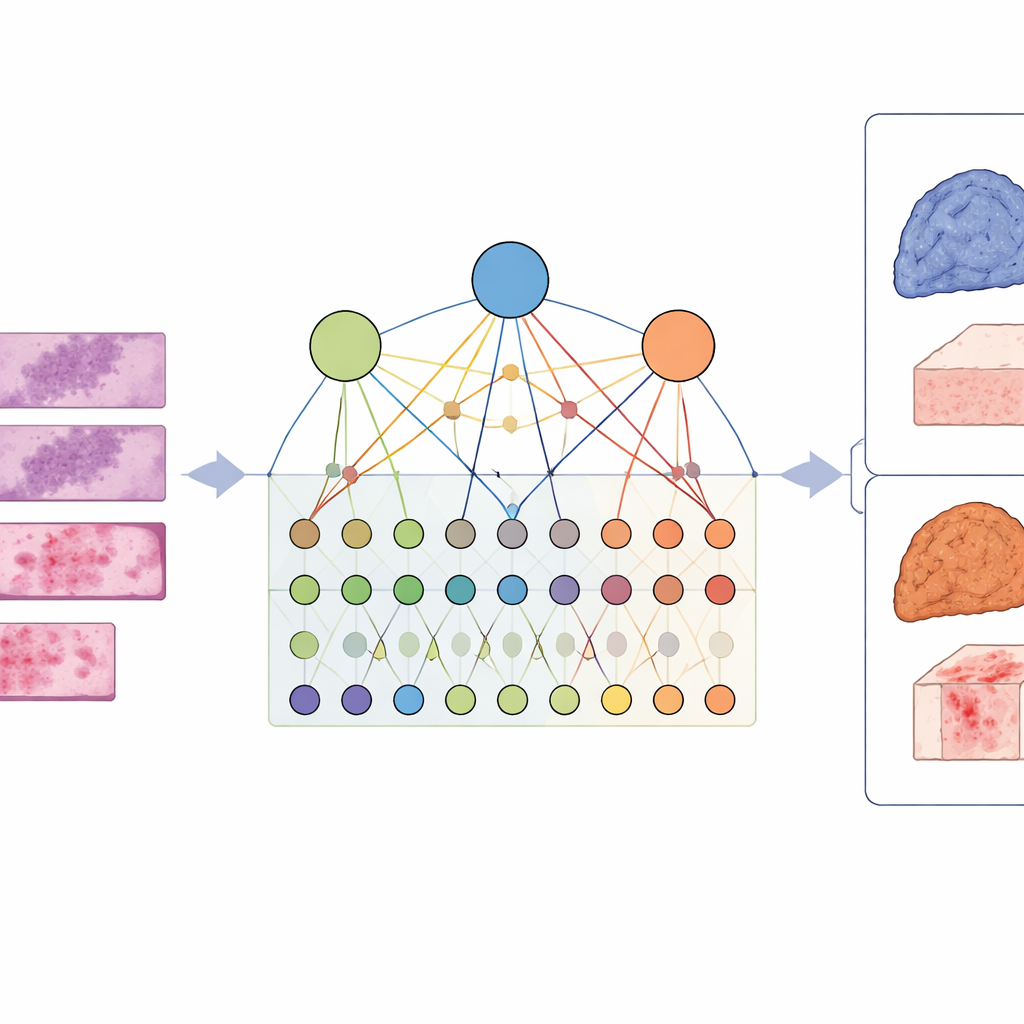
Para capturar esta complejidad, los investigadores diseñaron un marco llamado LCG-HGNN que vincula tres capas de información. Primero, dividen cada imagen de corte completo de adenocarcinoma de pulmón en muchos parches pequeños y representan esos parches como un grafo, donde regiones cercanas o de aspecto similar están conectadas. Segundo, conectan marcadores genéticos con vías de señalización usando bases de datos biológicas consolidadas, construyendo un segundo grafo que codifica qué genes pertenecen a qué vías. Finalmente, permiten que un modelo de IA haga pasar información por este grafo combinado, de modo que los patrones de imagen, los genes y las vías se influyan mutuamente en lugar de tratarse de forma aislada.
Enseñar al sistema la biología conocida
Una innovación clave es que al modelo no se le permite aprender libremente sin guía. Los autores incorporan en el sistema declaraciones claras, del tipo regla, derivadas de décadas de investigación en cáncer. Por ejemplo, algunas mutaciones casi nunca aparecen juntas en el mismo tumor, y algunas vías están corriente arriba o corriente abajo de otras. Codifican estas reglas como restricciones lógicas que orientan suavemente las conexiones internas y las predicciones de la IA. Si el modelo propone una combinación de cambios genéticos y en vías que choca con la biología conocida o con similitudes entre las preparaciones de distintos pacientes, estas reglas lo empujan hacia alternativas más realistas.
Evaluación de la precisión frente a métodos existentes
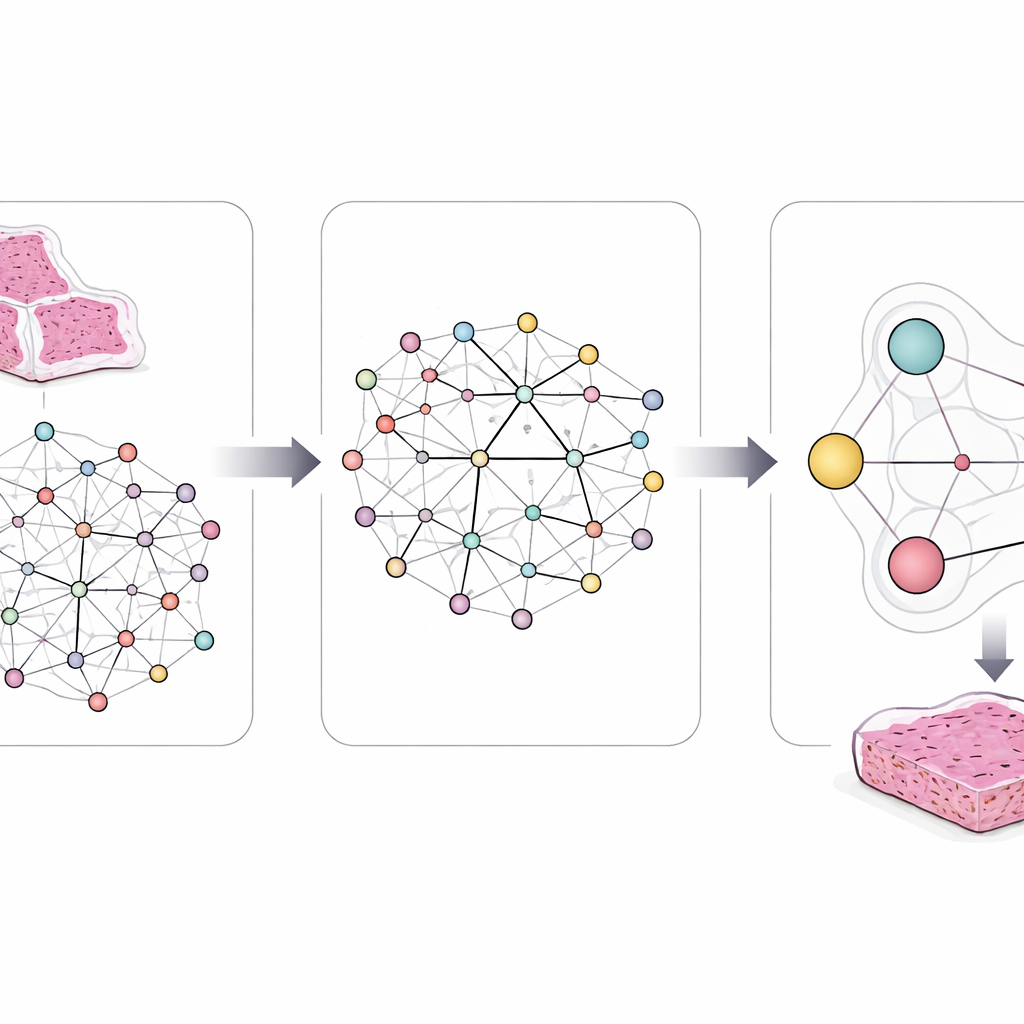
El equipo evaluó su sistema en más de 1.600 preparaciones de cáncer de pulmón vinculadas con datos genéticos. Lo compararon con modelos de aprendizaje profundo estándar que se centran en genes individuales y con métodos más avanzados que manejan muchos genes a la vez pero ignoran la estructura de vías. En varias vías importantes, incluidas las implicadas en señales de crecimiento celular y en el andamiaje del tejido, el nuevo modelo predijo cambios en grupos de genes y anomalías en vías con mayor precisión. También produjo parches de imagen cuya apariencia coincidía estrechamente con ejemplos clínicos reales asociados a mutaciones específicas, lo que sugiere que se centraba en patrones microscópicos significativos en lugar de rasgos espurios de la imagen.
Por qué esto importa para los pacientes
Para un público no especialista, el resultado principal es que este enfoque convierte una preparación de patología rutinaria en una rica fuente de información molecular. En lugar de solicitar pruebas genéticas separadas y a menudo costosas para cada posible diana, los médicos podrían usar eventualmente modelos así para cribar vías alteradas directamente a partir de las imágenes que ya recogen. Aunque el método todavía necesita validación más amplia en entornos reales y no sustituye aún a las pruebas genómicas, apunta a un futuro en el que la vista al microscopio también sea una ventana al cableado interno del tumor, ayudando a orientar una atención oncológica más precisa y basada en la biología.
Cita: Yu, Y., Shi, W., Chen, X. et al. Inferring signaling pathway abnormalities from histopathological images via logic-constrained gene-pathway heterogeneous knowledge graph. npj Biomed. Innov. 3, 23 (2026). https://doi.org/10.1038/s44385-026-00078-6
Palabras clave: vías del cáncer, IA en histopatología, redes neuronales en grafos, adenocarcinoma de pulmón, patología digital