Clear Sky Science · es
Uso de modelos de co-cultivo in vitro para orientar la ingeniería bacteriana en el tratamiento de tumores sólidos
Por qué las bacterias en el cáncer pueden importarte
Tratamientos contra el cáncer como la cirugía, la quimioterapia y la radioterapia salvan vidas, pero con frecuencia conllevan efectos secundarios severos y, demasiadas veces, fracaso terapéutico. Una idea fascinante es reclutar bacterias vivas como herramientas de precisión que localicen y ataquen tumores sólidos desde dentro. Este artículo explica cómo los científicos están construyendo sistemas de prueba en laboratorio —donde células humanas y bacterias crecen juntas— para diseñar terapias bacterianas más seguras e inteligentes antes de que lleguen a los pacientes.
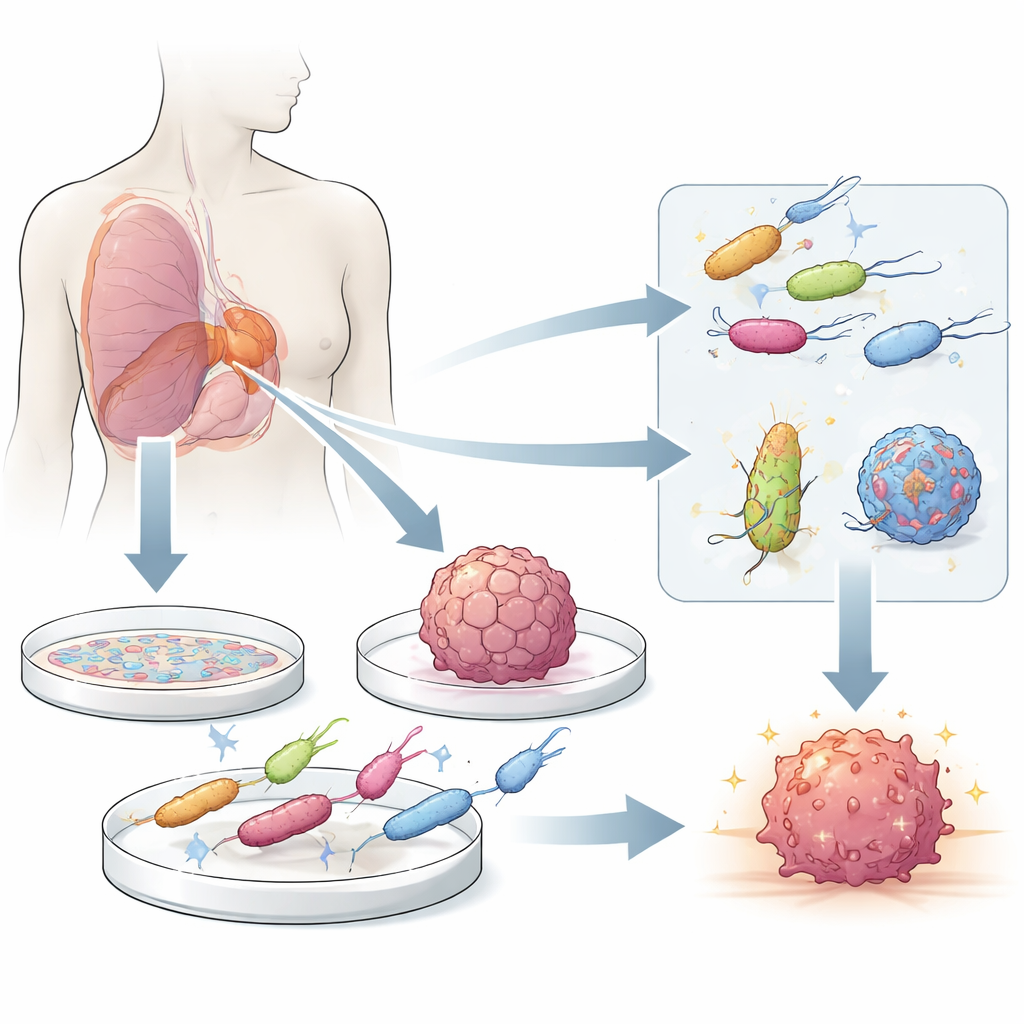
Pequeños auxiliares que buscan tumores
Algunas bacterias prefieren de forma natural el entorno hostil y con poco oxígeno del interior de los tumores sólidos frente a los tejidos sanos. Tras filtrarse por vasos sanguíneos tumorales permeables o viajar junto a células inmunitarias, estos microbios se desplazan hacia las células muertas y moribundas en el núcleo tumoral, donde pueden crecer y, en ocasiones, inducir la muerte de células cancerosas y desencadenar ataques inmunitarios locales. La ingeniería genética moderna convierte estas cepas naturalmente “tropistas” hacia tumores en vehículos vivos de entrega que pueden liberar fármacos, estimulantes inmunitarios u otras cargas directamente donde más se necesitan, mientras que los esfuerzos por atenuar sus rasgos dañinos mejoran la seguridad.
Construyendo mini-tumores de laboratorio realistas
Para entender y mejorar estos medicamentos vivos, los científicos necesitan bancos de ensayo que imiten lo que ocurre en el cuerpo humano lo más fielmente posible. Las capas celulares planas son fáciles de cultivar y útiles para un cribado rápido, pero no reproducen la estructura compleja ni los gradientes de oxígeno de los tumores reales. Los modelos tridimensionales, como los esferoides formados a partir de líneas celulares cancerosas y los organoides obtenidos de tejido de pacientes, reproducen mejor características clave como una capa externa viva, una zona interna poco activa y un núcleo necrótico. Cuando las bacterias se mezclan directamente con estos mini-tumores, los investigadores pueden observar cómo invaden, dónde se acumulan y qué tan bien funcionan los circuitos terapéuticos diseñados en condiciones que se asemejan a un tumor humano.
Separar células para estudiar señales
Otros diseños de co-cultivo se centran menos en el contacto físico y más en los intercambios químicos invisibles entre bacterias y células humanas. En sistemas transwell, una membrana porosa divide dos cámaras para que las moléculas pequeñas pasen mientras las células permanecen en su lugar. Esto permite a los científicos probar, por ejemplo, cómo una cepa bacteriana convierte un compuesto inocuo en un gas citotóxico que se difunde hacia las células cancerosas cercanas. Los chips microfluídicos —dispositivos diminutos con canales y compartimentos— añaden otra capa de realismo. Pueden controlar el flujo de fluidos, los niveles de oxígeno y la sincronización, permitiendo que bacterias diseñadas crezcan, lisen en ciclos sincronizados y bañen repetidamente a las células tumorales con moléculas terapéuticas, siguiendo de cerca cómo responden ambos socios a lo largo del tiempo.
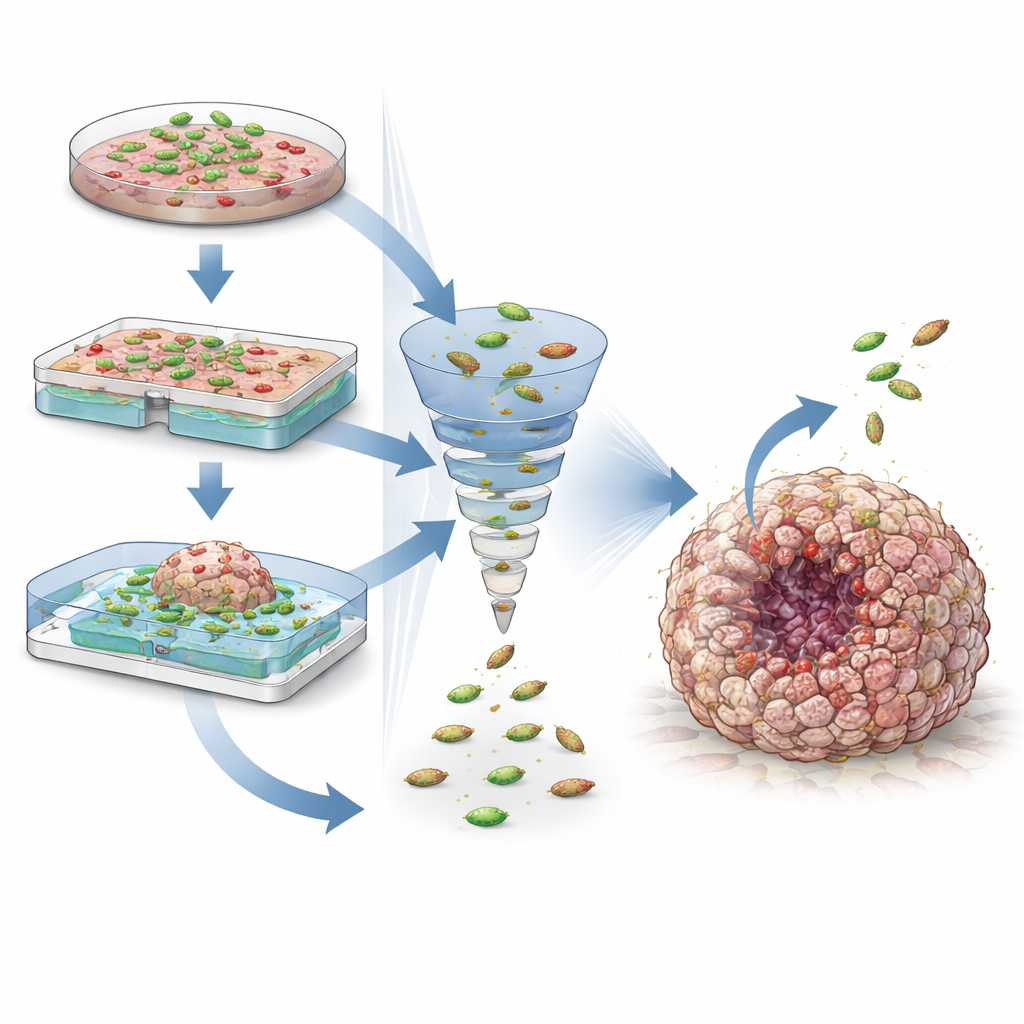
Escudriñar el ecosistema tumoral
Los modelos de co-cultivo también se utilizan para estudiar cómo interactúan las bacterias con el ecosistema tumoral más amplio. Los organoides derivados de pacientes individuales pueden conservar muchas de las particularidades genéticas y respuestas a fármacos de sus tumores originales, abriendo la puerta a pruebas personalizadas de terapias bacterianas. Añadir células inmunitarias a estos cultivos revela cómo las bacterias pueden potenciar o atenuar la inmunidad antitumoral y cómo podrían combinarse con fármacos inhibidores de puntos de control. Al mismo tiempo, estos modelos ponen de manifiesto riesgos de seguridad, como toxinas bacterianas que dañan el ADN y podrían contribuir al inicio del cáncer. Ajustando las condiciones de cultivo, los niveles de oxígeno y los métodos de medición —desde imágenes en vivo hasta secuenciación de ADN— los investigadores pueden explorar de forma sistemática estos beneficios y riesgos.
Del banco de laboratorio al paciente
A pesar de resultados prometedores en animales, muy pocas terapias bacterianas contra el cáncer han mostrado beneficios claros en ensayos humanos. Los autores sostienen que un uso más inteligente de los sistemas de co-cultivo puede cerrar esta brecha. Al capturar mejor las diferencias entre pacientes, la complejidad tumoral y los tratamientos previos, estos modelos pueden identificar qué cepas diseñadas son más prometedoras, cómo combinarlas con fármacos existentes y dónde pueden fallar. También subrayan la necesidad de estándares compartidos para que laboratorios de todo el mundo puedan comparar resultados y los reguladores evalúen la seguridad y la eficacia con mayor confianza. En términos sencillos, los mini-tumores de laboratorio cuidadosamente diseñados y cultivados junto a bacterias ofrecen una vía poderosa para refinar estos “microbios inteligentes”, aumentando las probabilidades de que futuros pacientes reciban terapias bacterianas que sean a la vez más seguras y más efectivas.
Cita: Foschini, S., Wright, J.A., Woods, S.L. et al. Use of in vitro co-culture models to inform bacterial engineering for the treatment of solid tumours. npj Biomed. Innov. 3, 21 (2026). https://doi.org/10.1038/s44385-026-00075-9
Palabras clave: terapia bacteriana contra el cáncer, organoides tumorales, modelos de co-cultivo, biología sintética, microambiente tumoral