Clear Sky Science · es
Modelos in vitro biofabricados en 3D como nuevas metodologías de enfoque para alternativas a los animales
Repensando cómo probamos los medicamentos nuevos
Durante casi un siglo, la mayoría de los fármacos nuevos se han probado en animales antes de llegar a los ensayos en humanos. Sin embargo, más de 9 de cada 10 candidatos a fármaco que parecen seguros en animales fracasan posteriormente en personas. Este artículo explora cómo una nueva generación de tejidos humanos "bioprintados" en 3D podría cambiar esa historia: ofreciendo formas más precisas y humanas de predecir cómo responde nuestro cuerpo a los medicamentos y, potencialmente, acelerando la llegada de tratamientos más seguros a los pacientes.

De los animales de laboratorio a las pruebas centradas en humanos
Una legislación reciente en EE. UU., conocida como la FDA Modernization Act 2.0, ha eliminado el requisito automático de que todo fármaco nuevo se pruebe en animales. En su lugar, los reguladores pueden ahora aceptar "Nuevas Metodologías de Enfoque" —sistemas de prueba relevantes para humanos diseñados para prever mejor las respuestas reales de los pacientes. Entre estas, la bioimpresión 3D destaca. Emplea impresoras especializadas para colocar células humanas vivas y materiales blandos tipo gel en formas complejas que imitan tejidos reales y miniórganos. El proceso a menudo comienza con imágenes médicas como TC o RM, que proporcionan un plano. Los científicos eligen entonces biomateriales adecuados, mezclan los tipos de células correctos para crear una "bio-tinta" imprimible y fabrican estructuras por capas o volumétricas que maduran hasta convertirse en modelos de tejido funcionales en biorreactores.
Cómo la bioimpresión 3D construye tejidos vivos
La bioimpresión no es una única tecnología, sino una familia de métodos. Las impresoras estilo inyección de tinta pulverizan diminutas gotas de un fluido que contiene células para construir capas delgadas con gran detalle, lo que las hace útiles para tejidos en miniatura como parches de piel o barreras pulmonares. Las impresoras de extrusión exprimen hebras continuas de bio-tintas más espesas, que pueden incluir muchas células y fibras de soporte, permitiendo la construcción de estructuras mayores y más robustas, como válvulas cardíacas, modelos de tumores hepáticos o redes vasculares. Una clase más reciente, llamada fotopolimerización en cubeta, proyecta luz con patrones en un líquido para solidificar formas complejas sin forzar las células a través de boquillas. Variantes de este método pueden esculpir características a escala micrónica, imprimir un órgano pequeño entero en segundos o incluso conformar tejidos dentro de un baño transparente, todo ello manteniendo las células vivas.
Reemplazando y refinando las pruebas de fármacos
Estos tejidos impresos ya se están usando para replantear la cadena de desarrollo farmacéutico. En el descubrimiento temprano, construcciones específicas de pacientes o enfermedades —como modelos tumorales bioimpresos— permiten a los investigadores probar muchos candidatos a fármaco en entornos 3D realistas que se parecen más a la enfermedad humana que las capas celulares planas en una placa. En las pruebas preclínicas, tejidos impresos de piel, pulmón e hígado demuestran ser más precisos que los animales para detectar toxicidades o efectos secundarios específicos humanos. Algunos estudios van más allá e imprimen "ensayos clínicos en un chip", donde tejidos fabricados con células de distintos donantes se exponen en paralelo a un fármaco, revelando quién podría beneficiarse o verse perjudicado. Los reguladores ahora animan a las empresas a presentar datos de estos modelos junto con estudios en animales, acumulando la evidencia necesaria para una aceptación más amplia.
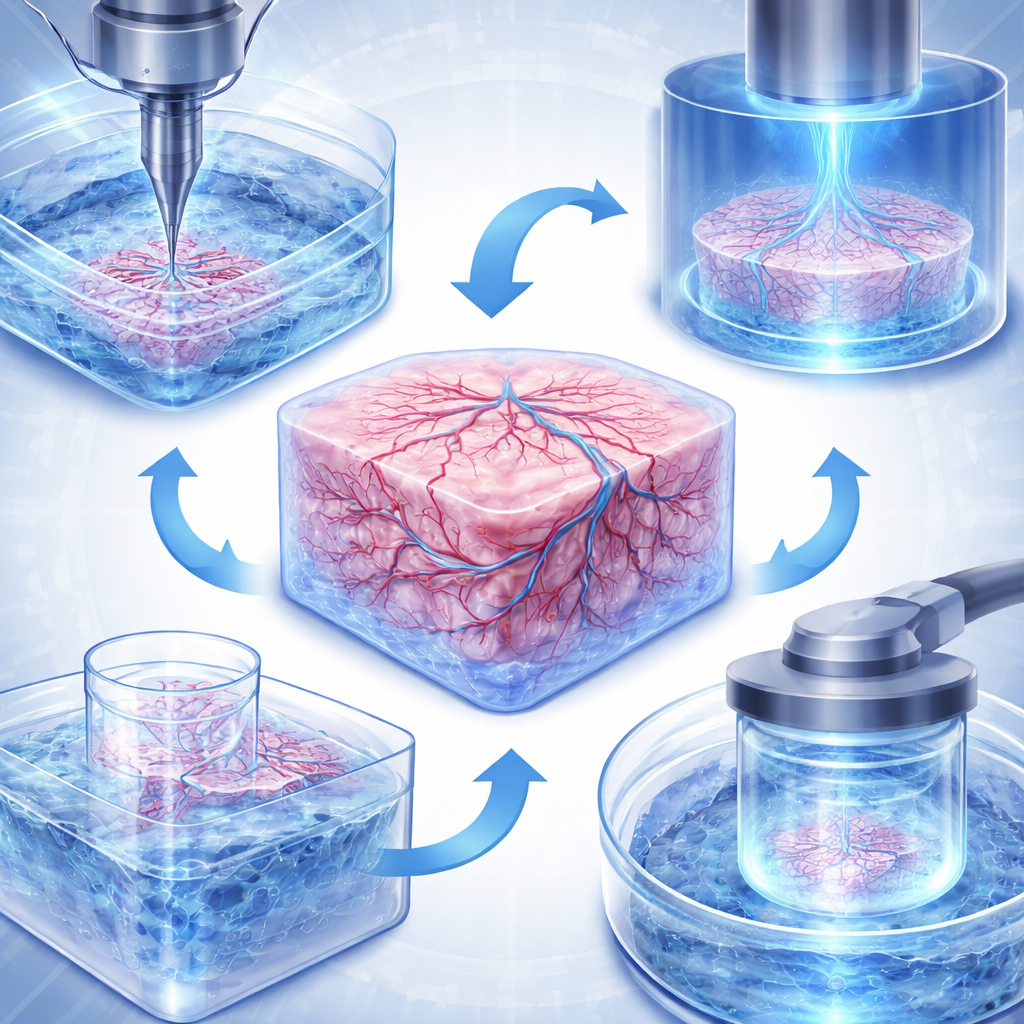
Ingeniería de órganos sin un cuerpo
A pesar del rápido avance, todavía existen varios obstáculos antes de que los tejidos bioimpresos puedan sustituir de forma rutinaria las pruebas en animales. Un desafío principal es el suministro sanguíneo: los órganos reales contienen redes de vasos que van desde grandes arterias hasta capilares del grosor de un cabello, mientras que las construcciones impresas deben superar un límite natural sobre la distancia a la que pueden difundirse oxígeno y nutrientes. Los investigadores abordan esto con nuevas estrategias de impresión que crean canales ramificados, con baños de soporte que mantienen los tejidos blandos en su lugar mientras se forman diminutos vasos, y con impresoras volumétricas ultrarrápidas que fabrican estructuras gruesas y densas en células antes de que estas empiecen a sufrir. Otro reto es el realismo: los tejidos vivos son mezclas de muchos tipos celulares bañadas en señales químicas complejas y, a menudo, influidas por el microbioma y órganos distantes. Los modelos avanzados ahora combinan múltiples poblaciones celulares, gradientes controlados de oxígeno y pH e incluso sistemas "multi-órgano" conectados que enlazan tejidos de intestino, hígado, sistema inmune y cerebro mediante flujo de fluidos para imitar respuestas de todo el cuerpo.
Un futuro humano y predictivo para el desarrollo de fármacos
En conjunto, estos avances apuntan a un futuro en el que modelos de tejido humanos de alta fidelidad se conviertan en el núcleo de cómo evaluamos los medicamentos. El artículo concluye que la bioimpresión 3D está pasando de ser una técnica de laboratorio de nicho a una herramienta central para construir sistemas de prueba estandarizados y aptos para reguladores. Para realizar plenamente esta promesa, científicos y reguladores deben ponerse de acuerdo sobre dónde y cómo deben usarse estos modelos, demostrar que predicen de forma fiable los resultados humanos y resolver los retos técnicos pendientes, como construir una vasculatura estable y órganos anatómicamente complejos. Si lo logran, este cambio podría reducir la dependencia de las pruebas en animales, recortar costosos fracasos en etapas tardías del desarrollo farmacéutico y ofrecer terapias más seguras y eficaces, reflejando mejor la biología que más importa: la nuestra.
Cita: Hua, W., Gaharwar, A.K. 3D biofabricated in vitro models as new approach methodologies for animal alternatives. npj Biomed. Innov. 3, 20 (2026). https://doi.org/10.1038/s44385-026-00073-x
Palabras clave: bioimpresión 3D, alternativas a la experimentación animal, desarrollo de fármacos, modelos de tejido, bioimpresión volumétrica