Clear Sky Science · es
Ingeniería de macrófagos para la inmunoterapia del cáncer: conocimientos emergentes y potencial terapéutico
Convertir al equipo de limpieza del cuerpo en combatientes contra el cáncer
Nuestros cuerpos están llenos de macrófagos: células “limpiadoras” que patrullan y devoran gérmenes y tejido muerto. Este artículo de revisión explora cómo los científicos aprenden a redirigir estas células contra el cáncer. Dado que los macrófagos son abundantes dentro de los tumores, incluidos aquellos que resisten las inmunoterapias líderes actuales, comprenderlos e ingeniería-los podría abrir nuevas opciones para pacientes con cánceres de difícil tratamiento.
Las muchas caras de un mismo tipo celular
Los macrófagos no son un único tipo celular fijo; son capaces de cambiar de forma. Pueden llegar desde el torrente sanguíneo o residir ya en los tejidos, y una vez establecidos responden a señales locales. En los tumores, estos macrófagos asociados al tumor pueden tanto ayudar a destruir células cancerosas como, de forma sorprendente, favorecer el crecimiento y la diseminación tumoral. Anteriormente, los investigadores intentaron encajonarlos en dos categorías: “M1” (modo de ataque) y “M2” (modo reparación o apoyo). Nuevas herramientas de cartografía genética y espacial muestran ahora un espectro mucho más rico de estados, con múltiples subgrupos y comportamientos que varían según el tumor y la localización. Incluso células que antes se consideraban firmemente “protumorales” pueden, en ciertos contextos, activar linfocitos T y apoyar la inmunidad antitumoral.
Sensando su entorno y devorando células cancerosas
Los macrófagos no solo escuchan señales químicas; también perciben el mundo físico que los rodea. Al desplazarse por la densa malla de proteínas de un tumor, apretarse entre células y soportar fuerzas fluidas, detectan rigidez y tensión mediante receptores especializados como Piezo1. Estas señales mecánicas, junto con las señales inmunes clásicas, pueden inclinar a los macrófagos hacia roles más inflamatorios o más calmantes. Funcionalmente, los macrófagos pueden engullir células cancerosas, trocearlas y presentar fragmentos (antígenos) a los linfocitos T, conectando la inmunidad innata y adaptativa. Las células tumorales se defienden enviando señales de “no me comas”, notablemente a través de la molécula de superficie CD47, que activa un freno en los macrófagos. Fármacos que bloquean esta interacción están en numerosos ensayos clínicos, aumentando la eliminación de células cancerosas pero requiriendo un ajuste cuidadoso para evitar dañar células sanas.
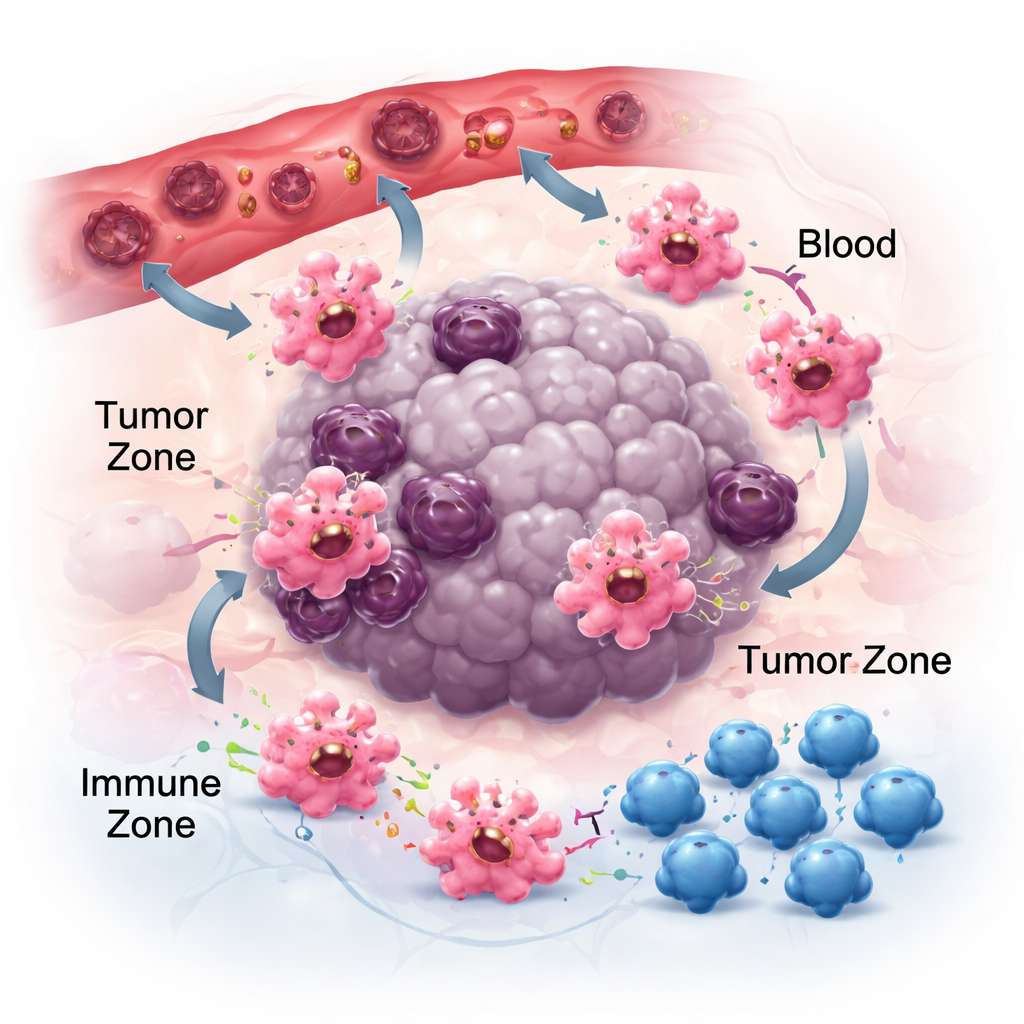
Moverse, adherirse y comunicarse en el vecindario tumoral
Para ser relevantes en el cáncer, los macrófagos deben primero alcanzar los tumores y luego posicionarse en los nichos adecuados. Siguen rastros químicos—quimioquinas y factores de crecimiento—liberados por las células tumorales y las adyacentes. Pares como CCR2–CCL2 ayudan a atraerlos al tumor, y fármacos que bloquean estas señales pueden reducir la acumulación de macrófagos, aunque no por completo, lo que señala la existencia de otros atractivos como CSF-1 y VEGF. Una vez en su lugar, la forma en que los macrófagos se adhieren a la matriz local también condiciona su comportamiento. Sus receptores de adhesión, llamados integrinas, no solo actúan como pegamento; amplifican señales inflamatorias y pueden empujar a las células hacia estados más antitumorales. Al mismo tiempo, los macrófagos liberan minúsculos paquetes llamados vesículas extracelulares que transportan ARN y proteínas a células vecinas. Según el tipo de tumor, estas vesículas pueden aplanar la respuesta inmune y facilitar la diseminación o, por el contrario, reforzar respuestas antitumorales, lo que subraya la naturaleza dependiente del contexto de la comunicación de los macrófagos.
Reprogramar macrófagos con genes y materiales
Dado que los macrófagos infiltran naturalmente tumores sólidos mejor que muchas células T, los investigadores los están reingenierizando como medicamentos vivos. Una estrategia genética toma prestado el enfoque de la terapia con receptores quiméricos de antígeno (CAR) en células T: añadir un receptor sintético para crear macrófagos CAR (CAR-M). Estas células diseñadas reconocen marcadores tumorales, engullen células cancerosas con mayor eficiencia, digieren la matriz circundante, liberan señales inflamatorias y activan linfocitos T presentando antígenos tumorales. Ensayos humanos iniciales de CAR-M dirigidos a HER2 muestran seguridad y actividad biológica alentadoras, aunque se necesita más trabajo para demostrar beneficios fuertes y duraderos. En paralelo, enfoques no genéticos usan partículas y “mochilas” hechas de lípidos o polímeros. Los macrófagos pueden tragarse nanopartículas cargadas de fármacos y transportarlas hasta el interior de los tumores como caballos de Troya, o portar parches adheridos a la superficie que liberan lentamente señales que refuerzan la inmunidad, ayudándoles a mantener una identidad antitumoral sin sobrecargar su interior. Las vesículas derivadas de macrófagos también se prueban como vehículos de entrega naturales y sin células.
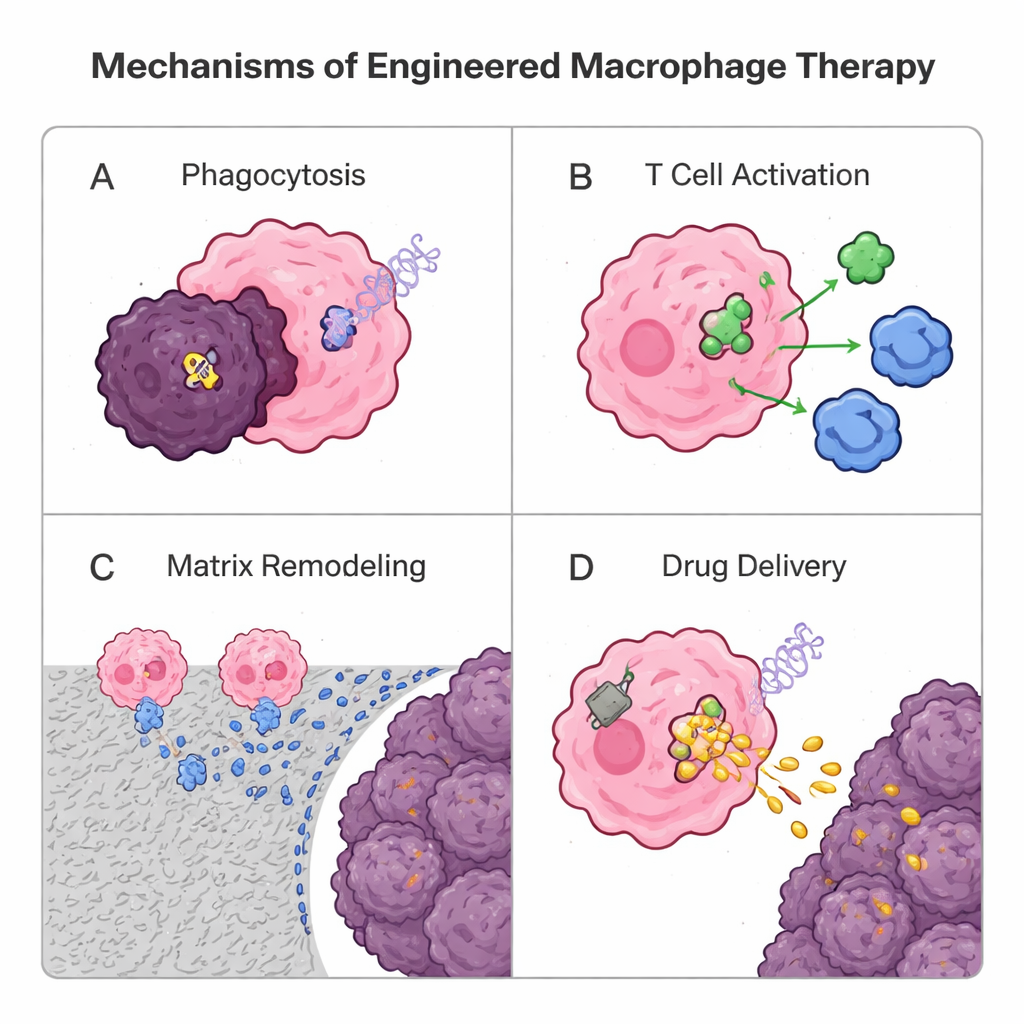
Retos por delante y motivos de esperanza
A pesar de su promesa, las terapias con macrófagos deben superar obstáculos prácticos. Generar una cantidad suficiente de células homogéneas a partir de pacientes es costoso y lento, y una vez infundidas, estas células no viven ni se multiplican indefinidamente. Su flexibilidad innata, aunque biológicamente útil, puede dificultar mantenerlas en un modo antitumoral dentro de un microambiente tumoral complejo y supresor. Los autores sostienen que modelos bioingenierizados avanzados—cultivos 3D, organoides y sistemas organ-on-a-chip que imitan la mecánica real de los tejidos—serán cruciales para entender y predecir el comportamiento de macrófagos ingenierizados en pacientes. Aun así, su capacidad natural para penetrar tumores sólidos, devorar células cancerosas y despertar linfocitos T, combinada con un historial inicial de seguridad, sugiere que las terapias basadas en macrófagos podrían convertirse en un arma importante, especialmente contra tumores “fríos” que actualmente resisten la mayoría de los tratamientos inmunológicos.
Cita: Block, A., Liu, X., Zhang, D. et al. Engineering macrophages for cancer immunotherapy: emerging insights and therapeutic potential. npj Biomed. Innov. 3, 18 (2026). https://doi.org/10.1038/s44385-026-00072-y
Palabras clave: inmunoterapia con macrófagos, microambiente tumoral, macrófagos CAR, fagocitosis, entrega de fármacos con nanopartículas