Clear Sky Science · es
Andamio electrohilado modificado en superficie soporta la función de células madre limbares derivadas de iPSC
Dar una segunda oportunidad a la vista
Cuando la ventana transparente en la parte frontal del ojo —la córnea— resulta dañada, las personas pueden perder la visión de forma permanente. Un factor determinante es la pérdida de unas células especiales en el borde de la córnea, llamadas células madre limbares, que normalmente mantienen la superficie clara y lisa. Este artículo describe un nuevo “vendaje vivo” fabricado en laboratorio que algún día podría transportar células madre de reemplazo al ojo y ayudar a restaurar la vista de forma más segura y fiable que los métodos actuales.
Por qué importa el borde del ojo
La córnea está formada por varias capas y debe permanecer lisa y transparente para desviar la luz correctamente. Un pequeño anillo de células madre situado en la frontera entre la córnea clara y la parte blanca del ojo renueva constantemente su capa más externa. Una lesión, infección o enfermedad autoinmune puede destruir estas células madre limbares, provocando una condición conocida como deficiencia de células madre limbares. Sin ellas, los vasos sanguíneos crecen hacia la córnea, normalmente transparente, la superficie se cicatriza y se vuelve irregular, y los pacientes pueden sufrir una pérdida grave de visión o ceguera. Los médicos pueden trasplantar células madre sanas, pero todavía necesitan un portador seguro, resistente y transparente para entregar estas células frágiles al ojo dañado.
Construir un “vendaje vivo” sintético
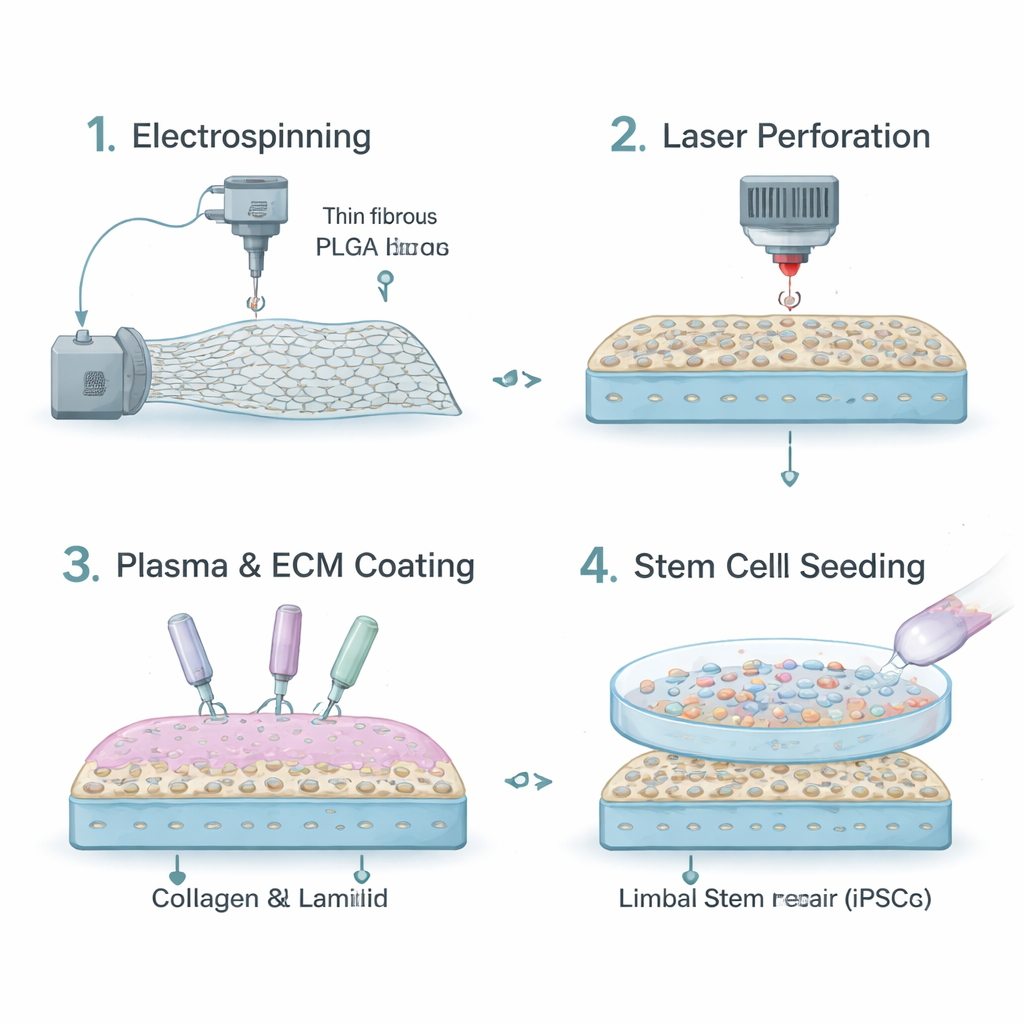
Hoy en día, muchos cirujanos confían en tejidos naturales como la membrana amniótica o láminas de colágeno como portadores. Aunque estos materiales son biocompatibles, varían entre donantes, pueden escasear y no permiten un control preciso sobre su duración o rigidez. Los investigadores recurrieron en su lugar a un plástico biodegradable llamado PLGA, ya utilizado en algunos dispositivos médicos. Mediante una técnica llamada electrospinning, estiraron el PLGA hasta formar una malla de fibras diminutas que recuerda a la capa de soporte natural del ojo. Esta lámina fibrosa es lo bastante resistente para manipularse durante la cirugía y puede ajustarse para disolverse lentamente a medida que el ojo se cura.
Hacer el andamio compatible con las células y transparente
Sin embargo, el PLGA simple repele el agua y no atrae células de forma natural. Para hacer su superficie más acogedora, el equipo trató las fibras con plasma atmosférico, que añade grupos químicos capaces de captar proteínas. A continuación recubrieron el andamio con colágeno IV y laminina‑521, dos componentes clave del “hogar” natural de las células madre alrededor de la córnea. Para mejorar la transparencia, utilizaron un láser preciso para perforar la membrana con agujeros microscópicos. Estas microperforaciones aumentaron la cantidad de luz que atraviesa el andamio de aproximadamente un 44% a cerca de un 60%, acercándolo a la claridad de una córnea real mientras se mantienen suficientes fibras intactas para la adhesión celular.
Probar células madre en la nueva superficie
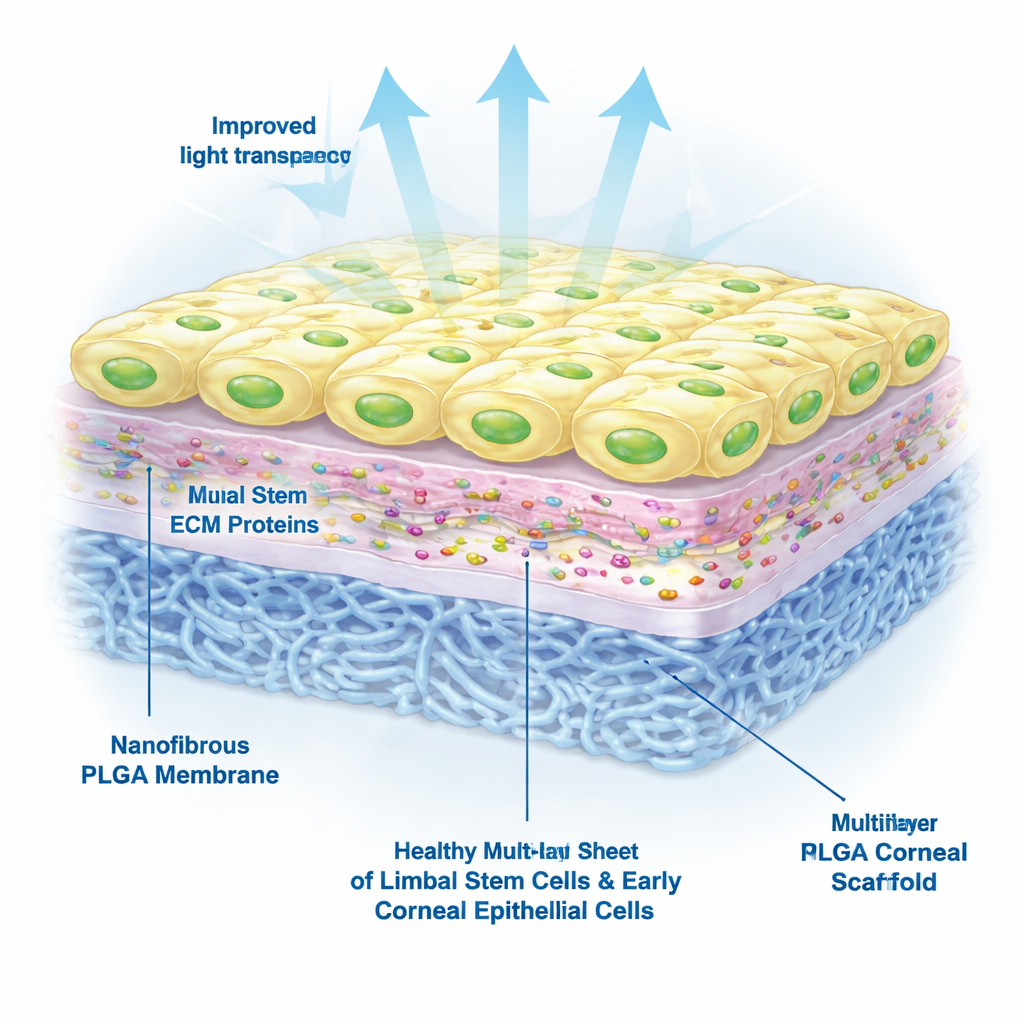
El equipo probó a continuación cómo crecían las células madre limbares derivadas de células madre pluripotentes inducidas —células adultas reprogramadas a un estado flexible similar al de las células madre— sobre el andamio. Compararon distintos tratamientos de superficie y hallaron que la laminina‑521 era esencial: los andamios tratados con plasma y recubiertos con laminina‑521, con o sin colágeno IV, favorecieron una buena adhesión, supervivencia y proliferación celular durante al menos una semana. En contraste, las células colocadas sobre PLGA sin tratar o sobre PLGA recubierto solo con colágeno IV a menudo morían o se desprendían. Bajo el microscopio, las células en el andamio optimizado formaron láminas densamente empaquetadas, en “adoquines”, similares a una superficie corneal normal.
Mantener a las células madre en un estado listo para reparar
Más allá de simplemente sobrevivir, las células trasplantadas deben permanecer en un estado en el que puedan renovarse y al mismo tiempo generar nuevas células de la superficie corneal. Los investigadores emplearon tinción de proteínas y pruebas genéticas para examinar la identidad de las células en su andamio. Encontraron señales fuertes de marcadores asociados con células madre limbares y células corneales tempranas, y solo señales débiles de marcadores de células totalmente maduras. Este patrón sugiere una mezcla saludable de células madre activas y células hijas tempranas preparadas para reconstruir la superficie corneal, en lugar de una población agotada o envejecida.
Qué podría significar esto para los pacientes
En conjunto, el estudio muestra que un andamio completamente sintético y cuidadosamente diseñado puede imitar muchas características del microambiente natural de las células madre del ojo. Al combinar un material fibroso ajustable, microperforaciones para mejorar la visión y un recubrimiento proteico que apoya específicamente a las células madre limbares, los autores crearon un portador prometedor para futuros trasplantes de células madre. Aunque este trabajo se realizó en laboratorio y aún quedan ensayos en animales y clínicos por delante, el enfoque podría ofrecer finalmente una forma más consistente, escalable y personalizada de restaurar una superficie corneal clara y sana y ayudar a personas con pérdida de visión hasta ahora intratable a recuperar la vista.
Cita: Mahmood, N., Zha, D., Gullion, S. et al. Surface modified electrospun scaffold supports iPSC-derived limbal stem cell function. npj Biomed. Innov. 3, 14 (2026). https://doi.org/10.1038/s44385-026-00066-w
Palabras clave: regeneración corneal, células madre limbares, andamio electrohilado, biomateriales, células madre pluripotentes inducidas