Clear Sky Science · es
Optimización de la inducción de inflamación en organoides epiteliales intestinales derivados de lactantes prematuros
Por qué esto importa para los recién nacidos frágiles
Los bebés que nacen muy prematuros afrontan una combinación peligrosa: un intestino inmaduro y una comunidad microbiana que cambia rápidamente. Juntos, estos factores pueden desencadenar una inflamación descontrolada que daña el intestino y conduce a condiciones potencialmente mortales, como la enterocolitis necrotizante. Dado que no es posible experimentar directamente con bebés prematuros, los científicos necesitan modelos de laboratorio realistas de sus intestinos para probar qué impulsa la inflamación y cómo detenerla. Este estudio refina uno de esos modelos usando pequeños tejidos intestinales cultivados en el laboratorio, ofreciendo una forma más clara de investigar qué señales microbianas inclinan la balanza desde la defensa normal hacia una inflamación perjudicial.
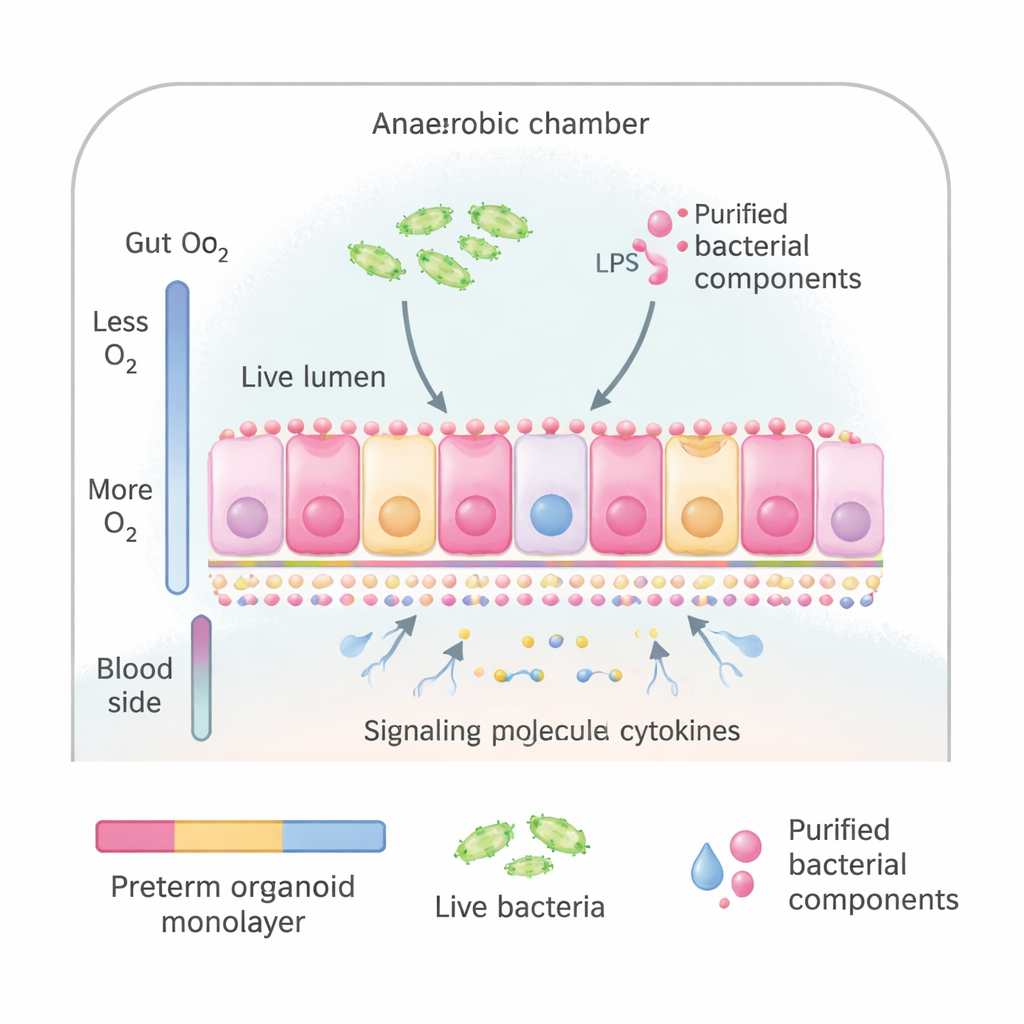
Cultivar un intestino prematuro en una placa
Los investigadores emplearon organoides intestinales: versiones en miniatura del revestimiento intestinal cultivadas a partir de células madre obtenidas de lactantes prematuros durante cirugías. Estos organoides pueden aplanarse hasta formar una lámina delgada de células que se parece y actúa como la superficie interna del intestino delgado, incluyendo la orientación correcta de la cara superior (hacia el contenido intestinal) y la inferior (hacia el torrente sanguíneo). El equipo colocó estas láminas en un sistema de cultivo especial que imita el gradiente de oxígeno natural del intestino: bajo en el lado expuesto a los microbios y más alto en el lado sanguíneo. Esto les permitió exponer la superficie «intestinal» ya sea a bacterias enteras tomadas de bebés prematuros o a componentes bacterianos purificados que se sabe activan el sistema inmune.
Probar qué desencadena mejor la alarma inflamatoria
Los científicos compararon varias maneras de provocar inflamación: una mezcla de bacterias vivas comúnmente halladas en lactantes prematuros enfermos; las mismas bacterias muertas por calor; y dos señales bacterianas purificadas, lipopolisacárido (LPS) de las paredes celulares y flagelina de los filamentos bacterianos. Midieron la liberación de IL‑8, una proteína señalizadora que atrae células inmunitarias y sirve como marcador general de inflamación, y usaron análisis proteómico a gran escala para ver cómo cambiaba la maquinaria interna de las células intestinales. Sorprendentemente, las bacterias vivas o muertas no aumentaron significativamente la IL‑8 en este sistema, ni siquiera tras 24 horas. En contraste, la flagelina y, especialmente, la combinación de flagelina y LPS desencadenaron un aumento claro de IL‑8 en tan solo tres horas, mostrando que estas señales purificadas podían activar de forma fiable un estado inflamatorio.
Encontrar la configuración más realista y eficiente
Para ajustarlo mejor a la biología intestinal real, el equipo prestó atención a dónde actúa naturalmente cada señal. El LPS suele detectarse en el lado del epitelio que mira al contenido intestinal, mientras que la flagelina se percibe principalmente por el lado tisular. Usando dosis mucho más bajas y más fisiológicas que en experimentos anteriores, aplicaron LPS en el lado superior (orientado al lumen) y flagelina en el lado inferior (orientado a la sangre) de la lámina de organoide. Este sencillo cambio produjo una respuesta fuerte y amplia en tres horas: múltiples mensajeros inflamatorios —incluida la IL‑8, TNF y varias quimiocinas— se secretaron desde ambos lados del tejido. Al mismo tiempo, cientos de proteínas celulares variaron en abundancia, indicando una activación a gran escala de rutas defensivas.
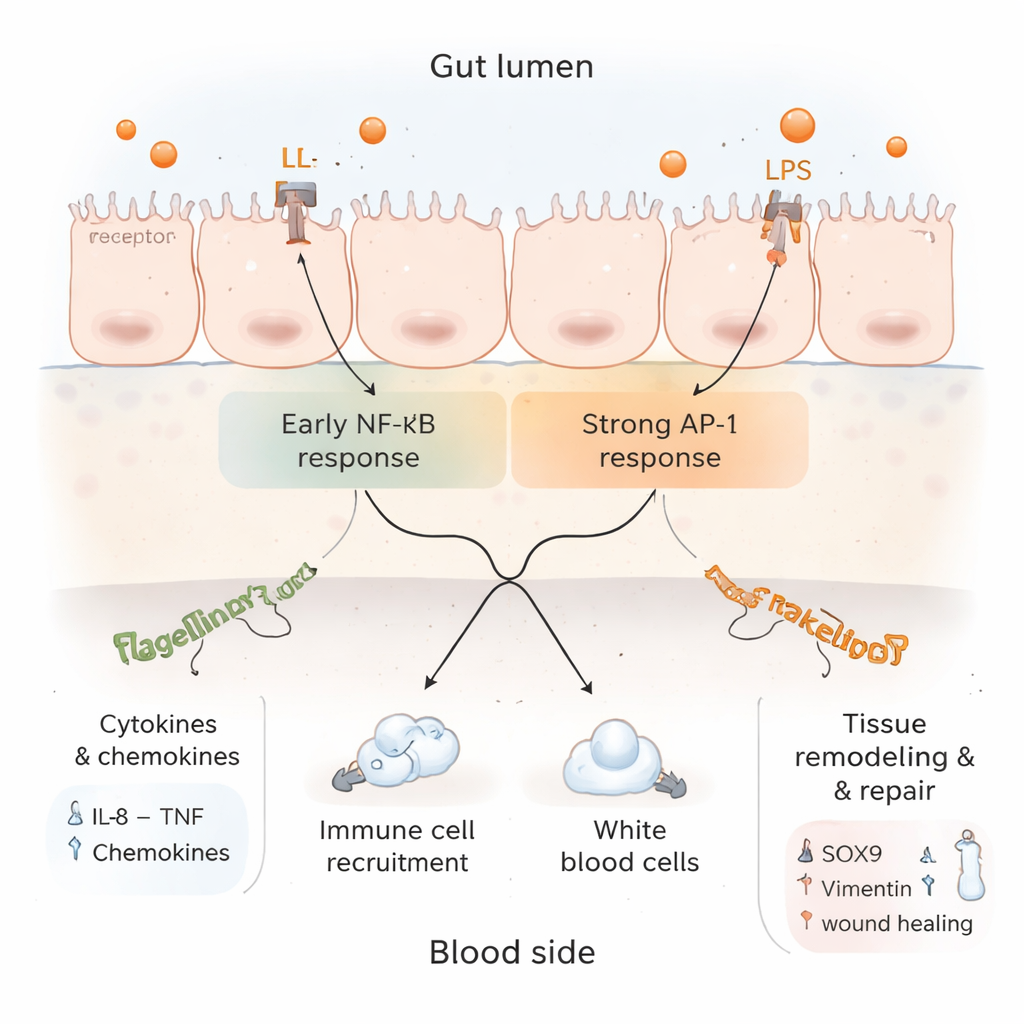
Inflamación, frenos y reparación en el mismo modelo
Al profundizar en los datos proteómicos, los investigadores hallaron un panorama complejo. Por un lado, se incrementaron marcadores de inflamación activa y de reclutamiento de células inmunitarias, y se activaron vías de señalización vinculadas a TNF e IL‑17 —ambas centrales en la defensa intestinal—. Por otro lado, varios componentes de la vía clásica NF‑κB, que impulsa muchos genes inflamatorios, se redujeron, mientras que una vía alternativa que involucra AP‑1 permaneció activa. Esto sugiere que, tras una alarma inicial, el tejido comienza a aplicar frenos para evitar un daño incontrolado. Al mismo tiempo, aumentaron proteínas asociadas con regeneración tisular, remodelado estructural y muerte celular controlada, lo que insinúa que el revestimiento intestinal no solo estaba inflamado, sino también intentando remodelarse y curarse.
Qué significa esto para futuros tratamientos
Al comparar sistemáticamente distintos estímulos microbianos, dosis, posiciones y tiempos de exposición, los autores concluyen que una exposición de tres horas a LPS en dosis bajas en el lado intestinal junto con flagelina en el lado sanguíneo es la forma más robusta y reproducible de inducir inflamación en organoides intestinales derivados de prematuros. Este modelo refinado captura no solo el estallido inflamatorio, sino también los mecanismos de freno integrados, la tolerancia y las respuestas de reparación del frágil intestino prematuro. Proporciona una hoja de ruta práctica para que otros laboratorios estudien cómo microbios específicos, fármacos o factores nutricionales podrían empeorar o calmar la inflamación intestinal en bebés muy prematuros —un paso esencial hacia estrategias más seguras y específicas para prevenir enfermedades intestinales devastadoras en este grupo vulnerable.
Cita: Chapman, J.A., Frey, A.M., Dueñas, M.E. et al. Optimising the induction of inflammation within preterm infant-derived intestinal epithelial organoids. npj Gut Liver 3, 5 (2026). https://doi.org/10.1038/s44355-026-00054-2
Palabras clave: intestino de lactante prematuro, organoides intestinales, inflamación intestinal, microbioma, enterocolitis necrotizante