Clear Sky Science · es
Transducción quimio-mecánica fuera de equilibrio del desenrollado de proteínas impulsado por ATP en el proteasoma 26S
Cómo una pequeña máquina mantiene nuestras proteínas en orden
Dentro de cada célula, un triturador microscópico llamado proteasoma 26S destruye constantemente proteínas dañadas o que ya no son necesarias, manteniendo la célula sana. En el centro de esta máquina hay un motor en forma de anillo que quema combustible químico (ATP) para agarrar, desenrollar y tirar de las proteínas hacia una cámara central donde se descomponen. Este artículo utiliza simulaciones por ordenador avanzadas para revelar cómo ese motor convierte la energía química en movimiento mecánico, ofreciendo una imagen detallada y cuantitativa de un proceso que sustenta el envejecimiento, las enfermedades cerebrales, la inmunidad y el cáncer.
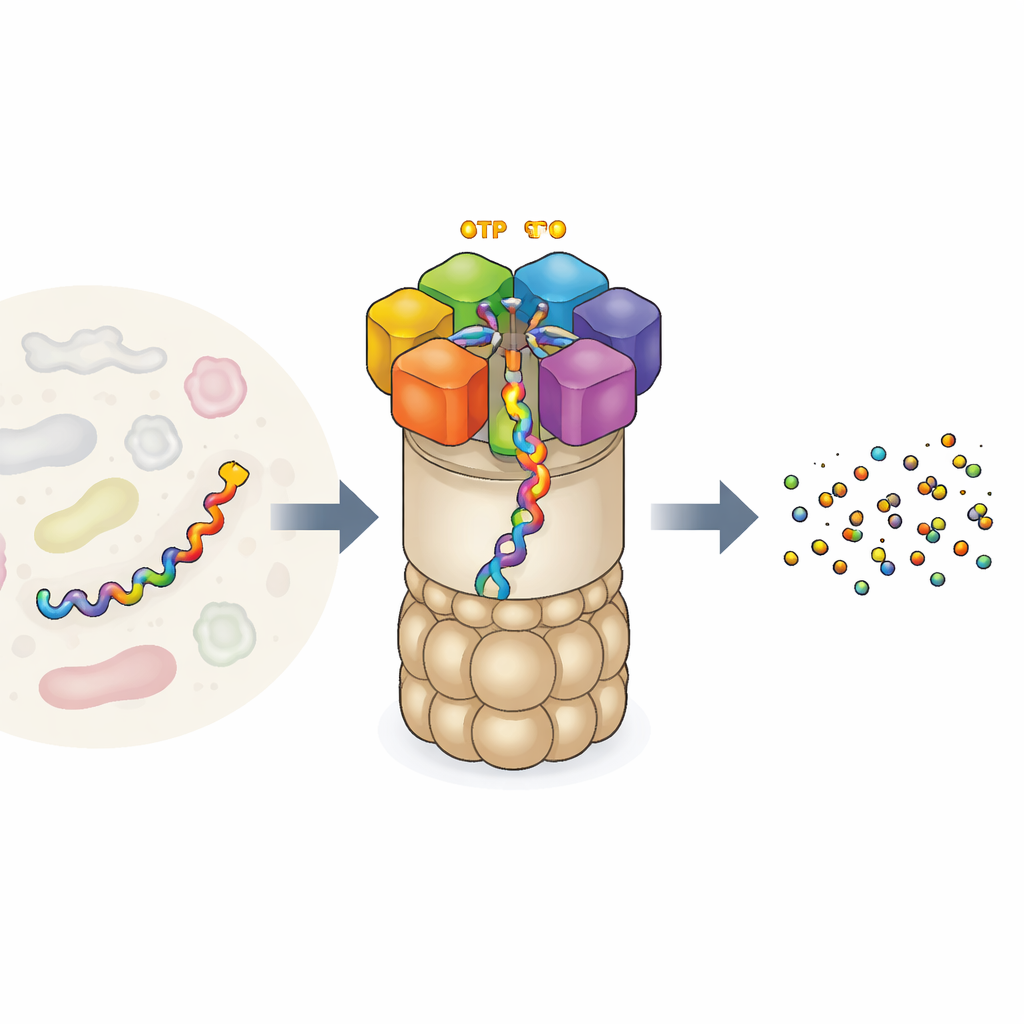
La fábrica de reciclaje de proteínas de la célula
El proteasoma 26S es una de las máquinas proteicas más grandes e intrincadas de nuestras células. Consiste en un núcleo con forma de barril que corta proteínas y una tapa reguladora que reconoce qué proteínas destruir. En la entrada se sitúa un anillo de seis unidades motoras diferentes. Cada unidad puede enlazar ATP, la moneda energética universal de la célula, y usa esa energía para agarrar una cadena proteica y tirarla hacia el núcleo para su descomposición. Este motor no actúa al azar: experimentos anteriores sugerían que las seis unidades trabajan de forma coordinada «mano a mano», pasando la proteína como escaladores en una cuerda. Pero los experimentos solo pudieron captar unas pocas instantáneas de esta acción, dejando preguntas abiertas sobre la secuencia completa de movimientos y cómo exactamente la quema de combustible se vincula al trabajo mecánico.
Simulando un tira y afloja molecular
Los autores construyeron un modelo probabilístico por ordenador que trata al motor como un sistema que salta entre muchas formas posibles mientras moléculas de ATP y sus productos se unen y separan. Definieron 30 conformaciones principales del anillo en las que una, dos o tres subunidades del motor pierden su agarre sobre la proteína, además de un estado especial muy cerrado en el que las seis sujetan la cadena. Usando un algoritmo estándar para simular eventos químicos aleatorios, siguieron cientos de miles de pasos en los que ocurren la unión de ATP, la ruptura de ATP y los cambios de forma del motor. A partir de estas ejecuciones pudieron predecir con qué rapidez se tira de una proteína en distintas condiciones, como variaciones en la cantidad de ATP, su forma gastada ADP, y un análogo de ATP no rompible que suele emplearse en experimentos.
Cuando demasiado combustible hace que el motor vaya más despacio
Las simulaciones reprodujeron varios hallazgos experimentales desconcertantes. Cuando los niveles de ATP aumentan desde valores bajos, el motor tira de las proteínas más rápido, porque la unión del combustible es el paso más lento. Pero más allá de aproximadamente 1 milimolar de ATP, la velocidad alcanza un pico y luego cae: el anillo pasa más tiempo en una conformación atascada y no translocante en la que las seis subunidades están ocupadas por ATP pero la proteína no se mueve. Añadir ADP o el análogo no rompible de ATP ralentiza el motor de forma constante, porque estas moléculas compiten con el ATP por los sitios de unión pero no pueden completar el golpe de fuerza. El modelo también predice cómo se comporta el motor cuando encuentra regiones de una proteína muy fuertemente plegadas, que actúan como obstáculos. En esos casos, el motor pasa más tiempo luchando contra la resistencia y la tasa global de degradación baja, coincidiendo con mediciones en dominios proteicos artificialmente estabilizados.
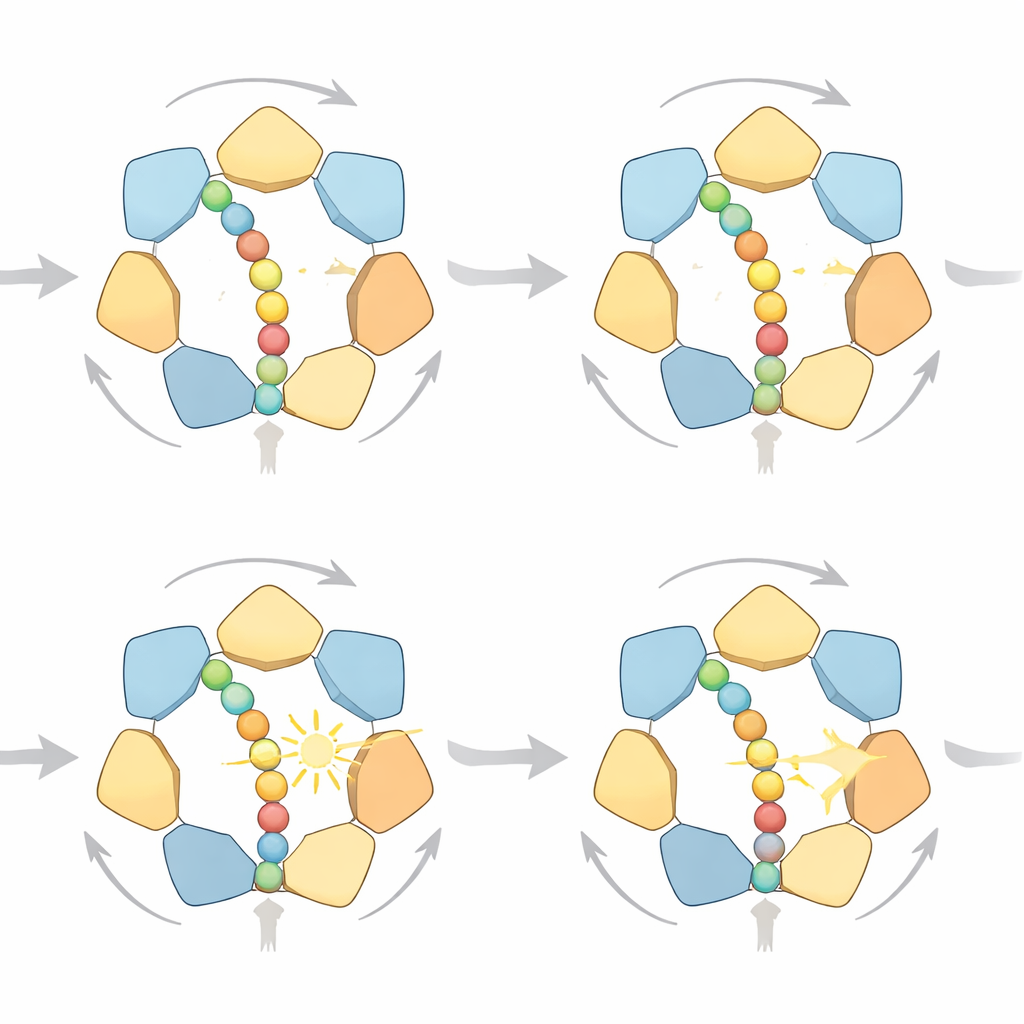
Muchas maneras de dar un paso
Al examinar las trayectorias simuladas en detalle, los investigadores encontraron que el anillo no sigue un único ciclo rígido. En su lugar, existen múltiples vías de alta probabilidad que todas respetan la misma regla direccional «mano a mano»: las subunidades cercanas a la salida del anillo liberan la proteína tras la ruptura del ATP, se desplazan a la parte superior de una escalera en espiral de subunidades y vuelven a agarrar la cadena más arriba. A veces la proteína avanza un paso pequeño, a veces dos, en función de cuántas subunidades se sueltan a la vez. Con abundante combustible, predominan los movimientos de un paso porque desperdician menos trabajo frente a fuerzas opuestas; cuando el combustible escasea, el modelo predice saltos de dos pasos más frecuentes. Las simulaciones también conectan la carga mecánica con el estado químico del motor: a medida que aumenta la resistencia y la proteína se bloquea, el ADP tiende a acumularse en más de los seis sitios de unión—exactamente lo que observan los estudios estructurales de alta resolución.
Uso de energía y reglas de diseño compartidas
El modelo permite a los autores mapear cómo aumenta la energía del motor cuando se rompe el ATP y cómo disminuye cuando esa energía se transforma en movimiento. Calculan una curva de eficiencia que muestra que el motor funciona mejor frente a una fuerza opuesta intermedia: muy poca resistencia y quema ATP de forma derrochadora; demasiada y casi se paraliza. Cuando el equipo comparó sus predicciones con datos de máquinas relacionadas que destruyen proteínas en bacterias y levaduras, encontraron tendencias muy similares sobre cómo un análogo de ATP no rompible ralentiza estos motores. Esto sugiere que muchos miembros de la misma familia de enzimas en forma de anillo probablemente comparten un mecanismo común y conservado para tirar de las proteínas.
Por qué esto importa para la salud y la enfermedad
Al convertir instantáneas estructurales dispersas y mediciones bioquímicas en un marco único y verificable, este trabajo muestra en detalle cuantitativo cómo un diminuto motor molecular traduce combustible químico en fuerza para reciclar las proteínas de la célula. El modelo no solo explica una amplia gama de experimentos existentes, sino que también hace predicciones sobre cómo cambios en los niveles de combustible, la carga mecánica o mutaciones en el motor podrían alterar la destrucción de proteínas. Dado que máquinas similares operan en todas las formas de vida y son centrales en condiciones que van desde la neurodegeneración hasta el cáncer, entender su funcionamiento interno a este nivel puede, en última instancia, guiar el diseño de fármacos que ajusten, potencien o bloqueen selectivamente a estos trituradores microscópicos.
Cita: Wu, D., Ouyang, Q., Wang, H. et al. Nonequilibrium chemomechanical transduction of ATP-driven protein unfolding in the 26S proteasome. npj Biol. Phys. Mech. 3, 4 (2026). https://doi.org/10.1038/s44341-026-00034-w
Palabras clave: proteasoma, motor AAA+ ATPasa, degradación de proteínas, máquinas moleculares, acoplamiento quimio-mecánico