Clear Sky Science · es
Detección ultrasensible de proteínas sin enzimas mediante inmunoensayo de proximidad con microscopía por resonador fotónico de absorción
Por qué importa encontrar trazas ínfimas de proteínas
Médicos e investigadores dependen cada vez más de las proteínas en sangre para alertar sobre cáncer, enfermedades cardiovasculares, infecciones o inflamación nociva mucho antes de que los síntomas sean graves. Pero muchas de estas señales moleculares aparecen en niveles tan bajos que las pruebas de laboratorio estándar actuales tienen dificultades para detectarlas con rapidez o a bajo coste. Este estudio presenta un nuevo método de ensayo, denominado PINATA, que puede identificar cantidades extremadamente pequeñas de una proteína asociada a la inflamación usando equipo simple y pasos a temperatura ambiente, abriendo la puerta a diagnósticos más accesibles y sensibles.
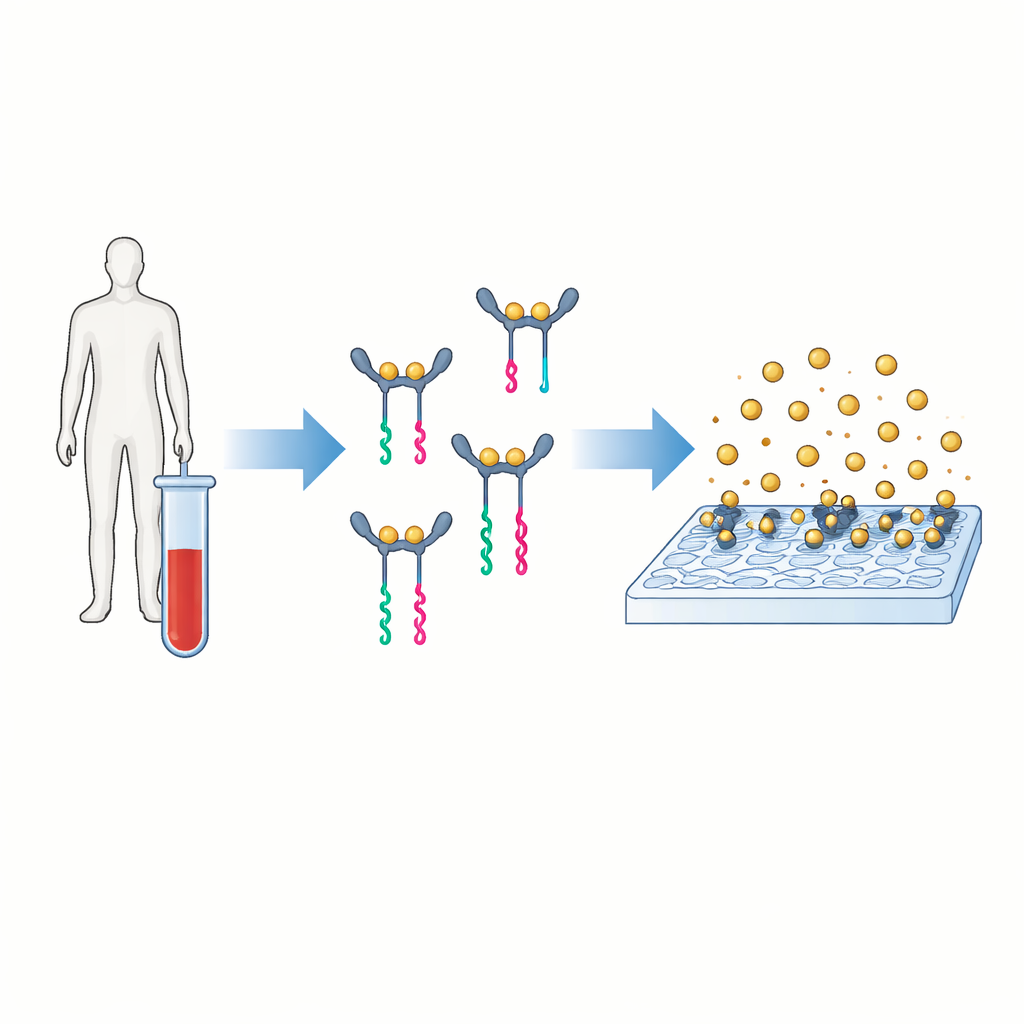
Una nueva forma de convertir proteínas en señales legibles
La idea central de PINATA es traducir la presencia de una proteína en un fragmento corto de ADN que es fácil de amplificar y contabilizar. Los autores se centran en la interleucina-6, una molécula mensajera en la sangre que aumenta en condiciones que van desde infecciones hasta cáncer. En las pruebas convencionales, dos anticuerpos se adhieren a la proteína y llevan una enzima que genera una señal coloreada o fluorescente. PINATA conserva la noción básica de dos anticuerpos reconociendo la misma proteína, pero en lugar de enzimas fija cadenas cortas de ADN a cada anticuerpo. Cuando ambos anticuerpos se unen a la misma proteína y quedan próximos, sus piezas de ADN colaboran para liberar un fragmento de ADN separado llamado reportero. Cada molécula de proteína puede así desencadenar la liberación de muchos reporteros de ADN idénticos.
Usar “normas de tráfico” del ADN en lugar de enzimas
En el corazón del método hay circuitos de ADN cuidadosamente diseñados que funcionan como sistemas moleculares de tráfico, indicando cuándo las hebras pueden unirse, separarse o intercambiarse. Estos circuitos están construidos de modo que, a menos que una proteína acerque las dos piezas de ADN unidas a los anticuerpos, el ADN reportero permanece bloqueado y no se genera señal. Cuando la proteína está presente, su acción de puente libera el reportero. Este reportero liberado participa entonces en un proceso secundario de amplificación sobre una superficie preparada. Allí, participa repetidamente en reacciones de intercambio de hebras que permiten que una sola molécula reportera reclute muchas nanopartículas de oro en la superficie, creando una señal digital intensa sin usar enzimas ni ciclos de temperatura.
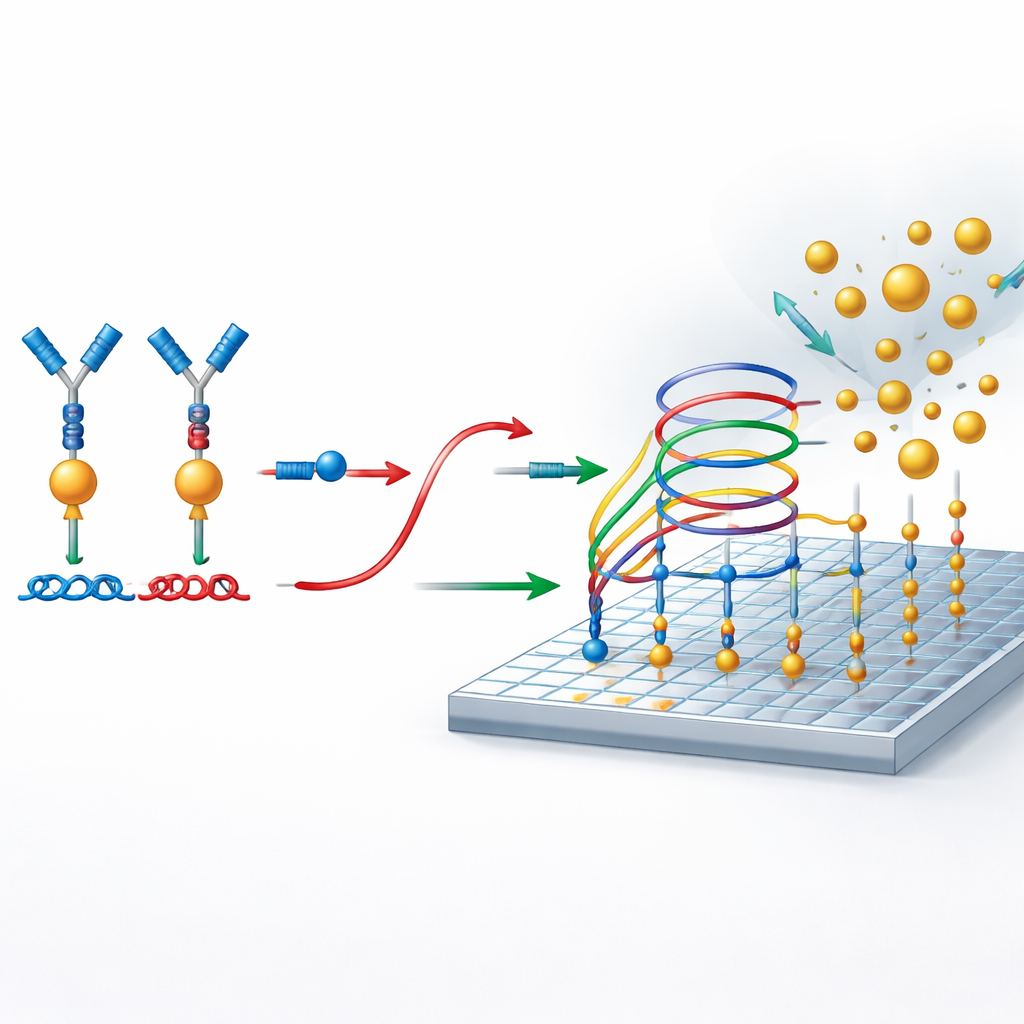
Contar nanopartículas individuales como eventos sí/no
Para leer el resultado, los investigadores usan microscopía por resonador fotónico de absorción, o PRAM. La superficie sensora es un material especialmente estructurado que refleja fuertemente la luz en un color particular. Cuando nanopartículas de oro aterrizan sobre esa superficie, absorben esa luz y aparecen como puntos oscuros en la imagen del microscopio. Dado que el sistema está diseñado para que las nanopartículas solo se unan cuando el ADN reportero está presente, cada punto oscuro representa un evento de detección exitoso vinculado a una molécula de proteína. A continuación se emplea una configuración óptica simple y de bajo coste y un software de procesamiento de imágenes para contar esos puntos en la superficie, convirtiendo el número de nanopartículas en una medida precisa de la concentración proteica.
¿Qué sensibilidad y selectividad tiene la prueba?
Con este enfoque, el equipo demuestra que pueden detectar interleucina-6 en niveles tan bajos como 37 femtogramos por mililitro —aproximadamente unas decenas de moléculas en una gota— a lo largo de un rango dinámico que abarca seis órdenes de magnitud. El ensayo funciona en un protocolo directo de dos pasos y 90 minutos realizado totalmente a temperatura ambiente. Los autores también muestran que la prueba mantiene precisión incluso cuando la interleucina-6 se mezcla en muestras complejas como suero y plasma humanos, que típicamente interfieren con mediciones sensibles. Además, confirman que los anticuerpos dirigidos a la interleucina-6 no responden a otras proteínas relacionadas, lo que subraya la selectividad del ensayo.
Qué podría significar esto para los diagnósticos futuros
Para un público no especializado, la conclusión clave es que PINATA ofrece una forma de detectar proteínas relacionadas con enfermedades a niveles extremadamente bajos usando un instrumento óptico compacto en lugar de aparataje de laboratorio voluminoso y caro. Al combinar circuitos de ADN inteligentes con el recuento digital de nanopartículas, el método evita enzimas frágiles y pasos de calentamiento, y aun así alcanza o supera la sensibilidad de muchas pruebas proteicas avanzadas. Con desarrollo adicional y adaptación a otros blancos, esta estrategia podría permitir diagnósticos más tempranos, monitorización más frecuente y pruebas en el punto de atención para una amplia gama de condiciones donde pequeños cambios en los niveles de proteínas tienen gran significado clínico.
Cita: Shepherd, S., Bhaskar, S., Xu, H. et al. Ultrasensitive non-enzymatic protein detection using proximity immunoassay with photonic resonator absorption microscopy. npj Biosensing 3, 21 (2026). https://doi.org/10.1038/s44328-026-00090-1
Palabras clave: detección de biomarcadores proteicos, diagnósticos ultrasensibles, desplazamiento de hebras de ADN, ensayo de interleucina-6, biosensado digital