Clear Sky Science · es
Vesículas extracelulares derivadas de neuronas y astrocitos, aisladas nanomagnéticamente en microfluidos, para diferenciar la enfermedad por cuerpos de Lewy y la enfermedad de Alzheimer
Por qué importa esto para familias y médicos
Demencia es un término paraguas que abarca varias enfermedades cerebrales con síntomas similares pero causas subyacentes muy diferentes. Dos de las más comunes, la enfermedad de Alzheimer y la enfermedad por cuerpos de Lewy, pueden parecer casi idénticas en la clínica, sin embargo responden de forma distinta a los fármacos y conllevan riesgos diferentes. Hoy en día, la única manera de saber con certeza qué enfermedad tuvo una persona es examinar el cerebro tras la muerte. Este estudio describe un nuevo tipo de análisis de sangre que lee pequeños mensajes liberados por las células cerebrales, con el objetivo de distinguir estas dos demencias mientras las personas aún están vivas.
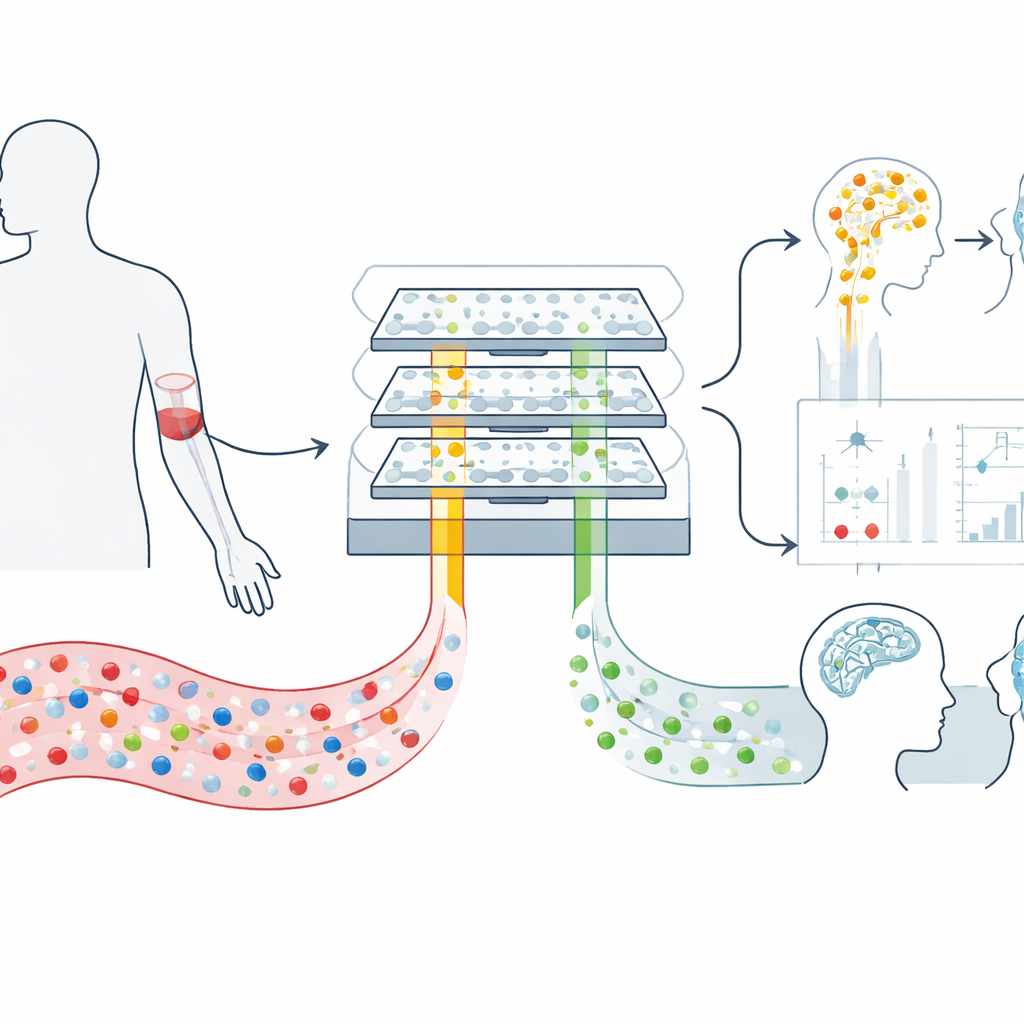
Pequeños paquetes que viajan del cerebro a la sangre
Nuestros cerebros desprenden constantemente burbujas microscópicas llamadas vesículas extracelulares hacia el torrente sanguíneo. Estas vesículas son como sobres acolchados enviados por las neuronas y sus células de soporte, que llevan fragmentos de material genético y proteínas que reflejan lo que ocurre dentro del cerebro. Debido a que pueden cruzar la barrera hematoencefálica y sobrevivir en circulación, ofrecen una ventana rara y mínimamente invasiva a la biología cerebral. El reto es que un mililitro de sangre contiene cientos de miles de millones de vesículas procedentes de todo el cuerpo, de modo que las de origen cerebral están muy superadas en número y son difíciles de aislar con métodos de laboratorio estándar.
Un chip magnético que separa las señales cerebrales
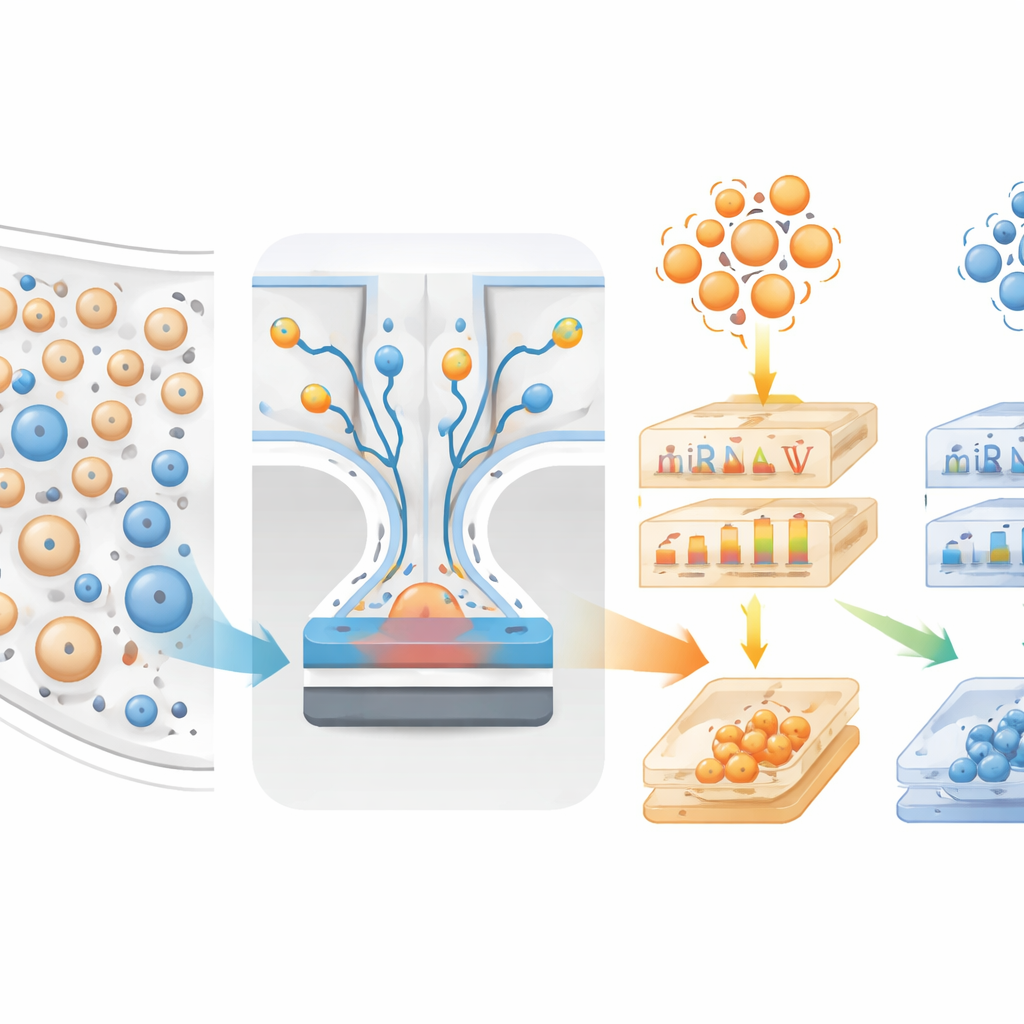
Para afrontar esto, los investigadores construyeron un dispositivo microfluídico llamado mTENPO que combina un chip del tamaño de una tarjeta de crédito con un imán potente. Antes de que una muestra de sangre entre en el chip, las vesículas se marcan con nanopartículas magnéticas mediante anticuerpos que se adhieren a proteínas de superficie típicamente presentes en vesículas de neuronas (GluR2) o de astrocitos (GLAST). A medida que la mezcla marcada fluye a través de millones de pequeños poros en el chip, el campo magnético atrae las vesículas cerebrales fuertemente marcadas hacia las paredes de los poros, reteniéndolas mientras el resto atraviesa. De este modo, el equipo puede enriquecer de forma independiente dos poblaciones de vesículas: las procedentes principalmente de neuronas y las procedentes principalmente de astrocitos, directamente a partir de una pequeña muestra de plasma.
Leer las huellas dactilares moleculares
A partir de 137 voluntarios con diagnósticos cerebrales confirmados post mortem, el equipo aisló estos dos tipos de vesículas y también midió proteínas clásicas de Alzheimer en sangre, como distintas formas de beta-amiloide y tau. Luego secuenciaron pequeños ARN regulatorios (miARN) dentro de las vesículas y analizaron cuáles diferían entre personas con enfermedad por cuerpos de Lewy pura, Alzheimer puro, patologías mixtas o sin demencia. Varios miARN transportados por vesículas neuronales y astrocitarias, junto con varias proteínas relacionadas con tau en plasma, mostraron patrones distintos entre los grupos de cuerpos de Lewy y Alzheimer. Cuando los investigadores mapearon los genes diana de estos miARN, encontraron vínculos sólidos con vías implicadas en la supervivencia celular, la inflamación y el manejo de proteínas, procesos ya asociados con la neurodegeneración.
Construir una prueba de sangre combinada y potente
Como ningún marcador por sí solo separaba claramente las enfermedades, el equipo utilizó herramientas de aprendizaje automático para ensamblar un panel compacto con las señales más informativas extraídas de los tres compartimentos: vesículas neuronales, vesículas de astrocitos y proteínas en sangre. El panel resultante de 15 características incluyó 14 miARN específicos de vesículas más dos proteínas tau fosforiladas. Probado con validación cruzada repetida para reducir el sobreajuste, este panel multimarcador distinguió la enfermedad por cuerpos de Lewy de la enfermedad de Alzheimer con aproximadamente un 95% de precisión y un área bajo la curva de 0,96, lo que resulta sustancialmente mejor que cualquier medida individual por sí sola. Las personas cuyos cerebros mostraban mezclas de patologías tendían a tener niveles intermedios de marcadores, lo que sugiere que dichos paneles podrían algún día ayudar a reconocer enfermedades mixtas en lugar de forzar una etiqueta excluyente.
Del estudio piloto al uso clínico futuro
El estudio es una demostración temprana pero importante de que las vesículas de células cerebrales en sangre pueden portar suficiente información detallada para separar los principales tipos de demencia. El trabajo aún debe confirmarse en cohortes más grandes y diversas y en pacientes seguidos a lo largo del tiempo, y los autores subrayan las limitaciones actuales para precisar la célula de origen exacta de cada vesícula. No obstante, la combinación de un chip magnético escalable y un panel multimarcador cuidadosamente elegido ofrece una hoja de ruta para futuras pruebas de sangre que podrían orientar las decisiones terapéuticas, mejorar los ensayos clínicos y proporcionar a las familias respuestas mucho más claras sobre la enfermedad específica detrás de la demencia de un ser querido.
Cita: Yang, S.J., Lin, A.A., Shen, H. et al. Microfluidic nanomagnetically isolated neuron- and astrocyte-derived extracellular vesicles to differentiate Lewy body and Alzheimer’s disease. npj Biosensing 3, 19 (2026). https://doi.org/10.1038/s44328-026-00086-x
Palabras clave: vesículas extracelulares, enfermedad por cuerpos de Lewy, enfermedad de Alzheimer, biomarcadores en sangre, diagnóstico por microfluidos