Clear Sky Science · es
Detección multiplex en el punto de atención de citocinas mediante una matriz de electrodos HexaPie para la tipificación del asma
Por qué analizar el asma con saliva podría cambiar la atención domiciliaria
El asma afecta a cientos de millones de personas, y aun así los médicos siguen teniendo dificultades para ajustar el tratamiento a cada paciente. Este estudio presenta un pequeño sensor electrónico, llamado HexaPie, que lee señales inmunitarias a partir de una simple muestra de saliva en lugar de sangre. Midiendo varios mediadores de la inflamación a la vez, podría permitir en el futuro que las personas controlen su asma —y otros problemas inmunitarios— de forma rápida e indolora en casa o en una clínica. 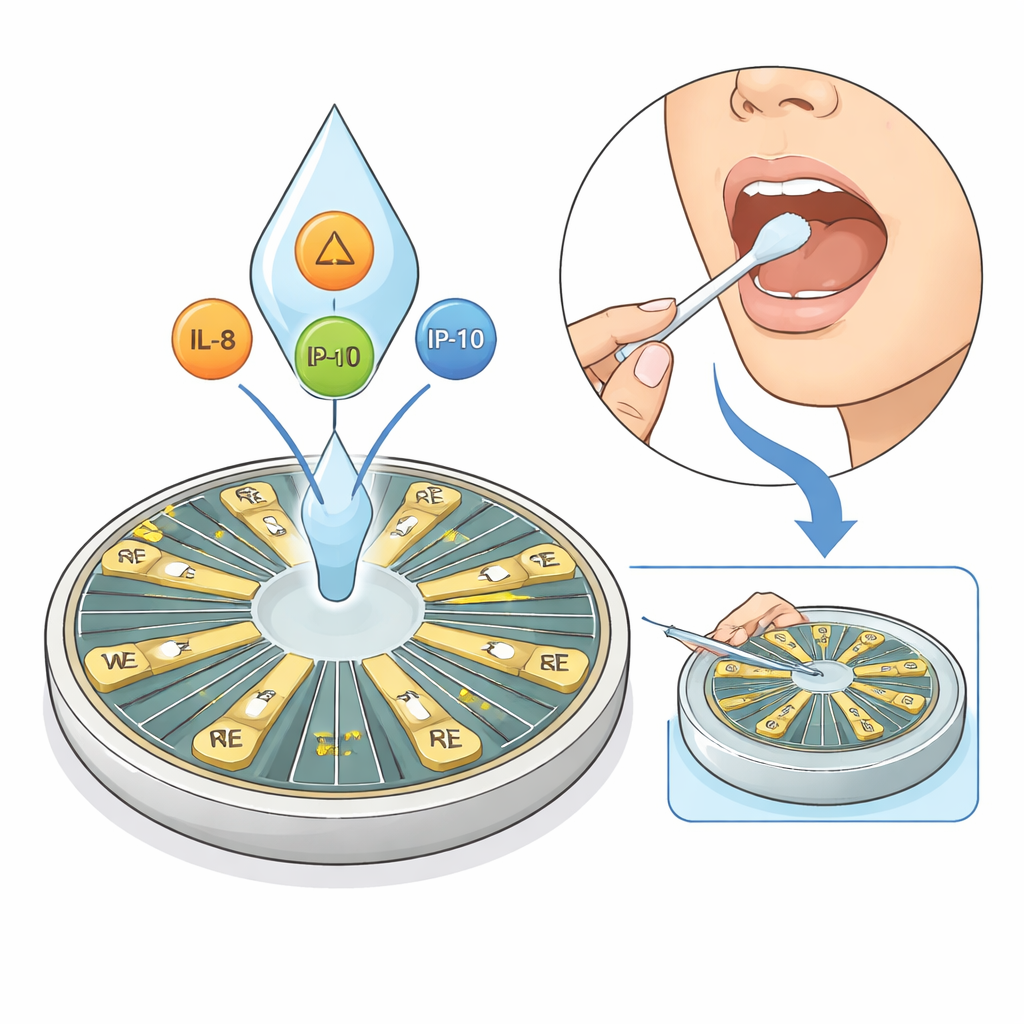
Una nueva forma de escuchar al sistema inmunitario
El asma no es una única enfermedad, sino un conjunto de “tipos” impulsados por vías inmunitarias distintas. Las pruebas tradicionales suelen centrarse en un marcador a la vez y normalmente requieren extracción de sangre y máquinas centralizadas de laboratorio, lo que resulta lento e incómodo para controles frecuentes. El sistema HexaPie pretende resolver esto detectando tres mensajeros inmunitarios clave en la saliva —IL-8, IL-10 e IP-10— que, combinados, dibujan una imagen más amplia de la inflamación de las vías respiratorias, incluidas las formas no eosinofílicas y de difícil tratamiento. Dado que la recolección de saliva es no invasiva y sencilla, es especialmente adecuada para monitorización repetida fuera de grandes hospitales.
Una pequeña matriz de oro que detecta sin químicos añadidos
HexaPie está construido sobre una placa de circuito impreso personalizada que aloja seis pares de diminutos electrodos de oro dispuestos como porciones de una tarta. Cada electrodo de trabajo está recubierto con un anticuerpo distinto que se une específicamente a una de las citocinas objetivo, mientras que el electrodo de referencia pareado permanece desnudo. En lugar de usar tintes o reactivos redox añadidos, el dispositivo se basa en un método eléctrico sin marcaje: cuando las citocinas en la saliva se unen a sus anticuerpos, reorganizan sutilmente partículas cargadas y moléculas de agua en la superficie metálica. Esto modifica la doble capa eléctrica —una región delgada justo en la interfaz— y el cambio resultante en la impedancia eléctrica puede leerse directamente, permitiendo la medición simultánea de las tres citocinas a partir de una sola y pequeña gota.
Poniendo el diseño a prueba mediante simulaciones y ensayos de laboratorio
Antes de fabricar dispositivos completos, el equipo utilizó simulaciones por ordenador para comprobar que la geometría de HexaPie distribuiría los campos eléctricos y las corrientes de manera controlada entre cada electrodo de trabajo y su referencia. Los modelos mostraron que el voltaje aplicado se mantiene bien confinado cerca de las zonas de detección y que la corriente fluye principalmente a través de las brechas previstas—condiciones necesarias para lecturas estables y repetibles. En el laboratorio, los investigadores verificaron la química sobre electrodos de oro añadiendo cada capa—enlazador, anticuerpo y antígeno—mientras seguían señales electroquímicas estándar. A medida que más material biológico cubría la superficie, el flujo de electrones se ralentizaba y la impedancia aumentaba en pasos previsibles, confirmando que las capas de anticuerpos se formaban correctamente y podían capturar sus blancos. 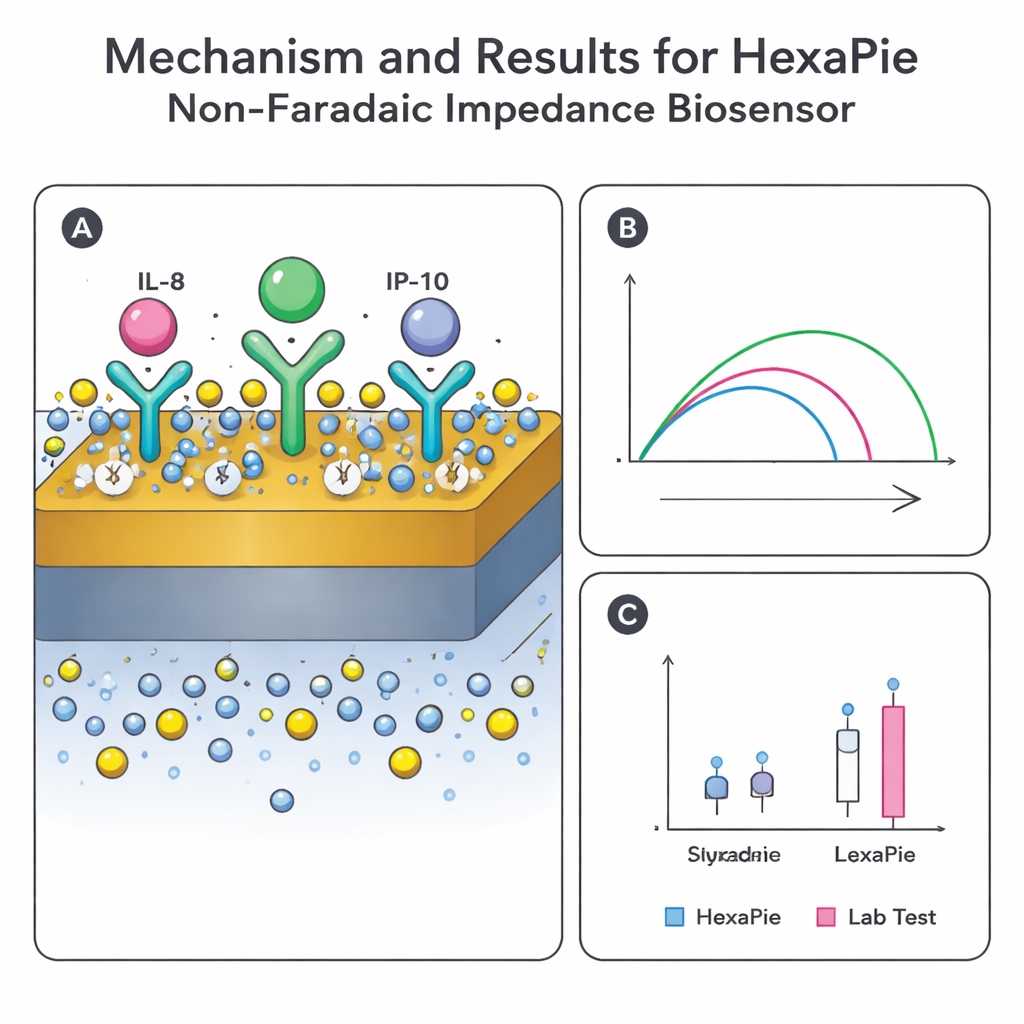
Qué tal mide el sensor muestras reales de saliva
Para evaluar si HexaPie podía proporcionar cifras fiables en la práctica, los autores añadieron cantidades conocidas de las tres citocinas a saliva humana agrupada y midieron los cambios de impedancia resultantes. Las señales variaron de forma ordenada y dependiente de la concentración, y ajustando los datos el equipo construyó curvas de calibración que convierten las lecturas eléctricas en niveles de citocinas. El dispositivo alcanzó límites de detección bajos—hasta billonésimas de gramo por mililitro para algunos marcadores—dentro de los rangos informados en personas con vías respiratorias inflamadas. Las mediciones repetidas en el mismo chip y entre chips distintos variaron menos del 15 por ciento, cumpliendo estándares clínicos aceptados. Cuando los investigadores añadieron componentes comunes de la saliva como albúmina, ácido úrico y vitamina C en niveles elevados, las respuestas del sensor cambiaron muy poco, lo que indica que los interferentes cotidianos probablemente no distorsionen las lecturas.
Comparándolo con pruebas de grado hospitalario
La prueba definitiva fue comparar HexaPie con plataformas de laboratorio consolidadas. Saliva de personas con asma (durante exacerbaciones y en fases estables) y de fumadores y no fumadores sanos se analizó en paralelo con HexaPie, un sistema inmunoensayo automatizado (ELLA) y una prueba multiplex basada en perlas (Luminex). Aunque este pequeño estudio no encontró diferencias claras entre grupos—probablemente por el momento de muestreo y el tamaño de la muestra—los valores del nuevo sensor para IL-8 e IP-10 coincidieron estrechamente con los de ambos métodos de referencia, con solo pequeñas desviaciones promedio. IL-10, que es naturalmente escasa y difícil de medir, mostró más desacuerdo entre plataformas, lo que subraya un reto mayor para detectar de forma fiable moléculas de tan baja abundancia en saliva.
Qué implica esto para la atención cotidiana
Para los no especialistas, la conclusión es que HexaPie traslada mediciones inmunológicas de nivel de laboratorio a un dispositivo compacto y sin reactivos que funciona directamente con saliva. Sigue de forma fiable aumentos clínicamente relevantes en tres citocinas relacionadas con el asma sin etiquetas añadidas ni manejo complejo de la muestra, y sus lecturas concuerdan bien con pruebas de referencia para dos de ellas. Aunque se necesita más trabajo para mejorar la detección de IL-10 y validar el sistema en cohortes de pacientes más amplias, esta tecnología apunta a un futuro en el que las personas con asma y otras enfermedades inflamatorias podrían monitorizar su estado inmunitario de forma rápida e indolora en el punto de atención, ayudando a que los médicos adapten los tratamientos al perfil inmunológico único de cada persona.
Cita: Churcher, N.K.M., Rizvi, F.Z., Qureshi, A. et al. Point-of-care multiplexed detection of cytokines using a HexaPie electrode array for asthma endotyping. npj Biosensing 3, 16 (2026). https://doi.org/10.1038/s44328-026-00081-2
Palabras clave: monitorización del asma, biosensor de saliva, detección de citocinas, diagnóstico en el punto de atención, impedancia electroquímica