Clear Sky Science · es
Resonancia Transmon Superficial (STR): un biosensor de nanogrieta de mano para cinética de unión molecular en tiempo real y sin etiquetas
Por qué un sensor electrónico diminuto importa para tu salud
La medicina moderna depende de pruebas que detectan proteínas y otras moléculas en la sangre para diagnosticar enfermedades, orientar tratamientos y vigilar la salud. Hoy en día, muchas de las pruebas más precisas usan máquinas ópticas voluminosas y caras que están en laboratorios centralizados. Este artículo presenta un nuevo tipo de sensor electrónico del tamaño de la palma que puede leer los mismos eventos de unión molecular en tiempo real, sin etiquetas fluorescentes ni complejos montajes ópticos. Si estos sensores pueden fabricarse de forma barata y portátil, podrían trasladar diagnósticos sofisticados desde laboratorios especializados a clínicas, ambulancias e incluso dispositivos domésticos.
Una nueva manera de “escuchar” a las moléculas
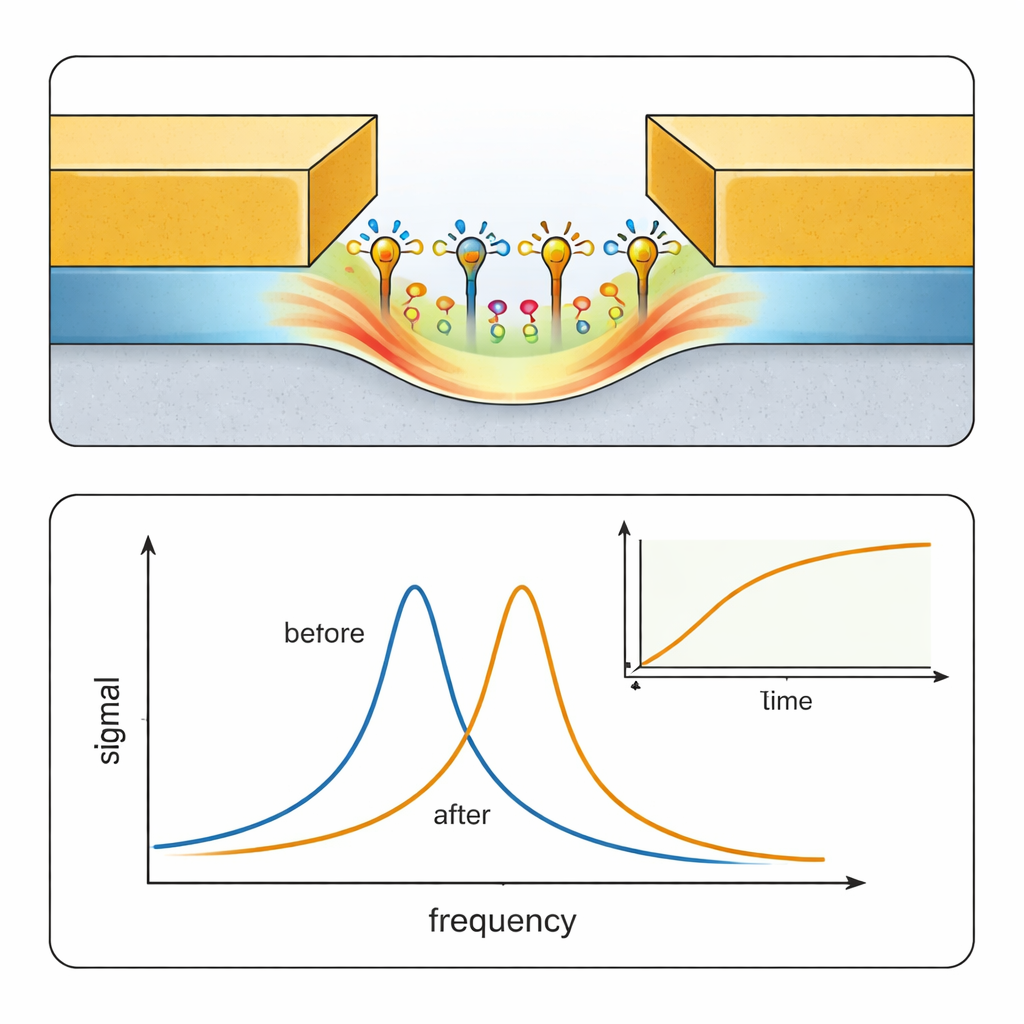
Los investigadores presentan una tecnología que llaman Resonancia Transmon Superficial (STR), un biosensor electrónico que toma ideas del hardware de la computación cuántica. En lugar de usar luz, STR se basa en ondas de radio de alta frecuencia enviadas a través de un circuito diminuto que incluye una brecha a escala nanométrica entre dos pistas metálicas. Cuando las moléculas se adhieren a las superficies dentro de esa brecha, cambian sutilmente la resonancia del circuito, de forma análoga a cómo añadir peso a una cuerda de guitarra altera su tono. Un instrumento portátil de bajo coste llamado nano analizador vectorial de red mide estos desplazamientos en fase y frecuencia de resonancia, produciendo curvas muy parecidas a las de la resonancia de plasmones superficiales (SPR), el “estándar de oro” óptico para estudiar la unión biomolecular.

Superando un obstáculo fundamental en la detección electrónica
Los biosensores electrónicos suelen tener dificultades en soluciones salinas acuosas como la sangre, porque los iones disueltos forman una capa de cribado que oculta las cargas moleculares al electrodo sensor. Este efecto, conocido como cribado de Debye, ha limitado muchos biosensores basados en transistores. STR aborda este problema operando a cientos de megahercios, un régimen en el que los iones no pueden seguir el campo eléctrico que oscila rápidamente. Como resultado, la capa de cribado se debilita y el campo puede sondear con mayor eficacia una capa delgada de moléculas en la superficie. El diseño del sensor concentra el campo eléctrico en una brecha de escala nanométrica, cuyo tamaño es comparable al de proteínas típicas, de modo que incluso una capa molecular fina ocupa una fracción significativa del volumen de detección y provoca un desplazamiento de resonancia medible.
Observando proteínas unirse en tiempo real
Para demostrar que STR puede realizar trabajo bioquímico serio, el equipo estudió un par de prueba clásico: albúmina sérica bovina (BSA), una proteína bien conocida, y anticuerpos que la reconocen. Primero hicieron fluir una solución tampón por un canal microfluídico sobre el sensor para obtener una línea base, luego inyectaron BSA para recubrir la superficie de oro dentro de la brecha y finalmente introdujeron anticuerpos anti‑BSA a diferentes concentraciones. El sensor siguió cómo su frecuencia de resonancia se desplazaba con el tiempo a medida que los anticuerpos se unían y luego se desunían cuando se volvió a introducir tampón limpio. Debido a que la nanogrieta es tan pequeña, los eventos de unión tienen un efecto grande en comparación con un dispositivo de control que tiene una brecha de 10 micrómetros de ancho, lo que confirma que STR responde principalmente a moléculas unidas a la superficie en lugar de a cambios en el líquido a granel. Ajustando las curvas de unión y disociación, los autores extrajeron velocidades de asociación y disociación y una constante de afinidad global que coincidió estrechamente con valores medidos de forma independiente con un instrumento SPR.
Rendimiento que rivaliza con el equipo óptico de laboratorio
Más allá de la simple detección, los autores cuantificaron la sensibilidad de STR. Mostraron que pequeños desplazamientos en la frecuencia de resonancia corresponden a cambios muy pequeños en las propiedades eléctricas de la solución cercana a la superficie, y determinaron un límite de detección de proteínas de aproximadamente 7 nanomolar para el anticuerpo probado. Ese rendimiento es comparable al de varios sensores SPR nanoplasmónicos avanzados reportados en la literatura. Es importante subrayar que esto se logró usando un prototipo diseñado para portabilidad y bajo coste, no para sensibilidad máxima. La principal fuente de ruido fue el propio analizador de mano, y los autores esbozan vías directas de mejora, como aumentar la potencia de la señal, mejorar la nitidez (factor Q) de la resonancia, estrechar aún más la brecha y refinar la química de superficie y la integración electrónica.
Del banco de laboratorio a diagnósticos de bolsillo
Para hacer STR práctico a escala, el equipo también desarrolló un enfoque de fabricación a nivel de oblea que puede producir matrices de sensores de nanogrieta usando técnicas compatibles con la microelectrónica convencional. Imaginan versiones futuras en las que las estructuras sensoras y los circuitos de radiofrecuencia estén integrados en el mismo chip, formando potencialmente el núcleo de herramientas diagnósticas portátiles o incluso vestibles. Dado que STR proporciona curvas de unión en tiempo real y datos cinéticos cuantitativos que normalmente se limitan a grandes instrumentos ópticos, podría llevar el análisis molecular de grado de laboratorio a muchos más entornos. Para los no especialistas, la conclusión es que este trabajo nos acerca a dispositivos de mano capaces de seguir cómo moléculas biomarcadoras específicas se unen e interactúan en tiempo real, abriendo la puerta a pruebas médicas más rápidas, accesibles y personalizadas.
Cita: Chantigian, B.K., Oh, SH. Surface Transmon Resonance (STR): a handheld nanogap biosensor for real-time, label-free molecular binding kinetics. npj Biosensing 3, 15 (2026). https://doi.org/10.1038/s44328-026-00080-3
Palabras clave: biosensor, diagnóstico molecular, nanotecnología, detección por radiofrecuencia, detección sin etiquetas