Clear Sky Science · es
Ensayo biológico mejorado por plasmones para la detección y cuantificación sin amplificación del ARN de SARS-CoV-2
Por qué importan las pruebas virales más rápidas y sencillas
La pandemia de COVID-19 dejó al descubierto cuánto dependemos de pruebas de laboratorio que son lentas, caras y difíciles de escalar cuando millones de personas necesitan respuestas con rapidez. El trabajo descrito aquí presenta un nuevo tipo de prueba de laboratorio capaz de detectar y contar cantidades muy pequeñas de material genético del coronavirus sin el paso de amplificación habitual de la PCR. Este enfoque pretende acercar la exactitud propia de un hospital a pruebas simples y de bajo coste que podrían desplegarse con mayor amplitud en futuros brotes.
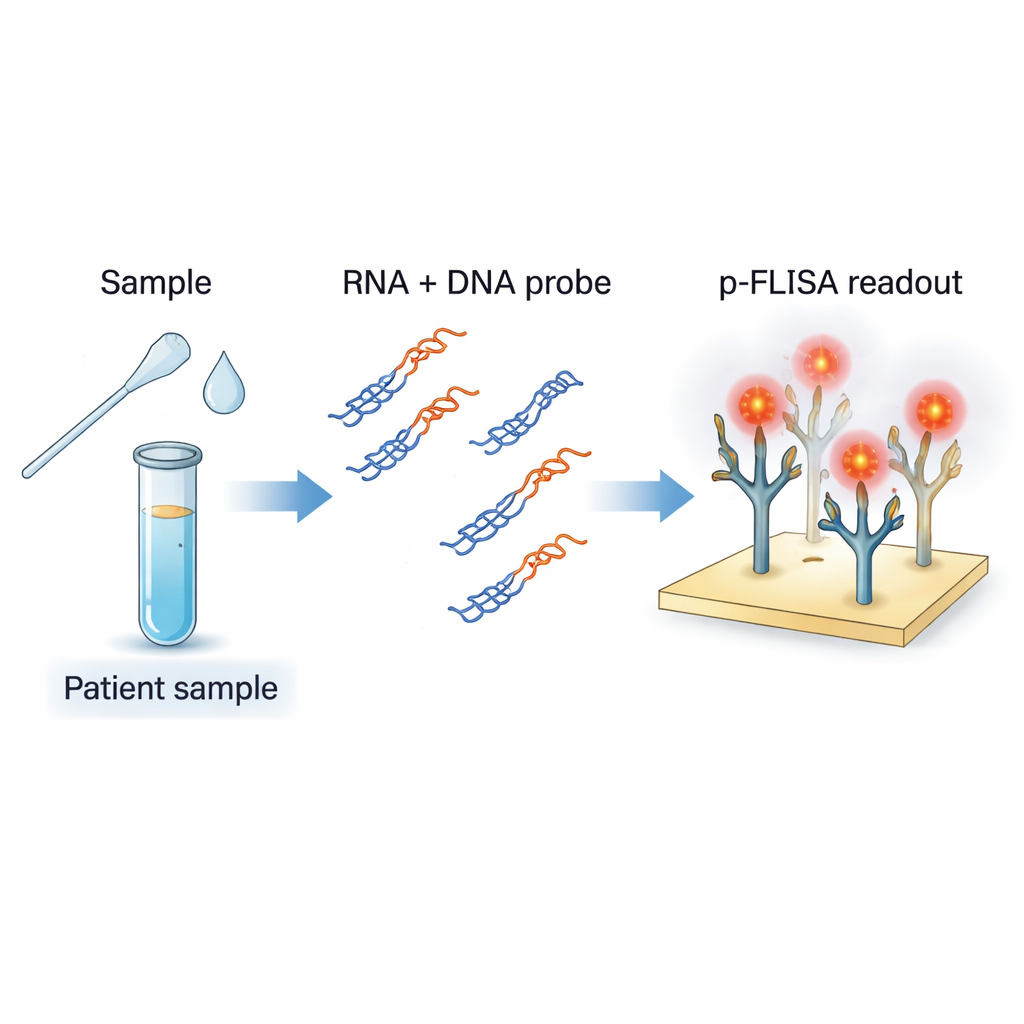
Una nueva forma de ver rastros genéticos virales
El diagnóstico estándar de COVID-19 utiliza RT-PCR, que copia muchas veces fragmentos del ARN viral para que puedan detectarse. Aunque muy sensible, la PCR requiere equipo complejo, personal entrenado y tiempo, y suele ofrecer una respuesta de «sí o no» en lugar de una carga viral precisa. Los autores se propusieron construir un ensayo que funcione más como una versión muy mejorada de un ELISA sanguíneo: un formato simple en placa, pero afinado para detectar directamente ARN viral y cuantificar su cantidad. Su método se dirige al ARN de SARS-CoV-2 en muestras como hisopos nasales y saliva, pero está diseñado para adaptarse fácilmente a otros virus de ARN.
Convertir el ARN en un objetivo capturable
El equipo utiliza fragmentos cortos de ADN diseñados para emparejarse con regiones específicas del genoma de SARS-CoV-2. Al mezclarse con el ARN extraído de una muestra de paciente y someterse a un suave calentamiento y enfriamiento, estas sondas de ADN se emparejan con cualquier ARN viral coincidente para formar híbridos ADN–ARN, como una pequeña cremallera con una hebra de ARN y otra de ADN. Un anticuerpo especial llamado S9.6 actúa como capturador: reconoce y se une con fuerza a estos híbridos, pero no al ADN de cadena simple o doble ni a ARN no relacionado. Al recubrir el fondo de una placa con S9.6, el ensayo atrapa selectivamente sólo esos híbridos que contienen las secuencias genéticas virales de interés, separando el resto del material genético de la muestra.
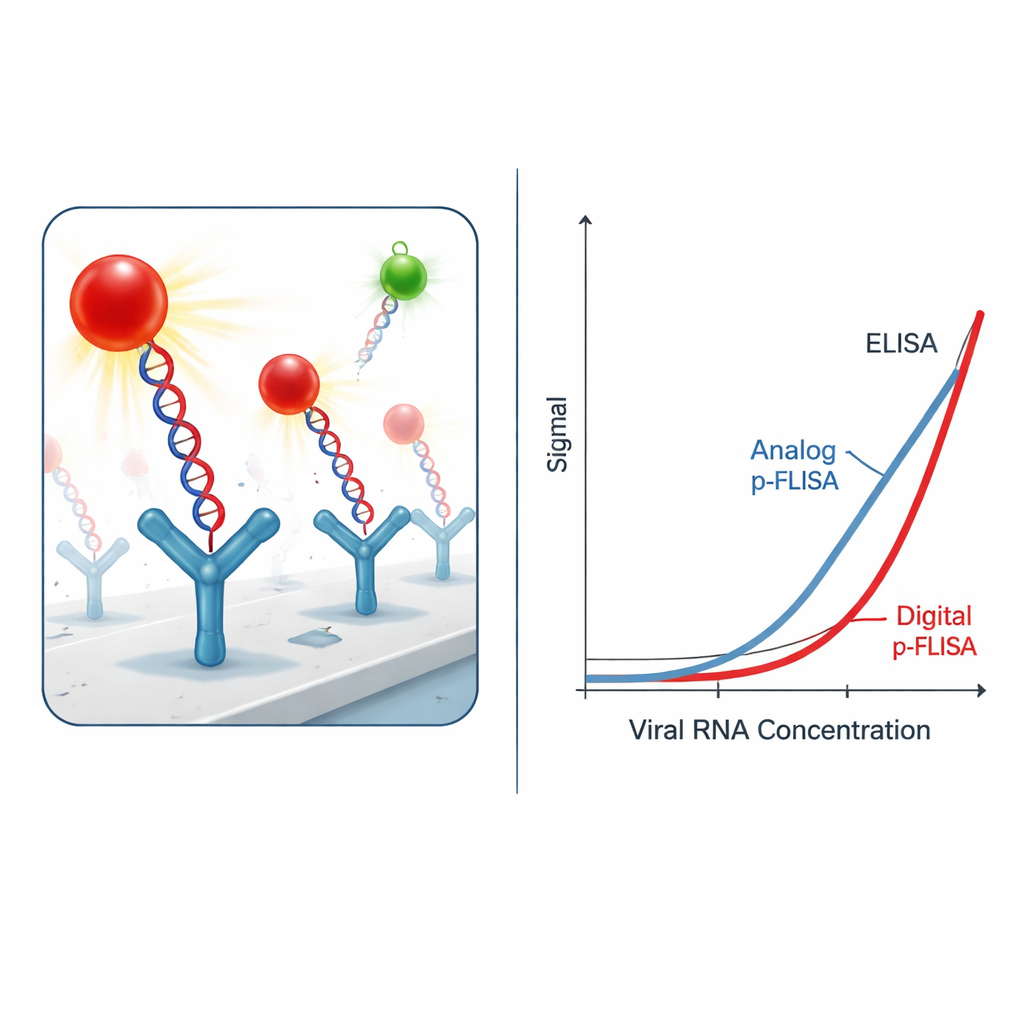
Hacer la señal ultrabrillante
Atraparlos no basta; el desafío es verlos por encima del ruido de fondo. En lugar de tintes fluorescentes convencionales, los investigadores usan nanomarcadores «plasmonic-fluor»: nanopartículas diseñadas que actúan como diminutas antenas para la luz. Cada marcador combina una nanobarra metálica con múltiples moléculas fluorescentes y un recubrimiento que le permite unirse a etiquetas de biotina en el ADN o el anticuerpo. Estos marcadores plasmónicos emiten luz más de mil veces más brillante que los tintes estándar en las mismas condiciones. En la práctica, eso significa que se necesitan muchos menos híbridos virales para producir un brillo detectable, mejorando drásticamente la sensibilidad de la prueba y reduciendo la concentración mínima de ARN viral que puede medirse.
De un brillo analógico a un conteo digital
En su forma más simple «analógica», el ensayo mide el brillo total de cada pocillo de la placa, de manera similar a una prueba fluorescente clásica. Incluso en este modo, el sistema mejorado por plasmones mejora el límite de detección y el nivel mínimo cuantificable de ARN de SARS-CoV-2 entre uno y tres órdenes de magnitud en comparación con un ELISA tradicional que usa enzimas o fluoróforos estándar. Los autores llevan la idea más allá al cambiar a un formato «digital»: en lugar de promediar la luz de todo el pocillo, se imagen la superficie con un microscopio de fluorescencia y se cuentan los nanomarcadores individuales brillantes mediante software de análisis de imagen personalizado. Este enfoque de conteo de partículas individuales proporciona otra ganancia de sensibilidad de entre diez y treinta veces, llevando a aproximadamente 2.300 veces mejores límites de detección y 460 veces mejores límites de cuantificación que el ELISA en conjunto.
Poner la prueba a trabajar con muestras reales
Para comprobar si el método funciona fuera de mezclas controladas de laboratorio, los investigadores probaron ARN extraído de hisopos nasales y saliva de pacientes con COVID-19, incluyendo infecciones por distintas variantes virales como alfa/beta y delta, así como muestras de personas con otros virus respiratorios. Su ensayo mejorado por plasmones detectó ARN de SARS-CoV-2 en todas las muestras PCR-positivas, sin señal por encima del fondo en muestras PCR-negativas o en aquellas que albergaban otros virus, lo que indica una excelente sensibilidad y especificidad clínica comparable a la RT-PCR. Además, las concentraciones de ARN medidas mostraron una relación inversa con los valores del umbral de ciclos de la PCR: las muestras que necesitaron menos ciclos de PCR (indicando mayor carga viral) presentaron niveles más altos de ARN según el nuevo ensayo, coherente con las expectativas biológicas y sugiriendo que puede proporcionar información cuantitativa significativa sobre la carga viral.
Qué podría significar esto para futuros brotes
Para un público no especializado, el mensaje clave es que este ensayo ofrece una forma de leer cuánto virus hay presente sin el paso adicional de copia que hace que la PCR sea lenta y dependa de mucho equipo. Al combinar un anticuerpo selectivo para híbridos ARN–ADN con fuentes de luz nanoscópicas ultrabrillantes y conteo digital, el método se aproxima al rendimiento de la PCR manteniendo un flujo de trabajo simple en placa. Con mayor validación e ingeniería, estos ensayos mejorados por plasmones podrían adaptarse a muchos objetivos de ARN y posiblemente transformarse en formatos rápidos para punto de atención, ayudando a los clínicos no sólo a diagnosticar infecciones sino también a valorar la fase de la enfermedad y la contagiosidad a partir de una medida absoluta del ARN viral.
Cita: Liu, L., Seth, A., Liu, Y. et al. Plasmon-enhanced bioassay for amplification-free detection and quantification of SARS-CoV-2 RNA. npj Biosensing 3, 13 (2026). https://doi.org/10.1038/s44328-026-00078-x
Palabras clave: detección de ARN de SARS-CoV-2, nanomarcadores plasmónicos, inmunoensayo digital, diagnósticos sin amplificación, cuantificación de carga viral