Clear Sky Science · es
Un biosensor microfluídico basado en microórganos para el control continuo de los niveles de glucosa in vivo
Por qué esto importa para las personas con diabetes
Para las personas con diabetes tipo 1, los sistemas actuales de “páncreas artificial” todavía requieren atención constante: anunciar comidas, gestionar alarmas y preocuparse por la hipoglucemia nocturna. Este estudio explora un tipo de sensor de glucosa radicalmente distinto que no depende de una sola enzima o de una ecuación informática, sino que toma prestada una pequeña parte viva de la propia maquinaria corporal de control del azúcar: cúmulos de células pancreáticas llamados islotes. Al dejar que estos mini-órganos hagan lo que la evolución ha optimizado, los investigadores pretenden construir monitores de glucosa más inteligentes y seguros que algún día puedan funcionar de forma más independiente en segundo plano.
Un órgano diminuto como sensor vivo
La mayoría de los biosensores actuales detectan químicos usando moléculas purificadas o líneas celulares individuales. Responden a una sustancia específica y luego pasan la señal bruta a un software que intenta interpretarla. Los autores sostienen que este enfoque ignora un “ordenador” incorporado y poderoso: los micro-órganos, como los islotes pancreáticos, que de forma natural detectan muchas señales a la vez y las convierten en una respuesta coordinada. Cada islote contiene varios tipos celulares productores de hormonas que se comunican constantemente entre sí. Juntos mantienen la glucosa en sangre dentro de un rango estrecho y seguro, reaccionando no solo a la glucosa sino también a aminoácidos, hormonas intestinales y del estrés, y a la historia reciente de altos y bajos del organismo. Esta complejidad incorporada, sugieren, podría aprovecharse para producir información más rica y confiable que la de un simple sensor de glucosa-oxidasa.
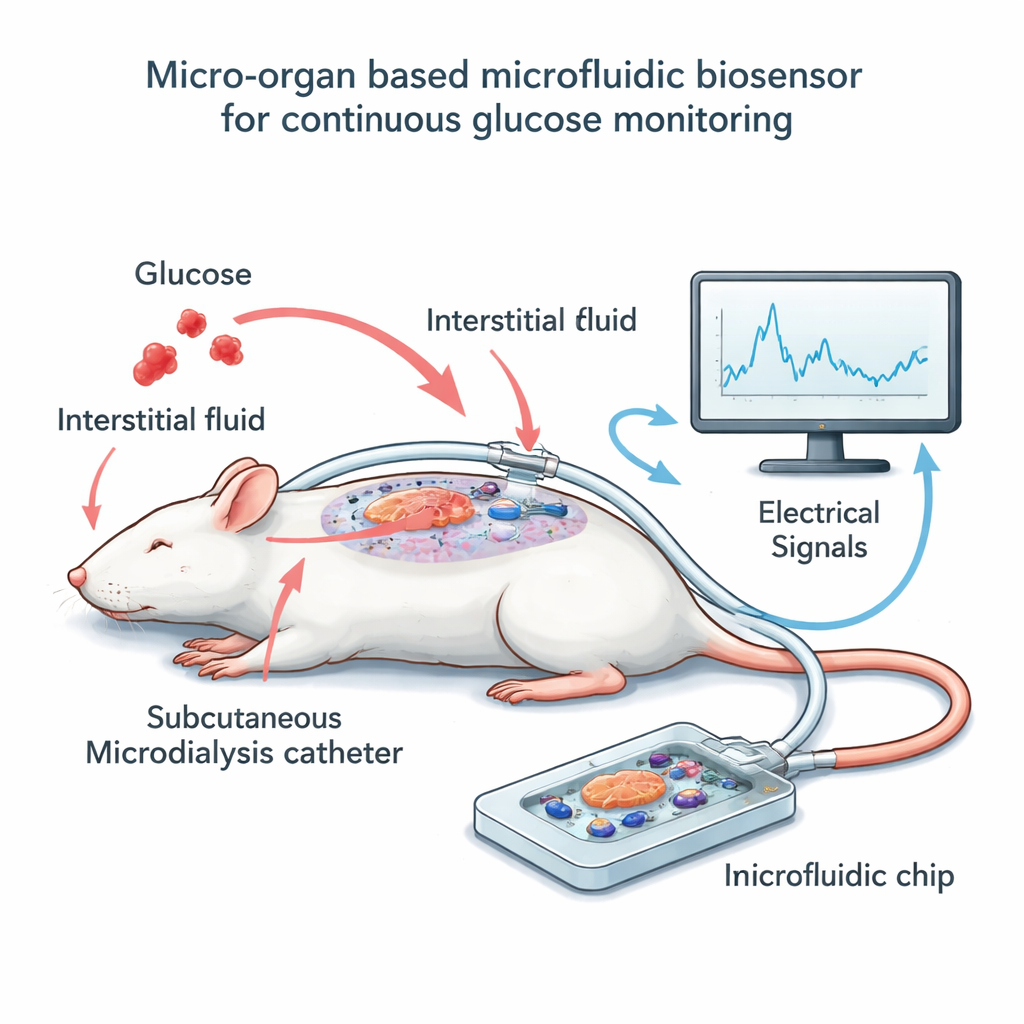
Construyendo el sistema chip–catéter
Para probar la idea, el equipo construyó un pequeño dispositivo extracorpóreo que aloja unas pocas docenas de islotes de ratón sobre una rejilla de electrodos microscópicos. En lugar de bañar estas células directamente en sangre, usaron una técnica llamada microdiálisis: un catéter fino y flexible se coloca justo debajo de la piel de ratas anestesiadas y recoge lentamente el líquido tisular circundante, que sigue de cerca la glucosa sanguínea pero con un breve retardo. Un flujo bajo y constante transporta este fluido a través de un canal estrecho sobre los islotes en el chip. A medida que los niveles de glucosa en el dialisado suben y bajan, los islotes modifican su actividad eléctrica, que los electrodos capturan como señales lentas y ondulatorias. En paralelo, los investigadores midieron periódicamente la glucosa en la sangre de las ratas y en el dialisado, lo que les permitió alinear la lectura eléctrica con los niveles reales de azúcar a lo largo del tiempo.
Cómo respondió el sensor vivo a los cambios de azúcar
Primero, los científicos comprobaron si los islotes sobre los electrodos podían responder a componentes sanguíneos reales en lugar de soluciones de laboratorio simples. Los expusieron a suero humano y de rata con distintos niveles de glucosa y observaron cambios claros y graduados tanto en la frecuencia como en el tamaño de sus ondas eléctricas. Las respuestas fueron lo bastante fuertes como para distinguir pasos pequeños en la concentración de azúcar dentro del rango relevante para la diabetes. Luego pasaron a experimentos en ratas, administrando una inyección de glucosa para elevar la glucemia y más tarde inyectando insulina para reducirla. Tras tener en cuenta el tiempo que tarda la glucosa en pasar de la sangre al líquido tisular y por la tubería, encontraron que la frecuencia de las señales eléctricas lentas de los islotes subía y bajaba casi al mismo ritmo que la glucemia. El análisis estadístico en varios animales mostró una relación sorprendentemente estrecha y repetible entre la frecuencia de la señal y el nivel de glucosa, mientras que la amplitud de la señal, aunque informativa, fue algo más variable.
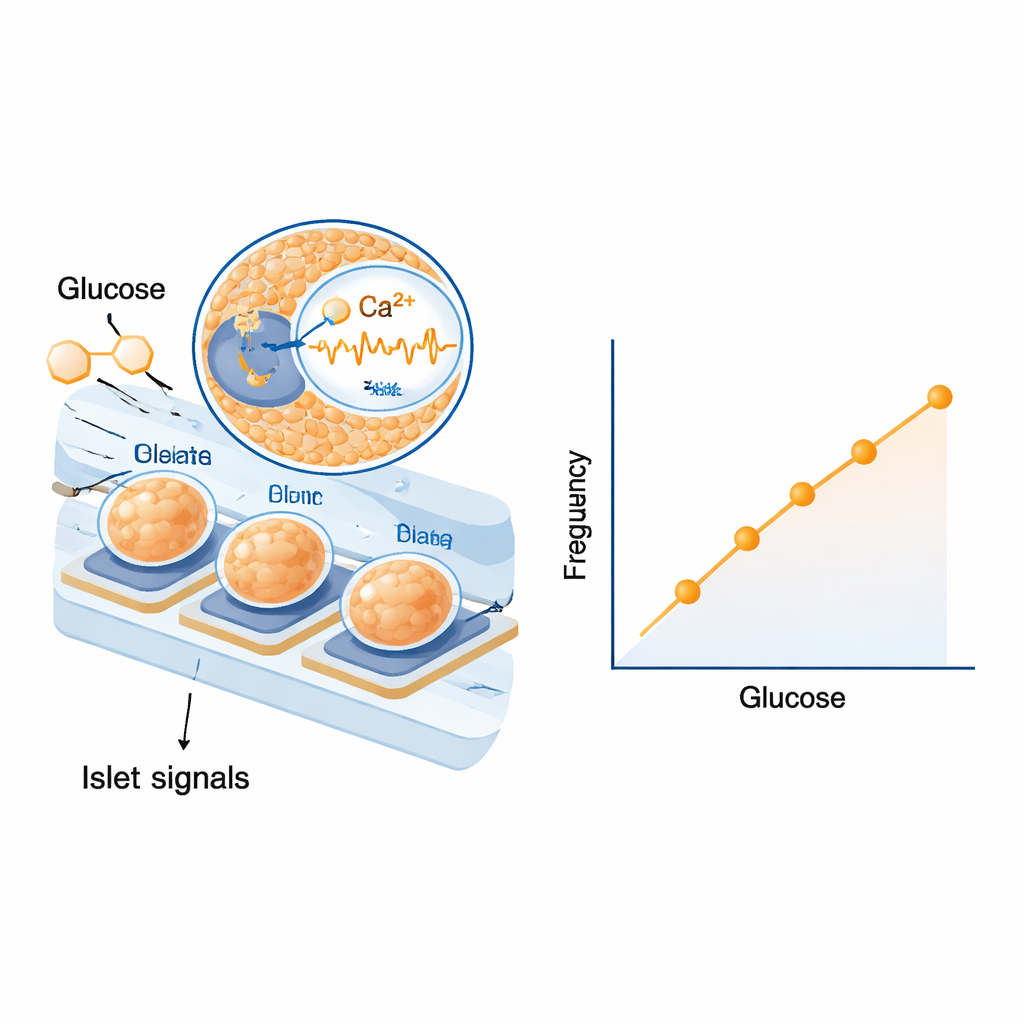
Funciones de seguridad incorporadas por la biología
Una ventaja importante de usar islotes enteros, en lugar de una sola molécula, es que su comportamiento ya incluye mecanismos de seguridad moldeados por la evolución. Trabajos anteriores, y indicios de este estudio, muestran que los islotes reaccionan con mayor intensidad cuando la glucosa está disminuyendo que cuando está aumentando—una forma de “histéresis” que ayuda a proteger contra hipoglucemias peligrosas. Los patrones eléctricos también están modulados por tipos celulares vecinos que amplifican o atenúan la liberación de insulina según las necesidades del organismo. Porque el chip simplemente escucha estas señales integradas sin añadir colorantes o modificaciones genéticas, puede registrar durante días sin dañar las células. Los autores señalan desafíos técnicos por delante, como evitar burbujas de aire, asegurar el rendimiento de la microdiálisis a largo plazo y decidir qué tipo de islotes humanos o derivados de células madre deberían usarse finalmente. Aun así, simulaciones informáticas usando un modelo establecido de diabetes sugieren que un sensor basado en islotes podría igualar o incluso superar a los monitores de glucosa actuales en condiciones difíciles.
Qué podría significar esto para el cuidado futuro de la diabetes
Este trabajo muestra que un puñado de micro-órganos pancreáticos, mantenidos vivos en un pequeño chip y conectados al cuerpo mediante un catéter fino, pueden seguir la glucosa en sangre de forma continua en animales vivos mediante su charla eléctrica natural. Para un público no especializado, el mensaje clave es que, en lugar de pedirle a un sensor químico simple que mida glucosa y luego obligar a un ordenador a adivinar qué significa eso para el cuerpo, este enfoque escucha directamente al mismo tipo de tejido vivo que normalmente decide cuánto insulina liberar. Si se perfecciona y se hace práctico para uso humano, tales biosensores vivos podrían convertirse en el núcleo de sistemas de páncreas artificial verdaderamente autónomos—dispositivos que anticipen con discreción las necesidades del cuerpo y reduzcan la carga diaria del manejo de la diabetes.
Cita: Puginier, E., Pirog, A., de Gannes, F.P. et al. A micro-organ based microfluidic biosensor for continuous monitoring of glucose levels in vivo. npj Biosensing 3, 12 (2026). https://doi.org/10.1038/s44328-025-00077-4
Palabras clave: monitorización continua de glucosa, páncreas artificial, islotes pancreáticos, biosensor microfluídico, diabetes tipo 1