Clear Sky Science · es
Técnicas avanzadas de imagen para la navegación intraoperatoria de tumores
Ver el cáncer con mayor claridad en el quirófano
La cirugía oncológica suele implicar un delicado equilibrio: extirpar hasta la última célula cancerosa preservando, a la vez, la mayor cantidad posible de tejido sano. Este artículo de revisión explica cómo una nueva generación de herramientas de imagen ayuda a los cirujanos a ver realmente los tumores y sus márgenes en tiempo real durante la operación. Para un lector general, el atractivo es directo: estas tecnologías prometen menos reintervenciones, extirpaciones tumorales más precisas y mejores probabilidades de supervivencia a largo plazo, todo al proporcionar a los cirujanos un “mapa” más claro mientras trabajan.
Por qué importa tener mejor visión durante la cirugía
El cáncer es hoy una de las principales causas de muerte en el mundo, y la cirugía sigue siendo una pieza fundamental del tratamiento. Sin embargo, incluso el cirujano más hábil ha estado limitado por lo que puede verse y palparse y por las exploraciones realizadas días o semanas antes de la intervención. Herramientas tradicionales como el ultrasonido, la TC, la RM y la PET ayudan a planificar la cirugía, pero a menudo son voluminosas, lentas o no aptas para un uso continuo durante la operación. Como resultado, puede ser difícil determinar exactamente dónde termina un tumor y comienza el tejido sano, lo que aumenta el riesgo de dejar cáncer residual o de resecar tejido normal en exceso. La revisión expone cómo la “imagen intraoperatoria” —imágenes en directo utilizadas en el propio quirófano— está cambiando ese panorama.
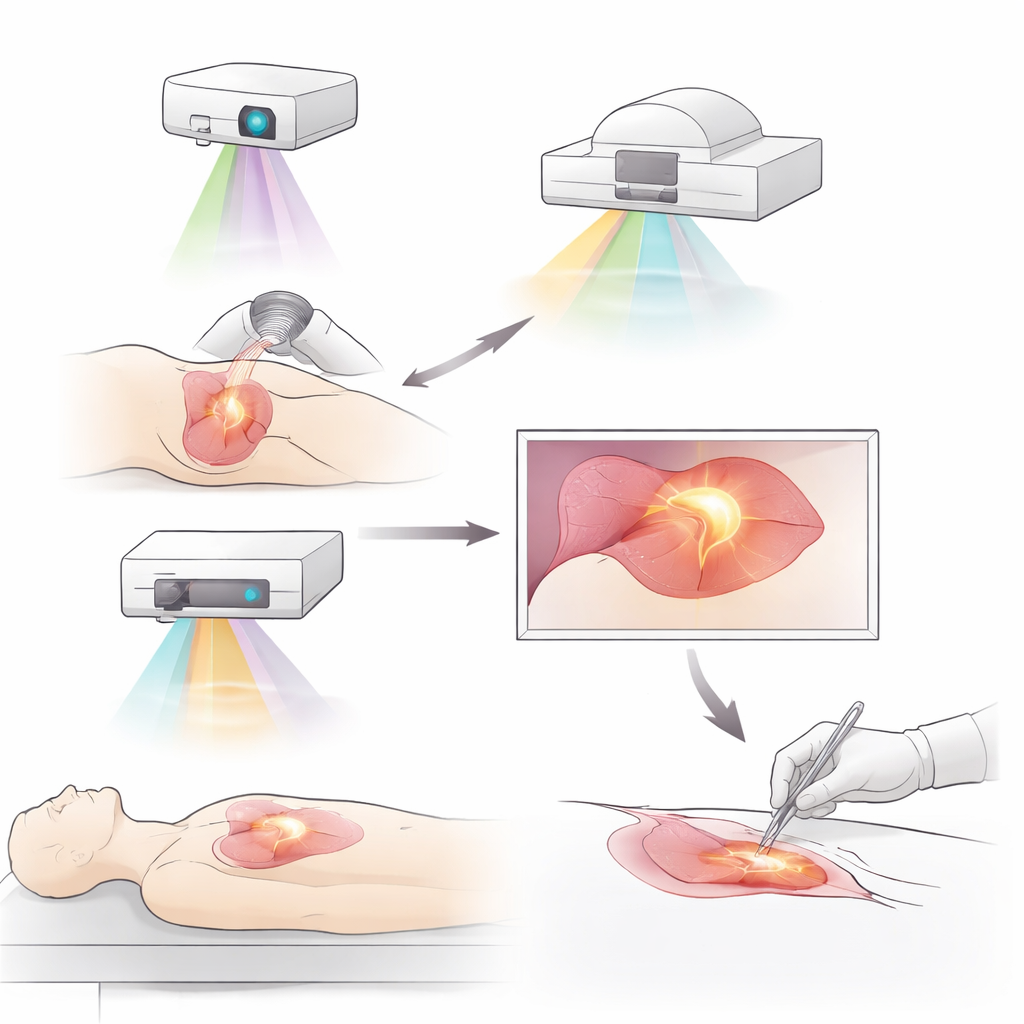
Tumores que brillan y nuevas formas de iluminarlos
Un avance importante es la imagen por fluorescencia, en la que colorantes especiales o sondas moleculares hacen que los tumores brillen bajo luz en el infrarrojo cercano. Colorantes no dirigidos más antiguos, como el verde de indocianina, ya han ayudado a los cirujanos a delimitar tumores, trazar vasos linfáticos y localizar ganglios linfáticos relevantes en cánceres de mama, hígado, pulmón y estómago. Sondas dirigidas más recientes van más allá al localizarse en moléculas sobreproducidas por las células tumorales o por su microambiente. Ejemplos incluyen sondas que se unen a receptores de factores de crecimiento, puntos de control inmunitarios o proteínas abundantes en el tejido de sostén del tumor o en zonas con baja oxigenación. Algunos de estos agentes pueden incluso ligarse a fármacos oncológicos, combinando visualización precisa con terapia en la misma molécula. Ensayos clínicos tempranos muestran que dichos trazadores pueden descubrir depósitos tumorales ocultos y reducir la necesidad de reintervenciones tras cirugías conservadoras de mama.
Más allá del brillo: sonido, luz y muchos colores
Aunque la fluorescencia es central, la revisión destaca varias aproximaciones complementarias que captan diferentes aspectos de un tumor. La imagen fotoacústica usa pulsos de luz para generar ondas sonoras dentro del tejido, combinando el detalle de los métodos ópticos con la profundidad del ultrasonido, y ha logrado revelar metástasis muy pequeñas que otras exploraciones pasan por alto. La imagen multiespectral e hiperespectral divide la luz en muchas bandas, captando sutiles diferencias en cómo los tejidos absorben y reflejan la luz; esto puede distinguir el cáncer del tejido normal con alta precisión en tumores mamarios, cervicales y del tracto gastrointestinal. Avances en ultrasonidos —incluidas técnicas que miden la rigidez tisular— aportan información de profundidad y ayudan a mostrar hasta qué punto ha infiltrado el cáncer. La espectroscopía Raman, que lee la “huella” química del tejido según cómo las moléculas dispersan la luz, ofrece identificación de cáncer sin marcador y muy específica durante la cirugía, especialmente cuando se combina con otras modalidades.
Construir mapas 3D y combinar múltiples vistas
Otro tema del artículo es la combinación de imágenes en vistas tridimensionales y multimodales que los cirujanos puedan usar de forma intuitiva. Reconstrucciones tridimensionales de vasos sanguíneos, canales linfáticos y órganos, superpuestas con señales fluorescentes, ayudan a planificar resecciones segmentarias precisas de hígado y pulmón y orientan disecciones de ganglios linfáticos complejas. Sistemas híbridos que fusionan PET con imagen óptica o que emparejan trazadores de medicina nuclear con fluorescencia permiten usar la misma sonda para el cribado preoperatorio de todo el cuerpo y la orientación intraoperatoria. Plataformas emergentes integran ablación láser, tomografía de coherencia óptica y robótica para localizar y tratar lesiones automáticamente con alta precisión. Estos enfoques buscan ofrecer a los cirujanos tanto la “visión global” de la extensión tumoral como el detalle fino necesario para cortar siguiendo márgenes limpios y seguros.
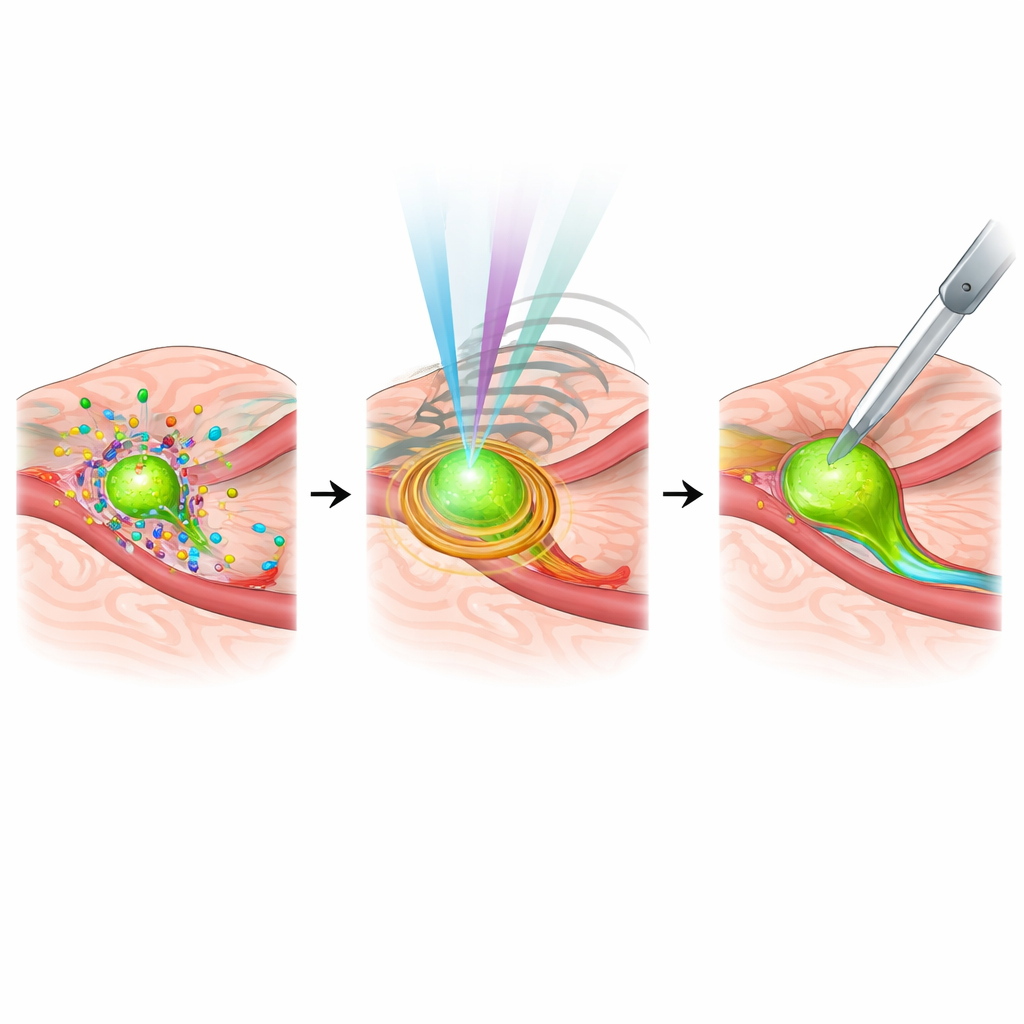
Sistemas más inteligentes, dianas personalizadas y obstáculos pendientes
La revisión también mira hacia el papel de la inteligencia artificial y la medicina personalizada. Modelos de aprendizaje automático ya ayudan a distinguir tejido canceroso de tejido normal en tiempo real, reconocer estructuras anatómicas críticas e incluso predecir la diseminación a ganglios linfáticos durante la cirugía pancreática, lo que podría reducir la dependencia de la anatomía patológica rápida. Al mismo tiempo, las sondas de imagen se están rediseñando para ajustarse a las firmas moleculares únicas del tumor de cada paciente, vinculando las imágenes intraoperatorias con perfiles genéticos y moleculares. No obstante, permanecen obstáculos: muchos sistemas son costosos, complejos y difíciles de integrar en los flujos de trabajo rutinarios; algunos requieren agentes de contraste especializados con perfiles de seguridad cuidadosamente gestionados; y los estándares para integrar todos estos datos en sistemas de navegación aún están en desarrollo.
Qué significa esto para los pacientes
En términos accesibles, la conclusión del artículo es que los cirujanos están ganando algo que nunca tuvieron realmente antes: la capacidad de ver el cáncer vivo con gran claridad mientras operan. Al iluminar tumores, leer su química, cartografiarlos en 3D y combinar múltiples tipos de imagen —a menudo asistidos por IA—, estas herramientas pueden ayudar a asegurar que se extraiga más tumor y se preserve más tejido sano. Aunque el coste, la formación y las brechas tecnológicas deben abordarse antes de que tales sistemas estén ampliamente disponibles, la dirección es clara. La imagen intraoperatoria avanzada está lista para convertirse en una parte clave de la cirugía oncológica estándar, ofreciendo a los pacientes intervenciones más precisas, menos recidivas y mejores probabilidades de control a largo plazo.
Cita: Li, K., Zhang, Y., Yang, H. et al. Advanced imaging techniques for tumor intraoperative navigation imaging. npj Imaging 4, 18 (2026). https://doi.org/10.1038/s44303-026-00150-1
Palabras clave: imagen intraoperatoria, cirugía guiada por fluorescencia, detección de márgenes tumorales, imagen multimodal del cáncer, imagen fotoacústica