Clear Sky Science · es
Imagen multimodal correlativa para el mapeo espacial a microescala de las interacciones entre colágeno y actividad génica en tejidos humanos
Por qué importa mirar dentro de los músculos
Las enfermedades que cicatrizan lentamente nuestros órganos, como la distrofia muscular de Duchenne (DMD), se desarrollan a escalas demasiado pequeñas para el ojo desnudo. La actividad génica ocurre dentro de células individuales, mientras que el tejido de sostén que las rodea está compuesto por diminutas fibras proteicas. Hasta ahora, los científicos rara vez han podido ver estos dos mundos juntos en la misma sección de tejido humano. Este estudio presenta una forma de hacer exactamente eso, revelando cómo interactúan los mensajes de los genes y el andamiaje estructural del cuerpo a microescala.
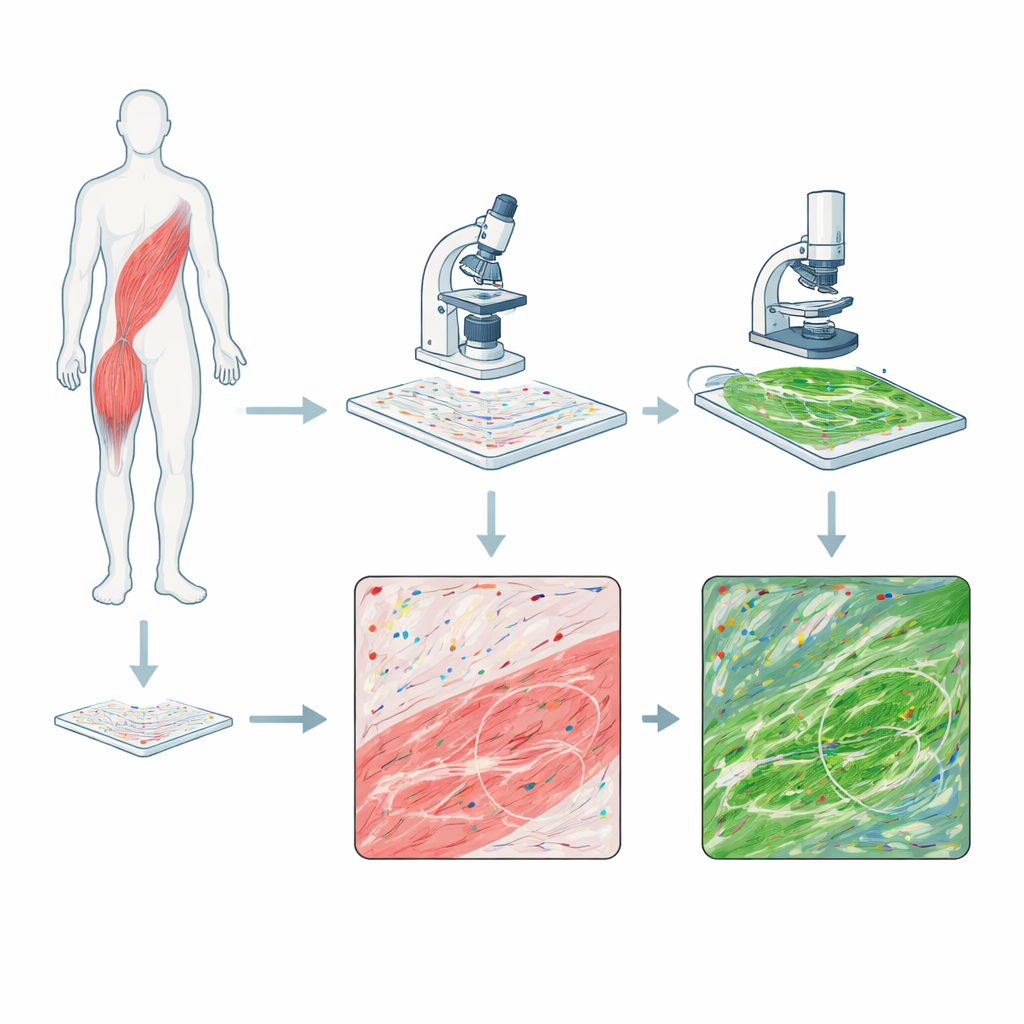
Dos «cámaras» en la misma pieza de tejido
Los investigadores combinaron dos potentes métodos de imagen en secciones únicas de biopsias de músculo esquelético humano procedentes de personas con DMD y de un voluntario sano. Un método, llamado RNAscope, tiñe moléculas individuales de ARN—las copias de trabajo de los genes—como puntos coloreados, mostrando dónde están presentes mensajes genéticos específicos. El segundo método, microscopía multiphotón, utiliza luz láser para hacer que las fibras de colágeno del tejido brillen sin tintes añadidos, capturando la arquitectura del tejido conectivo que se engrosa durante la cicatrización y la fibrosis. Al obtener primero las señales de ARN y luego las del colágeno en la misma portaobjetos, pudieron alinear las dos imágenes de modo que cada punto de actividad génica se comparara con la red de fibras circundante, píxel a píxel.
Lo que ya cuentan las vistas separadas
Observar cada método de imagen por separado ya resaltó diferencias claras entre el músculo enfermo y el sano. RNAscope mostró que los músculos de los pacientes con DMD contenían menos transcritos de distrofina—los mensajes de ARN necesarios para producir la proteína distrofina que falta—que la muestra sana. Las señales restantes también variaron en tamaño según qué parte del gen se dirigiera, lo que sugiere diferencias en el procesamiento del largo mensaje de la distrofina. Mientras tanto, las imágenes multiphotón mostraron que los músculos con DMD estaban llenos de fibras de colágeno largas y densas, una señal visual de cicatrización fibrótica, mientras que el músculo sano tenía fibras menos numerosas y más distribuidas. Estos hallazgos coinciden con la experiencia clínica: en la DMD, el tejido muscular se reemplaza gradualmente por grasa y cicatriz.
Panorámica: patrones amplios en el tejido
Tras registrar digitalmente los dos tipos de imagen, el equipo dividió cada sección de tejido en una cuadrícula, tratando cada cuadrado como un vecindario diminuto. En cada casilla midieron tanto características del colágeno—longitud de las fibras, orientación y qué tan sinuosas o rectas estaban—como la densidad local de puntos de ARN de distrofina. Esta vista tipo “mapa de calor” reveló variación parcheada, de región a región, tanto en la actividad génica como en la estructura del colágeno dentro del músculo con DMD. Sin embargo, cuando estas medidas se compararon mediante pruebas estadísticas, la abundancia de transcritos y las propiedades del colágeno mostraron casi ninguna relación consistente a esta escala gruesa. En otras palabras, al promediar sobre regiones relativamente grandes, las áreas ricas en ARN de distrofina no resultaron ser sistemáticamente más ni menos fibróticas que las áreas con menos señales de ARN.
Acercamiento: relaciones a escala celular
Los resultados más reveladores surgieron cuando los científicos se centraron en vecindarios medidos en solo unas decenas de micrómetros—aproximadamente el tamaño de fibras musculares individuales y sus alrededores inmediatos. Para cada punto de ARN trazaron una serie de círculos concéntricos crecientes y contabilizaron cuántas fibras de colágeno había dentro y cuál era la longitud de esas fibras. Tanto en tejidos con DMD como en tejidos sanos, las fibras de colágeno eran más largas justo al lado de las señales de ARN de distrofina y se hacían progresivamente más cortas a medida que aumentaba la distancia. En las muestras con cicatrización más severa, los puntos de transcrito casi siempre tenían colágeno cercano, incluso a distancias muy pequeñas, mientras que en la muestra sana muchos puntos de ARN se encontraban en regiones con poco o ningún colágeno cercano. Análisis de control usando puntos colocados al azar y ajustes ligeros en el procesamiento de imágenes mostraron que este patrón no podía explicarse simplemente por azar ni por peculiaridades del software.
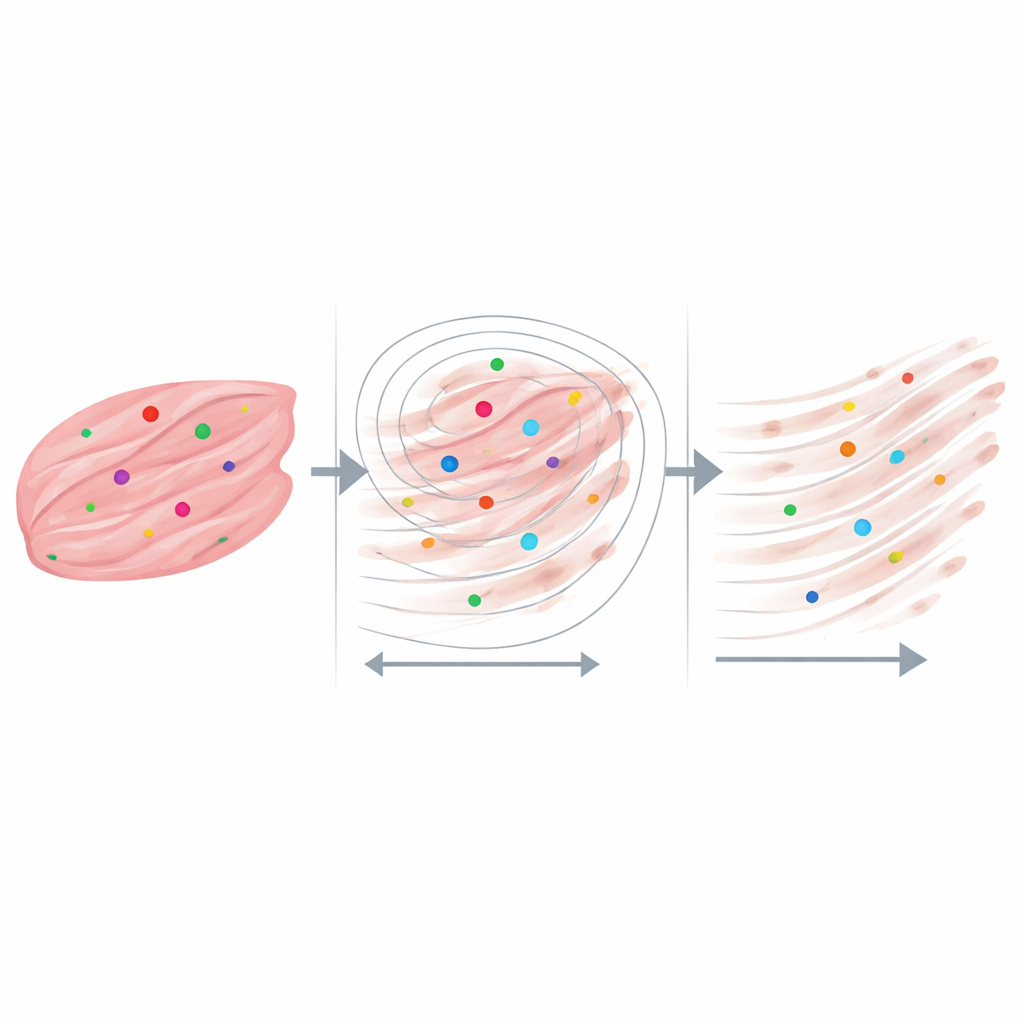
Qué podría significar esto para la enfermedad muscular y más allá
Estos hallazgos sugieren que los vínculos importantes entre los mensajes génicos y la estructura del tejido pueden permanecer ocultos si solo se observan promedios amplios, pero se hacen visibles cuando se examinan a nivel celular. En este estudio de prueba de concepto, las regiones enriquecidas en transcritos específicos de distrofina tendían a ubicarse cerca de fibras de colágeno más largas y densas, lo que indica que la actividad génica local y la remodelación fibrótica podrían influenciarse mutuamente dentro de microambientes microscópicos del músculo. Los autores enfatizan que su grupo de pacientes es pequeño y que el trabajo aún no es una prueba clínica. En cambio, presentan una plataforma flexible que puede extenderse a otros genes, tipos de tejido y métodos de imagen. Al vincular dónde están activos los genes y cómo se construye el andamiaje del tejido, este enfoque abre la puerta al descubrimiento de nuevos biomarcadores espaciales de fibrosis, regeneración y respuestas a terapias emergentes basadas en ARN.
Cita: Scodellaro, R., Mietto, M., Ferlini, A. et al. Correlative multimodal imaging for microscale spatial mapping of collagen-gene activity interactions in human tissues. npj Imaging 4, 17 (2026). https://doi.org/10.1038/s44303-026-00149-8
Palabras clave: imagen multimodal, distrofia muscular de Duchenne, fibrosis por colágeno, expresión génica espacial, biopsia de músculo esquelético